名校
解题方法
1 . 中和反应是一类重要的化学反应,兴趣小组利用图1研究稀盐酸与氢氧化钠溶液反应的过程,并用pH和电导率传感器测定反应过程中pH和电导率的变化(如图2和图3),下列说法错误的是(电导率越大,导电性越强)
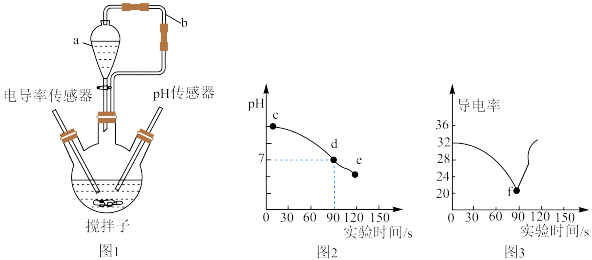
| A.图1中通过仪器a和橡皮管b可以控制液体滴加的速度 |
| B.图2中c→d能证明稀盐酸和氢氧化钠溶液发生了化学反应 |
| C.图2中的e点所示溶液中的溶质是NaCl和HCl |
| D.图3中90s之前电导率下降是因为生成的电解质不能电离 |
您最近一年使用:0次
2023-11-14更新
|
152次组卷
|
3卷引用:吉林省长春市第二实验中学2023-2024学年高一上学期期中考试化学试题
解题方法
2 . 某化学兴趣小组同学利用以下装置制备干燥的氯气并对氯气的性质进行探究。
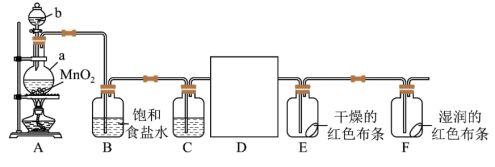
(1)A装置中b仪器名称_____ 。
(2)仪器a中发生反应的离子方程式为_____ ,D为收集干燥的氯气仪器,可以选择_____ (填序号)。

(3)下列有关该实验的说法中不正确的是______ (填字母)。
a.B中饱和食盐水主要作用之一是除去氯气中的氯化氢气体
b.C中试剂是浓硫酸,目的是干燥氯气
c.E中红色布条不褪色,F中红色布条褪色,证明氯气具有漂白性
d.尾气处理时,所用试剂可以选用澄清石灰水
(4)新冠肺炎疫情期间,“84消毒液”被广泛应用于物体表面杀菌消毒。制备“84消毒液”的化学反应方程式为______ 。
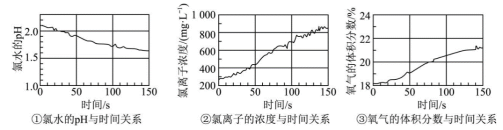
(5)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:_____ 。
(6)该兴趣小组在40℃条件下,将一定量的Cl2通入一定量的NaOH溶液中,得到的产物中含有NaCl、NaClO和NaClO3,已知Cl-和ClO-的个数比为8:3,则此过程中氧化剂和还原剂的个数之比为_____ 。

(1)A装置中b仪器名称
(2)仪器a中发生反应的离子方程式为

(3)下列有关该实验的说法中不正确的是
a.B中饱和食盐水主要作用之一是除去氯气中的氯化氢气体
b.C中试剂是浓硫酸,目的是干燥氯气
c.E中红色布条不褪色,F中红色布条褪色,证明氯气具有漂白性
d.尾气处理时,所用试剂可以选用澄清石灰水
(4)新冠肺炎疫情期间,“84消毒液”被广泛应用于物体表面杀菌消毒。制备“84消毒液”的化学反应方程式为
(5)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:

(6)该兴趣小组在40℃条件下,将一定量的Cl2通入一定量的NaOH溶液中,得到的产物中含有NaCl、NaClO和NaClO3,已知Cl-和ClO-的个数比为8:3,则此过程中氧化剂和还原剂的个数之比为
您最近一年使用:0次
名校
3 . 下列说法中正确的是
A.某酸性溶液中: 、 、 、 、 、 、 能大量共存 能大量共存 |
B.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 能大量共存 能大量共存 |
C.某透明溶液中: 、 、 、 、 、 、 可能大量共存 可能大量共存 |
D.取少量某溶液,向其中加入盐酸酸化的 溶液,观察到有白色沉淀生成,则证明该溶液中含有 溶液,观察到有白色沉淀生成,则证明该溶液中含有 |
您最近一年使用:0次
2021-12-12更新
|
739次组卷
|
4卷引用:吉林省吉林松花江中学2022-2023学年高一上学期1月期末考试化学试题
名校
4 . 硅是大数据时代的关键材料。工业上常在1800—2000℃时,用碳单质还原的方法制取单质硅。涉及反应的相关数据如表所示。下列相关说法正确的是
| 反应 | △H/(kJ•mol-1) | △S/(J•K-1•mol-1) |
| 反应(1):SiO2(s)+2C(s)=Si(s)+2CO(g) | 687.27 | 359.04 |
| 反应(2):SiO2(s)+C(s)=Si(s)+CO2(g) | 514.85 | 183.35 |
| A.反应(1)可证明Si的还原性大于C |
| B.生活中利用单晶硅良好的导光性能做光导纤维 |
| C.工业生产条件下反应(2)无法自发进行发生 |
| D.C(s)+CO2(g)=2CO(g) △H=-172.42kJ·mol-1 |
您最近一年使用:0次
2022-01-08更新
|
1344次组卷
|
6卷引用:吉林省通化市梅河口市第五中学2023-2024学年高二上学期第三次月考化学试题
吉林省通化市梅河口市第五中学2023-2024学年高二上学期第三次月考化学试题河南省郑州市2022届高三上学期第一次质量预测(1月)化学试题河南省郑州市第四高级中学2021-2022学年高二下学期第二次调研考试西藏班化学试题(已下线)专题04氧化还原反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题04氧化还原反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题04氧化还原反应-三年(2020~2022)高考真题汇编(全国卷)
名校
5 . 下列有关说法不正确的是
| A.碳原子间能形成单键、双键或三键,多个碳原子也可以构成碳链或碳环 |
B.分子式为 的有机化合物一定为丙烯 的有机化合物一定为丙烯 |
| C.甲烷的二氯代物只有一种证明甲烷为正四面体结构 |
| D.钠与乙醇反应比水的缓和,说明受乙基影响,醇羟基中H原子活泼性减弱 |
您最近一年使用:0次
2021-07-11更新
|
518次组卷
|
4卷引用:吉林省白山市抚松县第一中学2021-2022学年高二下学期第一次月考(平行班)化学试题
名校
解题方法
6 . 根据氨气溶于水的喷泉实验,以下说法不正确的是
| A.该实验证明氨气极易溶于水 |
| B.烧瓶中充满氯气,胶头滴管和烧杯中加入浓碱液也可能形成喷泉 |
| C.烧杯中换成其他液体无法形成喷泉 |
| D.红色喷泉说明氨水显碱性 |
您最近一年使用:0次
2021-05-08更新
|
1133次组卷
|
10卷引用:长春市榆树高级中学2020-2021学年高一下学期期中考试化学试题
长春市榆树高级中学2020-2021学年高一下学期期中考试化学试题辽宁省大连市第一中学2020-2021学年高一下学期期中(合格性)考试化学试题人教2019版必修第二册第五章第二节 氮及其化合物课后习题甘肃省民乐县第一中学2021-2022学年高一下学期3月第一次月考化学试题新疆和田地区洛浦县第一中学2021-2022学年高一下学期3月月考化学试题黑龙江省饶河县高级中学2021-2022学年高一下学期学业水平(合格考)化学试题7.2.1氨气(课后)-2019苏教版必修2课前课中课后新疆阿克苏市实验中学2022-2023学年高一下学期第二次月考化学试题云南省红河哈尼族彝族自治州第一中学2023-2024学年高一下学期3月月考化学试题四川省甘孜藏族自治州某重点中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
7 . 2023 年诺贝尔化学奖授予发现量子点的三位科学家,量子点的尺寸一般在1 nm~10 nm之间,是一种纳米级别的半导体。量子点的尺寸不同,则发光颜色不同,吸收光谱波长不同。实验室一种制备CdSe量子点的方法如下:
一、CdSe量子点前驱体的制备
Ⅰ.N2气氛中,取1 mmol Se粉于三颈烧瓶中,加入15 mL的十八烯溶剂,加热到280℃,Se粉完全溶解形成橙色透明溶液;
Ⅱ.N2气氛中,将1 mmol CdCl2溶于4 mL油酸,加热至120℃,使CdCl2完全溶于油酸,形成油酸镉澄清液体。
二、CdSe量子点的生长与制备
Ⅲ.将步骤Ⅱ中制备好的油酸镉溶液注射至步骤Ⅰ中含有Se粉的三颈烧瓶中,如下图所示,保持反应温度为260℃,反应45min。
Ⅳ.待反应液冷却后,加入20 mL乙醇溶液,CdSe析出,离心分离,加入正己烷分散后,再次加入乙醇,离心分离,重复2~3次后,用乙醇和丙酮洗涤 CdSe,即可得到干净的CdSe量子点。
回答下列问题:
(1)Cd为第五周期ⅡB族,则Cd的价层电子排布式为___________ 。
(2)步骤Ⅱ中N2的作用为___________ ,油酸与镉配位的原子为___________ 。
(3)Se的一种制备方法如下:向Na2SeO3水溶液中加入 进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为
进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为___________ ;此方法获得Se单质过程中无需使用的仪器是___________ (填名称)。___________ 现象时,证明CdSe量子点生长基本停止,制备完成。除此方法外,还可利用___________ 物理现象初步鉴定CdSe量子点制备成功。
(5)步骤Ⅳ中加入20 mL乙醇的作用是___________ 。
(6)CdSe洗涤干净的标志是___________ 。
一、CdSe量子点前驱体的制备
Ⅰ.N2气氛中,取1 mmol Se粉于三颈烧瓶中,加入15 mL的十八烯溶剂,加热到280℃,Se粉完全溶解形成橙色透明溶液;
Ⅱ.N2气氛中,将1 mmol CdCl2溶于4 mL油酸,加热至120℃,使CdCl2完全溶于油酸,形成油酸镉澄清液体。
二、CdSe量子点的生长与制备
Ⅲ.将步骤Ⅱ中制备好的油酸镉溶液注射至步骤Ⅰ中含有Se粉的三颈烧瓶中,如下图所示,保持反应温度为260℃,反应45min。
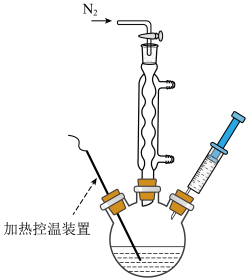
Ⅳ.待反应液冷却后,加入20 mL乙醇溶液,CdSe析出,离心分离,加入正己烷分散后,再次加入乙醇,离心分离,重复2~3次后,用乙醇和丙酮洗涤 CdSe,即可得到干净的CdSe量子点。
回答下列问题:
(1)Cd为第五周期ⅡB族,则Cd的价层电子排布式为
(2)步骤Ⅱ中N2的作用为
(3)Se的一种制备方法如下:向Na2SeO3水溶液中加入
 进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为
进行还原,得Se单质,过滤,洗涤,干燥,静置。制备过程中,会产生一种对环境无污染的气体,则该反应的离子方程式为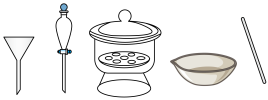
(5)步骤Ⅳ中加入20 mL乙醇的作用是
(6)CdSe洗涤干净的标志是
您最近一年使用:0次
2024-05-11更新
|
142次组卷
|
3卷引用:2024届东北三省四市教研联合体高三下学期高考模拟(二)化学试卷
名校
解题方法
8 . 还原铁粉与水蒸气的反应装置如图所示。取少量反应后的固体加入稀硫酸使其完全溶解得溶液a;另取少量反应后的固体加入稀硝酸使其完全溶解,得溶液b.下列说法正确的是
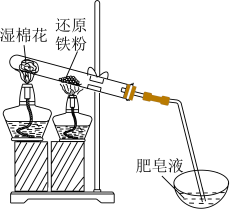
A.铁与水蒸气反应: |
B.肥皂液中产生气泡,不能证明铁与水蒸气反应生成 |
C.向溶液a中滴加 溶液,出现蓝色沉淀,说明铁粉未完全反应 溶液,出现蓝色沉淀,说明铁粉未完全反应 |
D.向溶液b中滴加 溶液,溶液变红,证实了固体中含有 溶液,溶液变红,证实了固体中含有 |
您最近一年使用:0次
2024-04-10更新
|
1081次组卷
|
6卷引用:2024年东北三省四校高三下学期第四次模拟考试化学试卷
(已下线)2024年东北三省四校高三下学期第四次模拟考试化学试卷北京市西城区2024届高三统一测试(一模)化学试题(已下线)题型6 元素及其化合物 化学实验基础(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届河南省焦作市博爱县第一中学高三下学期三模化学试题(已下线)化学(北京卷03)-2024年高考押题预测卷东北三省三校2023-2024学年高三四模化学试卷
解题方法
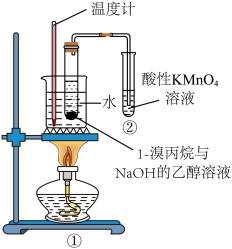
9 . 某化学兴趣小组设计实验探究1-溴丙烷的消去反应,实验装置如图所示。按要求回答下列问题:___________ 。
(2)甲同学认为装置②中酸性 溶液褪色即可说明1-溴丙烷发生了消去反应,乙同学认为装置②中酸性
溶液褪色即可说明1-溴丙烷发生了消去反应,乙同学认为装置②中酸性 溶液褪色并不能说明1-溴丙烷发生了消去反应,因为
溶液褪色并不能说明1-溴丙烷发生了消去反应,因为___________ 。
(3)丙同学认为把装置②中的酸性 溶液用溴的
溶液用溴的 溶液替换,若溴的
溶液替换,若溴的 溶液褪色,则可说明1-溴丙烷发生了消去反应,此时装置②中反应的化学方程式为
溶液褪色,则可说明1-溴丙烷发生了消去反应,此时装置②中反应的化学方程式为___________ 。
(4)实验结束后,丁同学取少量装置①试管中反应后的溶液于另一试管中,___________ (请填写实验过程和现象),证明装置①试管中反应后的溶液中含有 。丁同学认为根据该现象也可说明1-溴丙烷发生了消去反应。你
。丁同学认为根据该现象也可说明1-溴丙烷发生了消去反应。你___________ (填“认同”或“不认同”)丁同学的判断。
(5)该小组成员在观察试剂瓶上标签中对1-溴丙烷的描述时,发现其中含有极少量2-溴丙烷、写出2-溴丙烷发生消去反应的化学方程式:___________ 。
(6)根据该实验的启发,该小组成员设计了用1-溴丙烷经过三步反应制得1,2-丙二醇的合成路线,试写出第三步反应的化学方程式:___________ 。
(2)甲同学认为装置②中酸性
 溶液褪色即可说明1-溴丙烷发生了消去反应,乙同学认为装置②中酸性
溶液褪色即可说明1-溴丙烷发生了消去反应,乙同学认为装置②中酸性 溶液褪色并不能说明1-溴丙烷发生了消去反应,因为
溶液褪色并不能说明1-溴丙烷发生了消去反应,因为(3)丙同学认为把装置②中的酸性
 溶液用溴的
溶液用溴的 溶液替换,若溴的
溶液替换,若溴的 溶液褪色,则可说明1-溴丙烷发生了消去反应,此时装置②中反应的化学方程式为
溶液褪色,则可说明1-溴丙烷发生了消去反应,此时装置②中反应的化学方程式为(4)实验结束后,丁同学取少量装置①试管中反应后的溶液于另一试管中,
 。丁同学认为根据该现象也可说明1-溴丙烷发生了消去反应。你
。丁同学认为根据该现象也可说明1-溴丙烷发生了消去反应。你(5)该小组成员在观察试剂瓶上标签中对1-溴丙烷的描述时,发现其中含有极少量2-溴丙烷、写出2-溴丙烷发生消去反应的化学方程式:
(6)根据该实验的启发,该小组成员设计了用1-溴丙烷经过三步反应制得1,2-丙二醇的合成路线,试写出第三步反应的化学方程式:
您最近一年使用:0次
解题方法
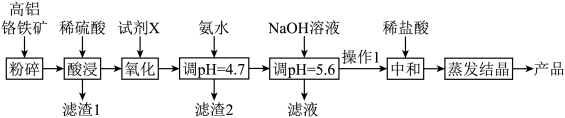
10 . CrCl3是重要的化工试剂,用高铝铬铁矿(主要含Cr2O3和Al2O3,还含Fe2O3、FeO、MgO、SiO2)制取CrCl3的流程如下:
已知:①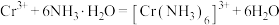
②相关金属离子在不同浓度下生成氢氧化物沉淀的 如图:
如图:
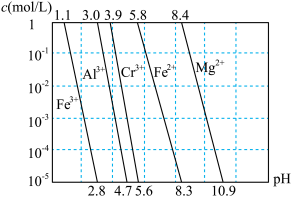
回答下列问题
(1)滤渣1主要成分是___________ ,滤渣2主要成分是___________ 。
(2)试剂X可选用___________ ,简述该流程设计添加X的好处与不好之处,好处是___________ ,不好之处是___________ 。
(3)“操作I”为过滤、洗涤,则证明沉淀洗涤干净的操作方法是___________ 。
(4)蒸发结晶操作应在___________ 条件下进行
(5)硼化铬(CrB)可用作耐磨、抗高温氧化涂层和核反应堆中的中子吸收涂层,硼化铬是在650℃时由金属镁与硼、氯化铬的混合物制得的,写出该反应的化学方程式:___________ 。

已知:①
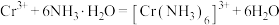
②相关金属离子在不同浓度下生成氢氧化物沉淀的
 如图:
如图:
回答下列问题
(1)滤渣1主要成分是
(2)试剂X可选用
(3)“操作I”为过滤、洗涤,则证明沉淀洗涤干净的操作方法是
(4)蒸发结晶操作应在
(5)硼化铬(CrB)可用作耐磨、抗高温氧化涂层和核反应堆中的中子吸收涂层,硼化铬是在650℃时由金属镁与硼、氯化铬的混合物制得的,写出该反应的化学方程式:
您最近一年使用:0次



