名校
解题方法
1 . 教师在课堂上通过以下装置对原电池的原理和形成条件开展了实验探究,结合探究判断下列说法不正确 的是
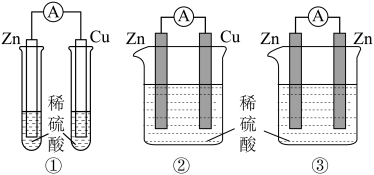
| A.通过装置①金属表面是否产生气泡,可证明Zn比Cu活泼 |
| B.对比①②中Cu片上是否有气泡,可预测②中电流表指针会偏转 |
| C.装置②③对比实验的目的是:探究原电池电极材料应满足的条件 |
D.装置③能形成原电池,正极的电极反应式为: |
您最近一年使用:0次
2023-07-12更新
|
263次组卷
|
4卷引用:云南省云南师范大学实验中学2023-2024学年高一下学期三月月考化学试题
名校
解题方法
2 . 根据氨气溶于水的喷泉实验,以下说法不正确的是
| A.该实验证明氨气极易溶于水 |
| B.烧瓶中充满氯气,胶头滴管和烧杯中加入浓碱液也可能形成喷泉 |
| C.烧杯中换成其他液体无法形成喷泉 |
| D.红色喷泉说明氨水显碱性 |
您最近一年使用:0次
2021-05-08更新
|
1133次组卷
|
10卷引用:云南省红河哈尼族彝族自治州第一中学2023-2024学年高一下学期3月月考化学试题
云南省红河哈尼族彝族自治州第一中学2023-2024学年高一下学期3月月考化学试题长春市榆树高级中学2020-2021学年高一下学期期中考试化学试题辽宁省大连市第一中学2020-2021学年高一下学期期中(合格性)考试化学试题人教2019版必修第二册第五章第二节 氮及其化合物课后习题甘肃省民乐县第一中学2021-2022学年高一下学期3月第一次月考化学试题新疆和田地区洛浦县第一中学2021-2022学年高一下学期3月月考化学试题黑龙江省饶河县高级中学2021-2022学年高一下学期学业水平(合格考)化学试题7.2.1氨气(课后)-2019苏教版必修2课前课中课后新疆阿克苏市实验中学2022-2023学年高一下学期第二次月考化学试题四川省甘孜藏族自治州某重点中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
3 . 同学们探究不同金属和浓硫酸的反应。向三等份浓硫酸中分别加入大小相同的不同金属片,加热,用生成气体进行下表实验操作并记录实验现象。
已知: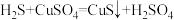 (CuS为黑色固体);
(CuS为黑色固体); 可燃
可燃
下列说法不正确 的是
| 实验操作 | 实验现象 | ||
| 金属为铜 | 金属为锌 | 金属为铝 | |
| 点燃 | 不燃烧 | 燃烧 | 燃烧 |
通入 酸性溶液 酸性溶液 | 褪色 | 褪色 | 褪色 |
通入 溶液 溶液 | 无明显变化 | 无明显变化 | 出现黑色沉淀 |
| 通入品红溶液 | 褪色 | 褪色 | 不褪色 |
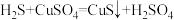 (CuS为黑色固体);
(CuS为黑色固体); 可燃
可燃下列说法
A.加入铜片的实验中,使 酸性溶液褪色的气体是 酸性溶液褪色的气体是 |
B.加入铝片的实验中,燃烧现象能证明生成气体中一定含 |
| C.加入锌片的实验中,生成的气体一定是混合气体 |
| D.金属与浓硫酸反应的还原产物与金属活动性强弱有关 |
您最近一年使用:0次
2021-05-10更新
|
1559次组卷
|
16卷引用:云南省昆明市第一中学2022-2023学年高一下学期期中考试化学试题
云南省昆明市第一中学2022-2023学年高一下学期期中考试化学试题北京市海淀区2021届高三二模化学试题(已下线)2021年高考化学押题预测卷(北京卷)(02)(已下线)第13讲 硫及其化合物(精练)-2022年高考化学一轮复习讲练测(已下线)专题12 硫及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练北京首都师范大学附属中学2021-2022学年高三上学期10月月考化学试题辽宁省沈阳市东北育才学校2021-2022学年高三上学期学段考试化学试题北京市北京师范大学附属实验中学2021-2022学年高一下学期期中考试化学试题北京师范大学附属实验中学2021-2022学年高一下学期期中考试化学试题趋势4 创新探究类实验(已下线)第四章 非金属及其化合物 第21练 硫酸 含硫物质的转化北京市房山区2022-2023学年高三二模化学试题广东省广州市番禺中学2022-2023学年高一下学期4月期中考试化学试题(已下线)第4讲 浓硫酸 不同价态含硫物质的转化北京市中国人民大学附属中学2023-2024学年高三下学期一模模拟化学试题北京市第八十中学2023-2024学年高一下学期期中考试化学(选考)试题
4 . 化学实验源于生活。下列实验方案设计、现象与结论均正确的是
| 选项 | 实验目的 | 实验方案 | 现象和结论 |
| A | 检验葡萄糖中是否含有醛基 | 向葡萄糖溶液中滴加少量酸性高锰酸钾溶液,观察高锰酸钾溶液是否褪色 | 若溶液褪色,说明葡萄糖中含有醛基 |
| B | 比较常温下 和 和 溶度积的大小 溶度积的大小 | 向5 mL 0.2 mol/L NaOH溶液中滴加4滴0.2 mol/L  溶液,充分振荡,再滴加8滴0.2 mol/L 溶液,充分振荡,再滴加8滴0.2 mol/L  溶液 溶液 | 若溶液中出现白色沉淀,之后又出现蓝色沉淀,说明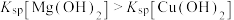 |
| C | 比较N和Cl的非金属性的强弱 | 分别取等浓度的 溶液和HClO溶液,用玻璃棒蘸取后点于pH试纸中部,与标准比色卡比较 溶液和HClO溶液,用玻璃棒蘸取后点于pH试纸中部,与标准比色卡比较 | 证明N的非金属性比Cl的弱 |
| D | 验证乙酸乙酯在碱性条件下可以水解 | 向盛有1mL乙酸乙酯的a、b两支试管中分别加入2 mL 、2 mL NaOH溶液,70~80℃热水浴 、2 mL NaOH溶液,70~80℃热水浴 | 若试管a液体分层,酯层无明显变化;试管b酯层消失,说明乙酸乙酯在碱性条件下可以水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 根据措施或事实,下列有关解释错误的是
| 选项 | 措施或事实 | 相关解释 |
| A | Na着火不能用CO2灭火 | Na会与CO2反应生成O2 |
| B | 在实验室配制Na2S溶液时,常滴加几滴NaOH浓溶液 | 抑制 的水解 的水解 |
| C | 当面粉在相对密闭的空间内悬浮在空气中达到一定浓度时,遇火会发生爆炸 | 增大接触面积,可加快化学反应速率 |
| D | 工业盐酸因含 呈亮黄色,为证明这种配离子只有在高浓度 呈亮黄色,为证明这种配离子只有在高浓度 条件下才稳定,可向其中滴加AgNO3溶液观察现象 条件下才稳定,可向其中滴加AgNO3溶液观察现象 | 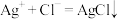 ,AgNO3可有效降低 ,AgNO3可有效降低 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
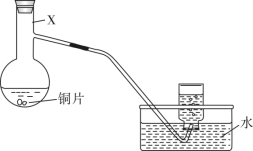
6 . 某小组利用如下装置(夹持装置略),探究浓、稀硝酸与铜反应的气体产物。回答下列问题:___________ 。
(2)请写出稀硝酸与铜反应的离子方程式___________ 。
(3)为节约药品用量,有人建议用具支试管(下图)代替仪器X,用试管代替集气瓶。为方便控制铜与硝酸反应的发生和停止,改进措施是___________ ;用改进后的装置进行铜与浓硝酸反应的实验,具支试管中产生的气体和排水收集到的气体___________ (填“相同”“不相同”)。 ,
, 仅得到一个
仅得到一个 ,稀硝酸与铜反应生成NO,
,稀硝酸与铜反应生成NO, 得到三个
得到三个 ,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较
,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较___________ ;角度二:同一种还原剂能被浓硝酸氧化,不能被稀硝酸氧化。根据角度二设计了如下装置,用以证明浓硝酸和稀硝酸的氧化性强弱关系。 ,目的是
,目的是___________ ;滴加浓硝酸后,当③中为稀硝酸时,其液面上方气体仍为无色;当③中为浓硝酸时,其液面上方气体由无色变为红棕色,反应的化学方程式为___________ 。
(5)有人提出(4)中角度二的验证实验不够简约,可将之前排水集气收集满NO的两支试管用橡胶塞塞紧,为防止气体逸出产生污染,在不取下胶塞的情况下向试管中分别加入稀硝酸、浓硝酸,简述其加入稀硝酸、浓硝酸的方法___________ 。
(2)请写出稀硝酸与铜反应的离子方程式
(3)为节约药品用量,有人建议用具支试管(下图)代替仪器X,用试管代替集气瓶。为方便控制铜与硝酸反应的发生和停止,改进措施是
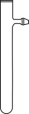
 ,
, 仅得到一个
仅得到一个 ,稀硝酸与铜反应生成NO,
,稀硝酸与铜反应生成NO, 得到三个
得到三个 ,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较
,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较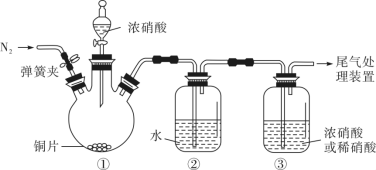
 ,目的是
,目的是(5)有人提出(4)中角度二的验证实验不够简约,可将之前排水集气收集满NO的两支试管用橡胶塞塞紧,为防止气体逸出产生污染,在不取下胶塞的情况下向试管中分别加入稀硝酸、浓硝酸,简述其加入稀硝酸、浓硝酸的方法
您最近一年使用:0次
解题方法
7 . 在化学学习中,我们经常利用实验现象或者数据来证明物质的性质,下列叙述正确的是
①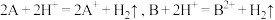 ,则证明
,则证明 的金属性强于
的金属性强于
②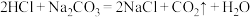 ,则证明
,则证明 的非金属性强于
的非金属性强于
③ 的最简单氢化物的热稳定性强于
的最简单氢化物的热稳定性强于 ,则证明
,则证明 的非金属性强于
的非金属性强于
④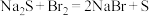 ,则证明
,则证明 的非金属性强于S
的非金属性强于S
⑤单质X比Y的熔沸点高,则证明X的非金属性强与Y
①
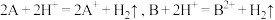 ,则证明
,则证明 的金属性强于
的金属性强于
②
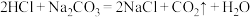 ,则证明
,则证明 的非金属性强于
的非金属性强于
③
 的最简单氢化物的热稳定性强于
的最简单氢化物的热稳定性强于 ,则证明
,则证明 的非金属性强于
的非金属性强于
④
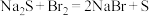 ,则证明
,则证明 的非金属性强于S
的非金属性强于S⑤单质X比Y的熔沸点高,则证明X的非金属性强与Y
| A.②④ | B.②③⑤ | C.①③④ | D.③④ |
您最近一年使用:0次
解题方法
8 . 人体必需的部分元素在周期表中的分布情况如下:
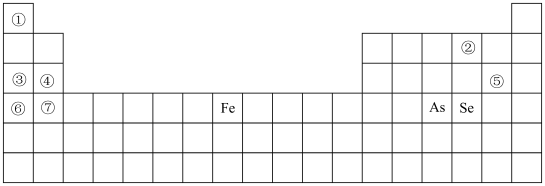
请根据以上信息回答下列问题:
(1)元素③能维持人体水分平衡、酸碱平衡等,元素③在周期表中的位置为___________ 。
(2)人体缺元素⑦会导致腿软、抽筋、乏力、烦躁、精力不集中等症状,牛奶中含有大量的元素⑦,有利于骨骼健康。根据元素⑦在周期表中的位置预测牛奶中的元素⑦以___________ 形式存在。(填“离子”或“单质”)
(3)硒(Se)元素对人体的抗衰老具有很好的作用,同时能增强人体免疫力、抵抗力,具有抗癌、抗肿瘤等功效,元素Se的两种核素 、
、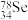 互称为
互称为___________ 。
(4)人体中的①元素通过选择性清除恶性自由基,保护细胞分裂分化,达到抗细胞变异和抗癌变的效果,请写出元素①与元素②组成的含10个电子的分子的电子式:___________ 。
(5)人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血,某种市售营养麦片中含有微量的铁粉,请写出铁粉在胃酸(主要成分HCl)中发生反应的离子方程式___________ 。
(6)适量的砷(As)有助于血红蛋白的合成,能够促进人体的生长发育,如果使用不当,砷对人体的危害就会非常的大,根据砷在周期表中位置预测非金属性As___________ Se(填“>”“<”或“=”)。
(7)人体应减少铝元素的摄入,铝元素可导致脑组织退行性病变,诱发老年痴呆等脑病,请写出铝与NaOH溶液反应的化学方程式___________ 。
(8)以上周期表信息中元素的最高价氧化物对应水化物酸性最强的是___________ (填化学式)
(9)下列不能证明元素⑥的金属性比④强的事实有___________ 。
a.元素⑥的原子最外层电子数比元素④的原子最外层电子数少。
b.⑥的单质能与冷水剧烈反应而④的单质不能
c.⑥的最高价氧化物对应水化物的碱性比④强

请根据以上信息回答下列问题:
(1)元素③能维持人体水分平衡、酸碱平衡等,元素③在周期表中的位置为
(2)人体缺元素⑦会导致腿软、抽筋、乏力、烦躁、精力不集中等症状,牛奶中含有大量的元素⑦,有利于骨骼健康。根据元素⑦在周期表中的位置预测牛奶中的元素⑦以
(3)硒(Se)元素对人体的抗衰老具有很好的作用,同时能增强人体免疫力、抵抗力,具有抗癌、抗肿瘤等功效,元素Se的两种核素
 、
、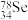 互称为
互称为(4)人体中的①元素通过选择性清除恶性自由基,保护细胞分裂分化,达到抗细胞变异和抗癌变的效果,请写出元素①与元素②组成的含10个电子的分子的电子式:
(5)人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血,某种市售营养麦片中含有微量的铁粉,请写出铁粉在胃酸(主要成分HCl)中发生反应的离子方程式
(6)适量的砷(As)有助于血红蛋白的合成,能够促进人体的生长发育,如果使用不当,砷对人体的危害就会非常的大,根据砷在周期表中位置预测非金属性As
(7)人体应减少铝元素的摄入,铝元素可导致脑组织退行性病变,诱发老年痴呆等脑病,请写出铝与NaOH溶液反应的化学方程式
(8)以上周期表信息中元素的最高价氧化物对应水化物酸性最强的是
(9)下列不能证明元素⑥的金属性比④强的事实有
a.元素⑥的原子最外层电子数比元素④的原子最外层电子数少。
b.⑥的单质能与冷水剧烈反应而④的单质不能
c.⑥的最高价氧化物对应水化物的碱性比④强
您最近一年使用:0次
名校
解题方法
9 . 焦亚硫酸钠 是工业上常用的抗氧化剂。一种湿法制备
是工业上常用的抗氧化剂。一种湿法制备 的生产工艺如下:
的生产工艺如下:

回答下列问题:
(1) 中硫元素的化合价为
中硫元素的化合价为___________ 。
(2)反应1中通入NH3和CO2的顺序为___________ 。
(3)关于上述流程,下列说法正确的是___________(填字母)。
(4)工业上添加 作抗氧化剂时会放出一种有刺激性气味的气体。实验室检验该气体的常用试剂是
作抗氧化剂时会放出一种有刺激性气味的气体。实验室检验该气体的常用试剂是___________ 。
(5)溶液A中阳离子有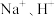 和X离子。检验X离子的操作和现象是
和X离子。检验X离子的操作和现象是___________ 。
(6)获得 需要经过多步反应,其中包括反应3制备
需要经过多步反应,其中包括反应3制备 溶液,然后加入
溶液,然后加入 溶液调
溶液调 转化为
转化为 溶液,再通入
溶液,再通入 生成
生成 ,当溶液中
,当溶液中 含量达到过饱和浓度时,析出
含量达到过饱和浓度时,析出 晶体,反应方程式为
晶体,反应方程式为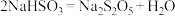 。
。
①反应3的化学方程式为___________ 。
②加入 转化为
转化为 的离子方程式为
的离子方程式为___________ 。
(7)工业上可用焦亚硫酸钠 处理含有
处理含有 的酸性废水,使其转化为毒性较低的
的酸性废水,使其转化为毒性较低的 ,理论上处理
,理论上处理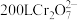 浓度为
浓度为 的废水需要焦亚硫酸钠
的废水需要焦亚硫酸钠___________ g。
 是工业上常用的抗氧化剂。一种湿法制备
是工业上常用的抗氧化剂。一种湿法制备 的生产工艺如下:
的生产工艺如下:
回答下列问题:
(1)
 中硫元素的化合价为
中硫元素的化合价为(2)反应1中通入NH3和CO2的顺序为
(3)关于上述流程,下列说法正确的是___________(填字母)。
| A.该流程中,CO2可以循环使用 |
| B.反应2为分解反应 |
| C.反应3证明硫的非金属性比碳的强 |
D.氨气溶于水使溶液呈碱性的原因是存在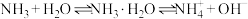 反应 反应 |
(4)工业上添加
 作抗氧化剂时会放出一种有刺激性气味的气体。实验室检验该气体的常用试剂是
作抗氧化剂时会放出一种有刺激性气味的气体。实验室检验该气体的常用试剂是(5)溶液A中阳离子有
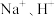 和X离子。检验X离子的操作和现象是
和X离子。检验X离子的操作和现象是(6)获得
 需要经过多步反应,其中包括反应3制备
需要经过多步反应,其中包括反应3制备 溶液,然后加入
溶液,然后加入 溶液调
溶液调 转化为
转化为 溶液,再通入
溶液,再通入 生成
生成 ,当溶液中
,当溶液中 含量达到过饱和浓度时,析出
含量达到过饱和浓度时,析出 晶体,反应方程式为
晶体,反应方程式为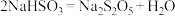 。
。①反应3的化学方程式为
②加入
 转化为
转化为 的离子方程式为
的离子方程式为(7)工业上可用焦亚硫酸钠
 处理含有
处理含有 的酸性废水,使其转化为毒性较低的
的酸性废水,使其转化为毒性较低的 ,理论上处理
,理论上处理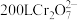 浓度为
浓度为 的废水需要焦亚硫酸钠
的废水需要焦亚硫酸钠
您最近一年使用:0次
2023-12-18更新
|
142次组卷
|
2卷引用:云南省楚雄东兴中学2023-2024学年高三上学期10月月考化学试题
解题方法
10 . 某实验小组欲探究硝酸氧化草酸溶液的气体产物及测定出草酸中碳的含量,设计装置如图所示(加热和仪器固定装置均已略去),回答下列问题:
已知:
Ⅰ.硝酸氧化草酸溶液: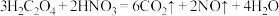 。
。
Ⅱ.控制反应液温度为55~60℃,边搅拌边滴加含有适量催化剂的混酸( 与
与 )溶液。
)溶液。
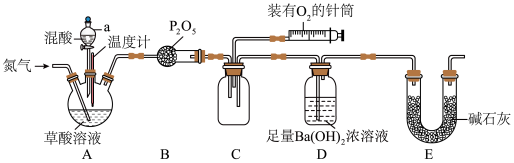
(1)仪器a的名称为______ ,A装置中三颈烧瓶的最佳加热方式为______ 。
(2)指出该套装置的错误之处:______ 。
(3)实验开始一段时间后,仍需通入氮气,此时通入氮气的作用为____________ 。
(4)实验开始后,要证明有NO产生的实验操作和现象为____________ 。
(5)下列各项措施中,能提高碳含量的测定准确度的是______ (填标号)。
a.滴加混酸不宜过快 b在加入混酸之前,排尽装置中的 气体
气体
c.球形干燥管中的药品换成 d.D中的溶液换成澄清饱和石灰水
d.D中的溶液换成澄清饱和石灰水
(6)在实验操作规范的条件下,实验测得草酸中碳的含量比实际的大,其原因可能是____________ 。
已知:
Ⅰ.硝酸氧化草酸溶液:
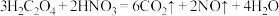 。
。Ⅱ.控制反应液温度为55~60℃,边搅拌边滴加含有适量催化剂的混酸(
 与
与 )溶液。
)溶液。
(1)仪器a的名称为
(2)指出该套装置的错误之处:
(3)实验开始一段时间后,仍需通入氮气,此时通入氮气的作用为
(4)实验开始后,要证明有NO产生的实验操作和现象为
(5)下列各项措施中,能提高碳含量的测定准确度的是
a.滴加混酸不宜过快 b在加入混酸之前,排尽装置中的
 气体
气体c.球形干燥管中的药品换成
 d.D中的溶液换成澄清饱和石灰水
d.D中的溶液换成澄清饱和石灰水(6)在实验操作规范的条件下,实验测得草酸中碳的含量比实际的大,其原因可能是
您最近一年使用:0次
2024-02-25更新
|
238次组卷
|
2卷引用:云南省楚雄彝族自治州2023-2024学年高三上学期1月期末考试理综化学试题



