人体必需的部分元素在周期表中的分布情况如下:
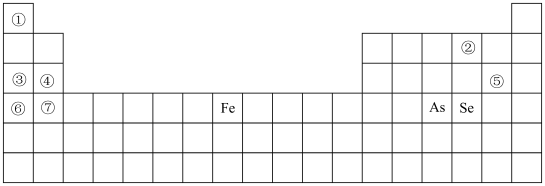
请根据以上信息回答下列问题:
(1)元素③能维持人体水分平衡、酸碱平衡等,元素③在周期表中的位置为___________ 。
(2)人体缺元素⑦会导致腿软、抽筋、乏力、烦躁、精力不集中等症状,牛奶中含有大量的元素⑦,有利于骨骼健康。根据元素⑦在周期表中的位置预测牛奶中的元素⑦以___________ 形式存在。(填“离子”或“单质”)
(3)硒(Se)元素对人体的抗衰老具有很好的作用,同时能增强人体免疫力、抵抗力,具有抗癌、抗肿瘤等功效,元素Se的两种核素 、
、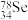 互称为
互称为___________ 。
(4)人体中的①元素通过选择性清除恶性自由基,保护细胞分裂分化,达到抗细胞变异和抗癌变的效果,请写出元素①与元素②组成的含10个电子的分子的电子式:___________ 。
(5)人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血,某种市售营养麦片中含有微量的铁粉,请写出铁粉在胃酸(主要成分HCl)中发生反应的离子方程式___________ 。
(6)适量的砷(As)有助于血红蛋白的合成,能够促进人体的生长发育,如果使用不当,砷对人体的危害就会非常的大,根据砷在周期表中位置预测非金属性As___________ Se(填“>”“<”或“=”)。
(7)人体应减少铝元素的摄入,铝元素可导致脑组织退行性病变,诱发老年痴呆等脑病,请写出铝与NaOH溶液反应的化学方程式___________ 。
(8)以上周期表信息中元素的最高价氧化物对应水化物酸性最强的是___________ (填化学式)
(9)下列不能证明元素⑥的金属性比④强的事实有___________ 。
a.元素⑥的原子最外层电子数比元素④的原子最外层电子数少。
b.⑥的单质能与冷水剧烈反应而④的单质不能
c.⑥的最高价氧化物对应水化物的碱性比④强

请根据以上信息回答下列问题:
(1)元素③能维持人体水分平衡、酸碱平衡等,元素③在周期表中的位置为
(2)人体缺元素⑦会导致腿软、抽筋、乏力、烦躁、精力不集中等症状,牛奶中含有大量的元素⑦,有利于骨骼健康。根据元素⑦在周期表中的位置预测牛奶中的元素⑦以
(3)硒(Se)元素对人体的抗衰老具有很好的作用,同时能增强人体免疫力、抵抗力,具有抗癌、抗肿瘤等功效,元素Se的两种核素
 、
、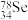 互称为
互称为(4)人体中的①元素通过选择性清除恶性自由基,保护细胞分裂分化,达到抗细胞变异和抗癌变的效果,请写出元素①与元素②组成的含10个电子的分子的电子式:
(5)人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血,某种市售营养麦片中含有微量的铁粉,请写出铁粉在胃酸(主要成分HCl)中发生反应的离子方程式
(6)适量的砷(As)有助于血红蛋白的合成,能够促进人体的生长发育,如果使用不当,砷对人体的危害就会非常的大,根据砷在周期表中位置预测非金属性As
(7)人体应减少铝元素的摄入,铝元素可导致脑组织退行性病变,诱发老年痴呆等脑病,请写出铝与NaOH溶液反应的化学方程式
(8)以上周期表信息中元素的最高价氧化物对应水化物酸性最强的是
(9)下列不能证明元素⑥的金属性比④强的事实有
a.元素⑥的原子最外层电子数比元素④的原子最外层电子数少。
b.⑥的单质能与冷水剧烈反应而④的单质不能
c.⑥的最高价氧化物对应水化物的碱性比④强
更新时间:2024-01-18 12:39:51
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
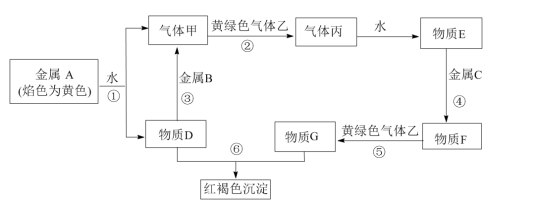
请根据以上信息回答下列问题:
(1)写出下列物质的化学式B________ 、乙________
(2)写出下列反应离子方程式:
反应①___________________________________________________________________
反应③___________________________________________________________________
反应⑤___________________________________________________________________

请根据以上信息回答下列问题:
(1)写出下列物质的化学式B
(2)写出下列反应离子方程式:
反应①
反应③
反应⑤
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】铁、铝的混合物进行如下实验:
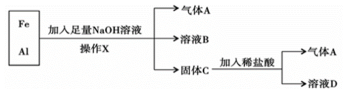
(1)操作X的名称是____ ;
(2)气体A是_____ (填化学式);
(3)A与Cl2混合光照可能发生爆炸,生成___ (填化学式),A在该反应中作为____ (填“氧化剂”或“还原剂”);
(4)溶液B中阴离子除OH-外还有____ (填离子符号),溶液D中存在的金属离子为___ (填离子符号);
(5)加入足量NaOH溶液时发生反应的离子方程式为:____ ;

(1)操作X的名称是
(2)气体A是
(3)A与Cl2混合光照可能发生爆炸,生成
(4)溶液B中阴离子除OH-外还有
(5)加入足量NaOH溶液时发生反应的离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
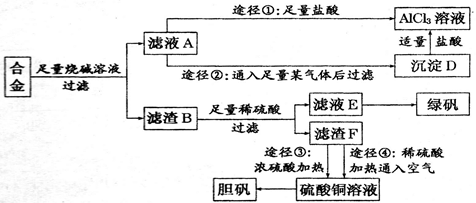
【推荐3】某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体[FeSO4·7H2O]和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
(1)写出合金与烧碱溶液反应的离子方程式____________________________ 。
(2)进行途径②时,所通入的气体化学式为____________________________ 。
(3)用滤渣F通过途径③或者途径④制取胆矾,相比之下,途径_______ (填序号)更好。通过途径④制取胆矾,必须进行的实验操作步骤:加硫酸、加热通空气、过滤、_______ 、_______ 、过滤、自然干燥。途径④的离子方程式为_____________ 。
(4)白磷有剧毒,不慎沾到皮肤上,可取少量胆矾配制成CuSO4溶液冲洗解毒。白磷可与热的CuSO4溶液反应生成Cu3P(Cu为+1价),与冷CuSO4溶液则析出Cu,反应方程式分别如下(均未配平)。若两反应中被氧化的P4的物质的量相等,则两反应分别消耗的CuSO4的物质的量之比为____________ 。
①P4+CuSO4+H2O Cu3P+H3PO4+H2SO4(未配平)
Cu3P+H3PO4+H2SO4(未配平)
②P4+CuSO4+H2O→Cu+H3PO4+H2SO4(未配平)
(1)写出合金与烧碱溶液反应的离子方程式
(2)进行途径②时,所通入的气体化学式为
(3)用滤渣F通过途径③或者途径④制取胆矾,相比之下,途径
(4)白磷有剧毒,不慎沾到皮肤上,可取少量胆矾配制成CuSO4溶液冲洗解毒。白磷可与热的CuSO4溶液反应生成Cu3P(Cu为+1价),与冷CuSO4溶液则析出Cu,反应方程式分别如下(均未配平)。若两反应中被氧化的P4的物质的量相等,则两反应分别消耗的CuSO4的物质的量之比为
①P4+CuSO4+H2O
 Cu3P+H3PO4+H2SO4(未配平)
Cu3P+H3PO4+H2SO4(未配平)②P4+CuSO4+H2O→Cu+H3PO4+H2SO4(未配平)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】根据表中几种短周期元素的原子半径及主要化合价,回答下列问题:
(1)元素C组成的常见单质有两种,分别是_______ 、_______ (写名称)
(2)用电子式表示ID2的形成过程:_______ 。
(3)A、H、J的离子半径由大到小顺序是_______ (用离子符号表示)。
(4)78 gJ2B2与足量的水反应生成_______ L(标准状况下)气体。
(5)元素D的单质与水反应的离子方程式为_______ 。
| 元素代号 | A | B | C | D |
| 化合价 |  |  |  、 、 |  |
原子半径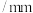 | 0.071 | 0.074 | 0.077 | 0.099 |
| 元素代号 | G | H | I | J |
| 化合价 |  、 、 |  |  |  |
原子半径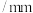 | 0.110 | 0.143 | 0.160 | 0.186 |
(2)用电子式表示ID2的形成过程:
(3)A、H、J的离子半径由大到小顺序是
(4)78 gJ2B2与足量的水反应生成
(5)元素D的单质与水反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题。
(1)元素③在周期表中所处位置_______ 。
(2)元素⑧的原子结构示意图是_______ 。
(3)③元素形成的简单阴离子的电子式为_______ 。
(4)上述元素中的三种元素可组成的离子化合物有_______ (写二即可)。
(5)⑥与⑨组成化合物甲,用电子式表示甲的形成过程:_______ 。
| IA | 0族 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)元素③在周期表中所处位置
(2)元素⑧的原子结构示意图是
(3)③元素形成的简单阴离子的电子式为
(4)上述元素中的三种元素可组成的离子化合物有
(5)⑥与⑨组成化合物甲,用电子式表示甲的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,并回答下列问题:
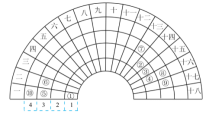
(1)⑩在常见元素周期表中的位置是___________ 。
(2)⑦原子的L层有___________ 个电子。
(3)由①、③、⑨形成的离子化合物的电子式为___________ 。用电子式表示一个④、两个⑤形成化合物的过程:___________ 。
(4)④、⑧形成的简单氢化物稳定性:④___________ (填“>”或“<”)⑧。
(5)③、⑧、⑨的最高价氧化物对应水化物的酸性最强的是___________ (填化学式)。
(6)④、⑤、⑥对应简单离子的半径由大到小的顺序为___________ (用离子符号表示)

(1)⑩在常见元素周期表中的位置是
(2)⑦原子的L层有
(3)由①、③、⑨形成的离子化合物的电子式为
(4)④、⑧形成的简单氢化物稳定性:④
(5)③、⑧、⑨的最高价氧化物对应水化物的酸性最强的是
(6)④、⑤、⑥对应简单离子的半径由大到小的顺序为
您最近一年使用:0次



