解题方法
1 . 某学习小组探究FeCl3与Na2SO3之间的反应,设计了以下实验。下列说法错误的是
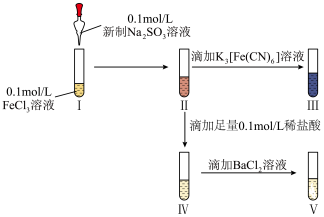
| A.Ⅱ中溶液颜色比Ⅰ中更深,是由于Fe3+水解程度增大 |
| B.Ⅲ中有深蓝色沉淀生成,无法证明FeCl3与Na2SO3发生了氧化还原反应 |
| C.从Ⅱ到Ⅳ滴加的溶液可改为0.05mol/L稀硫酸 |
| D.Ⅴ中有大量白色沉淀生成,证明FeCl3能氧化Na2SO3 |
您最近一年使用:0次
2024-05-07更新
|
166次组卷
|
2卷引用:江西省鹰潭市2024届高三下学期第二次模拟考试化学试卷
名校
解题方法
2 . 下列关于硫、氮及其化合物说法错误的是
| A.硝酸的浓溶液保存在棕色试剂瓶中,并放置在阴凉处 |
B.葡萄酒中添加适量 可以起到抗氧化的作用 可以起到抗氧化的作用 |
C.向盛有固体 的试管中加入浓硫酸并加热,管口出现白雾,证明酸性: 的试管中加入浓硫酸并加热,管口出现白雾,证明酸性: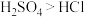 |
D.将少量浓氨水滴入装有碱石灰的烧瓶中,可快速获得 |
您最近一年使用:0次
名校
解题方法
3 . 下列有关钠的化合物的说法正确的是
| A.用加热法除去NaHCO3固体中混有的Na2CO3 |
| B.Na2O2与H2O的反应中有氢氧化钠生成,Na2O2是典型的碱性氧化物 |
| C.向酚酞溶液中加入过量的过氧化钠粉末,可以观察到溶液的颜色变化:先变红,后褪色 |
| D.某溶液样品的焰色试验火焰呈黄色,证明原溶液中有钠元素,一定没有钾元素 |
您最近一年使用:0次
2023-11-07更新
|
249次组卷
|
2卷引用:江西省抚州市乐安县第二中学2023-2024学年高一上学期11月期中化学试题
名校
4 . 某实验小组利用下图装置探究H2C2O4溶液与酸性KMnO4溶液的反应(夹持装置略去)。

查阅资料:①H2C2O4为二元弱酸。
②溶液浓度越大,越不利于气体的扩散。
(1)H2C2O4溶液与酸性KMnO4溶液反应的离子方程式为___________ 。
(2)仪器A的名称为___________ 。
(3)检查装置气密性的方法为___________ 。
(4)若以单位时间内生成的气体体积作为反应速率的观测指标,则量筒中的试剂为___________。
(5)探究H2C2O4溶液与酸性KMnO4溶液的浓度对反应速率的影响,实验数据如下表所示:
①c1=___________ 。
②某同学从实验1和2的褪色时间分析出实验2的反应速率小于实验1,请分析该结论是否正确,并说明原因:___________ 。
③结合实验数据,下列说法错误的是___________ 。(填标号)
A.其他条件不变时,c(H2C2O4)浓度越高,反应速率越快
B.其他条件不变时,当c(H2C2O4)为0.8mol·L-1,褪色时间一定介于163s至360s之间
C.实验5中v(H2C2O4)=0.15mol·L-1·min-1
D.其他条件不变时,当c(H2C2O4)>0.9mol·L-1,溶液浓度增大,不利于CO2扩散,可能导致褪色时间延长
(6)H2C2O4溶液与酸性KMnO4溶液生成的Mn2+对该反应有催化作用。请以实验1为对照组,设计实验方案证明Mn2+的催化作用___________ 。

查阅资料:①H2C2O4为二元弱酸。
②溶液浓度越大,越不利于气体的扩散。
(1)H2C2O4溶液与酸性KMnO4溶液反应的离子方程式为
(2)仪器A的名称为
(3)检查装置气密性的方法为
(4)若以单位时间内生成的气体体积作为反应速率的观测指标,则量筒中的试剂为___________。
| A.饱和NaHCO3溶液 | B.饱和NaCl溶液 | C.水 | D.饱和Na2CO3溶液 |
| 实验 序号 | KMnO4溶液 | H2C2O4溶液 | H2SO4溶液 | 褪色时间 | ||
| c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | t/s | |
| 1 | 0.005 | 4.0 | 0.2 | 2.0 | 0.120 | 307 |
| 2 | 0.020 | 4.0 | 0.2 | 2.0 | 0.120 | 545 |
| 3 | 0.010 | 4.0 | 0.5 | 2.0 | 0.120 | 201 |
| 4 | 0.010 | 4.0 | 0.7 | 2.0 | 0.120 | 163 |
| 5 | 0.010 | 4.0 | 0.9 | 2.0 | 0.120 | 360 |
| 6 | 0.010 | 4.0 | 1.0 | 2.0 | c1 | 512 |
②某同学从实验1和2的褪色时间分析出实验2的反应速率小于实验1,请分析该结论是否正确,并说明原因:
③结合实验数据,下列说法错误的是
A.其他条件不变时,c(H2C2O4)浓度越高,反应速率越快
B.其他条件不变时,当c(H2C2O4)为0.8mol·L-1,褪色时间一定介于163s至360s之间
C.实验5中v(H2C2O4)=0.15mol·L-1·min-1
D.其他条件不变时,当c(H2C2O4)>0.9mol·L-1,溶液浓度增大,不利于CO2扩散,可能导致褪色时间延长
(6)H2C2O4溶液与酸性KMnO4溶液生成的Mn2+对该反应有催化作用。请以实验1为对照组,设计实验方案证明Mn2+的催化作用
您最近一年使用:0次
2023-07-12更新
|
424次组卷
|
2卷引用:江西省萍乡市安源中学2022-2023学年高一下学期期末考试化学试题
名校
5 . 实验小组欲除去粗盐中的Ca2+、Mg2+和 ,下列有关该实验的说法错误的是
,下列有关该实验的说法错误的是
 ,下列有关该实验的说法错误的是
,下列有关该实验的说法错误的是| A.选用试剂的顺序可依次为:BaCl2、Na2CO3、NaOH、HCl |
B.可用 代替BaCl2和NaOH,简化实验操作步骤 代替BaCl2和NaOH,简化实验操作步骤 |
C.滴加Na2CO3溶液发生的反应只有: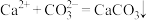 |
| D.为检验滴加盐酸是否过量,可用玻璃棒蘸取溶液滴在pH试纸中部,若变蓝,证明盐酸量不足 |
您最近一年使用:0次
2023-04-08更新
|
292次组卷
|
3卷引用:江西省抚州市金溪县第一中学2023-2024学年高一下学期第一次月考化学试卷
名校
6 . 短周期主族元素A、B、C、D的原子序数依次增大,A元素与C元素同主族,B的单质可以在A的单质中燃烧,生成一种具有强氧化性的物质,C元素与D元素相邻,D元素最高价氧化物对应的水化物和氢化物溶于水都能完全电离。下列说法错误的是
| A.元素A与元素B形成的两种化合物中,阴、阳离子个数比都是1:2 |
| B.利用D的单质和C的氢化物反应,可证明非金属性:D>C |
| C.可用酒精除去试管内壁附着的C单质 |
| D.简单离子半径:C>D>A>B |
您最近一年使用:0次
2023-05-30更新
|
385次组卷
|
3卷引用:江西省宜春市宜丰中学2023-2024学年高一下学期4月期中考试化学试题
江西省宜春市宜丰中学2023-2024学年高一下学期4月期中考试化学试题湘豫名校联考2023届高三下学期第三次模拟考试(5月)理科综合化学试题(已下线)考点巩固卷05 物质结构 元素周期律(2大考点50题)-2024年高考化学一轮复习考点通关卷(新高考通用)
名校
7 . 某同学通过实验“证明鸡蛋壳的主要成分是碳酸钙”,装置示意图如图。
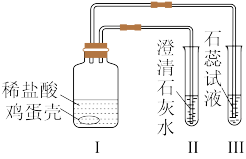
(1)按要求填写碳酸钙的类别属性(如按正离子分类,碳酸钙属于钙盐):按负离子分类,属于_____ ;按聚集状态分类,属于_____ ;按溶解性分类,属于_____ ;按电离程度分类,属于_____ 。
(2)根据碳酸钙的物质类别推知,下列说法或现象不合理的是_____ 。
(3)写出I中发生主要反应的离子方程式_____ ;此反应是否属于氧化还原反应_____ (填“是”或“否”);理由是_____ 。
(4)下列能在澄清石灰水中大量共存的离子组是_____ 。
(5)试用简要的文字说明III中现象产生的原因_____ 。

(1)按要求填写碳酸钙的类别属性(如按正离子分类,碳酸钙属于钙盐):按负离子分类,属于
(2)根据碳酸钙的物质类别推知,下列说法或现象不合理的是
| A.I中的鸡蛋壳发生了分解反应 | B.I中的鸡蛋壳表面产生气泡 |
| C.II中的澄清石灰水变浑浊 | D.III中紫色石蕊试液变浅红 |
(4)下列能在澄清石灰水中大量共存的离子组是
| A.Cu2+、C1- | B.K+、NO | C.H+、SO | D.Na+、CO |
您最近一年使用:0次
2023-01-10更新
|
272次组卷
|
2卷引用:江西省抚州市乐安县第二中学2023-2024学年高一上学期11月期中化学试题
解题方法
8 . T℃时,在体积为2L的密闭容器内,与同一个化学反应有关的A、B、C、D四种物质(D为固体,其余均为气体)的物质的量随反应时间变化的曲线如图所示,回答下列问题。
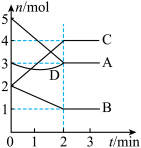
(1)该反应的化学方程式为_______ 。
(2)物质D在反应中的作用是______ 。
(3)若在上述反应中A是SO2、B是O2、C是SO3。下列说法能表示反应达到平衡状态的是______ (填字母);在0~2min内用O2表示的反应速率v(O2)=______ 。
A.容器内的气体压强保持不变 B.物质的量浓度:c(SO2)=2c(O2)
C.混合气的平均相对分子质量保持不变 D.化学反应速率:v(SO2)=v(SO3)
(4)某兴趣小组同学拟在实验室中制取SO2,并探究SO2使品红溶液褪色的原因。
①用Cu和浓硫酸反应制取SO2,化学反应方程式是_______ 。
②兴趣小组同学利用如图装置探究SO2的漂白性,观察到I中品红溶液不褪色,II中品红溶液褪色。
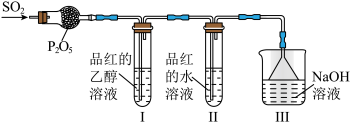
查阅资料:SO2通入水中存在如下反应:SO2+xH2O SO2•xH2O
SO2•xH2O H++HSO
H++HSO +(x-1)H2O;HSO
+(x-1)H2O;HSO
 SO
SO +H+。
+H+。
通过分析上述现象,猜测使品红水溶液褪色的微粒可能是i.H2SO3;ii.______ ;iii.______ 。
③为了证明上述猜测ii和iii,进行表中实验1和2,记录现象。
该实验说明,两种粒子中,______ 使品红水溶液褪色程度更大。
④取实验1所得溶液直接加热接近沸腾,溶液不恢复红色,在热溶液中滴加稀硫酸则恢复红色;说明______ ;取实验2所得溶液直接加热,则慢慢恢复浅红色,说明NaHSO3与品红生成的物质不稳定。

(1)该反应的化学方程式为
(2)物质D在反应中的作用是
(3)若在上述反应中A是SO2、B是O2、C是SO3。下列说法能表示反应达到平衡状态的是
A.容器内的气体压强保持不变 B.物质的量浓度:c(SO2)=2c(O2)
C.混合气的平均相对分子质量保持不变 D.化学反应速率:v(SO2)=v(SO3)
(4)某兴趣小组同学拟在实验室中制取SO2,并探究SO2使品红溶液褪色的原因。
①用Cu和浓硫酸反应制取SO2,化学反应方程式是
②兴趣小组同学利用如图装置探究SO2的漂白性,观察到I中品红溶液不褪色,II中品红溶液褪色。

查阅资料:SO2通入水中存在如下反应:SO2+xH2O
 SO2•xH2O
SO2•xH2O H++HSO
H++HSO +(x-1)H2O;HSO
+(x-1)H2O;HSO
 SO
SO +H+。
+H+。通过分析上述现象,猜测使品红水溶液褪色的微粒可能是i.H2SO3;ii.
③为了证明上述猜测ii和iii,进行表中实验1和2,记录现象。
| 实验序号 | 实验1 | 实验2 |
| 实验操作 |  2mL0.20mol•L-1Na2SO3溶液 |  2mL0.20mol•L-1NaHSO3溶液 |
| 实验现象 | 迅速褪色 | 褪色较慢 |
④取实验1所得溶液直接加热接近沸腾,溶液不恢复红色,在热溶液中滴加稀硫酸则恢复红色;说明
您最近一年使用:0次
2023-04-28更新
|
407次组卷
|
3卷引用:江西省南昌市等5地2022-2023学年高一下学期4月期中考试化学试题
解题方法
9 . 1810年,英国化学家戴维以大量事实为依据,确认一种黄绿色气体是一种新元素组成的单质——氯气。某化学兴趣小组同学利用以下装置制备干燥的氯气并对氯气的性质进行探究。

(1)仪器b的名称为_______ 。某同学认为该实验装置存在一处明显的不足,其改进措施为_______ 。
(2)仪器a中发生反应的化学方程式为_______ 。根据氯气的性质D中的收集装置可以选择_______ (填序号)。
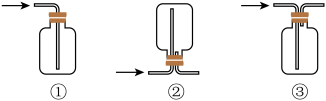
(3)下列有关该实验的说法中不正确的是_______ (填字母)。
A.将b中液体换为稀盐酸,同样可以产生氯气
B.C中试剂是浓硫酸,目的是干燥氯气
C.E中红色布条不褪色,F中红色布条褪色证明氯气具有漂白性
(4)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如下图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:_______ 。

(5)实验室还可用等物质的量的 与
与 的水溶液反应制取
的水溶液反应制取 ,同时生成
,同时生成 和
和 ,反应的化学方程式为
,反应的化学方程式为_______ 。
(6)已知氯气和 溶液在一定温度下能同时发生反应:
溶液在一定温度下能同时发生反应: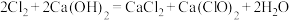 ,
,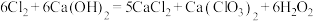 。某温度下,将氯气通入
。某温度下,将氯气通入 溶液中,反应得到
溶液中,反应得到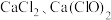 和
和 的混合溶液,该反应中,氧化产物为
的混合溶液,该反应中,氧化产物为_______ (填化学式),经测定 与
与 的个数比为2∶3,则氯气与氢氧化钙反应时,被还原的氯原子和被氧化的氯原子的个数比为
的个数比为2∶3,则氯气与氢氧化钙反应时,被还原的氯原子和被氧化的氯原子的个数比为_______ 。

(1)仪器b的名称为
(2)仪器a中发生反应的化学方程式为

(3)下列有关该实验的说法中不正确的是
A.将b中液体换为稀盐酸,同样可以产生氯气
B.C中试剂是浓硫酸,目的是干燥氯气
C.E中红色布条不褪色,F中红色布条褪色证明氯气具有漂白性
(4)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如下图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:

(5)实验室还可用等物质的量的
 与
与 的水溶液反应制取
的水溶液反应制取 ,同时生成
,同时生成 和
和 ,反应的化学方程式为
,反应的化学方程式为(6)已知氯气和
 溶液在一定温度下能同时发生反应:
溶液在一定温度下能同时发生反应: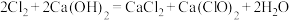 ,
,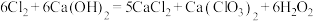 。某温度下,将氯气通入
。某温度下,将氯气通入 溶液中,反应得到
溶液中,反应得到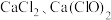 和
和 的混合溶液,该反应中,氧化产物为
的混合溶液,该反应中,氧化产物为 与
与 的个数比为2∶3,则氯气与氢氧化钙反应时,被还原的氯原子和被氧化的氯原子的个数比为
的个数比为2∶3,则氯气与氢氧化钙反应时,被还原的氯原子和被氧化的氯原子的个数比为
您最近一年使用:0次
2022-11-19更新
|
617次组卷
|
3卷引用:江西省上饶市万年县第一中学2023-2024学年高一上学期第二次月考化学试题
10 . 麦芽糖主要存在于发芽的谷粒中,其α-D-(+)-麦芽糖的结构如图所示,下列相关说法中正确的是


| A.麦芽糖是一种常见的寡糖 |
| B.如图麦芽糖分子结构中无醛基,因此属于非还原糖 |
| C.麦芽糖由一分子葡萄糖和一分子果糖脱水缩合形成 |
| D.将麦芽糖水解液调至碱性后,可发生银镜反应,证明部分麦芽糖发生了水解 |
您最近一年使用:0次
2022-03-04更新
|
436次组卷
|
4卷引用:江西省抚州市七校2021-2022学年高二下学期期末考试化学试题
江西省抚州市七校2021-2022学年高二下学期期末考试化学试题辽宁省名校联盟2021-2022学年下学期高三3月联合考试化学试题(已下线)第23讲 糖类(下)(word讲义)-【帮课堂】2021-2022学年高二化学同步精品讲义(人教2019选择性必修3)(已下线)生物大分子——课时1糖类



