名校
1 . 科学家通过X射线证明,MgO、CaO、NiO、FeO的晶体结构与NaCl的晶体结构相似。某同学画出的MgO晶胞结构示意图如图所示,下列说法错误的是


| A.图中的错误的是⑧ |
| B.MgO是优良的耐高温材料,MgO的熔点比CaO的高 |
| C.NiO晶胞中Ni和O周围等距离且最近的O和Ni分别为6、6 |
| D.晶体中与每个O2-距离最近且等距离的O2-有6个 |
您最近一年使用:0次
名校
2 . 下列说法错误的是
| A.用洁净的铂丝蘸取溶液进行焰色试验,火焰呈黄色,证明溶液中有Na+,可能有K+ |
| B.电解质溶于水或受热熔化时,形成自由移动的离子的过程叫做电离 |
| C.容量瓶需要用蒸馏水洗涤、干燥后才可使用 |
| D.不能用澄清的石灰水鉴别Na2CO3和NaHCO3两种溶液 |
您最近一年使用:0次
2021-12-18更新
|
199次组卷
|
2卷引用:贵州省黔南州都匀市都匀第一中学2021-2022学年高一上学期期中化学试题
3 . 硫酸亚铁铵 又称莫尔盐,是一种重要的化工原料,用途十分广泛。可用黄铁矿(主要含
又称莫尔盐,是一种重要的化工原料,用途十分广泛。可用黄铁矿(主要含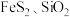 等)制备莫尔盐,该过程中产生的废气同时也可用于工业制硫酸,流程如下:
等)制备莫尔盐,该过程中产生的废气同时也可用于工业制硫酸,流程如下: 中S元素的化合价为
中S元素的化合价为_______ ;
(2)在焙烧前通常将黄铁矿粉碎,其目的是_______ ;焙烧的主要反应化学方程式是_______ ;
(3)滤渣1的主要成分是_______ ;
(4)为证实所得莫尔盐样品中不含 ,实验方案为:取其少量样品溶于试管中,加入
,实验方案为:取其少量样品溶于试管中,加入_______ (填化学式),现象是_______ ,证明不含 ;
;
(5)吸收 气体时用98.3%的浓硫酸而不用水,原因是
气体时用98.3%的浓硫酸而不用水,原因是_______ ;
(6)硫酸工厂的尾气中仍含有一定量 ,可用氨碱法进行处理。用过量氨水吸收
,可用氨碱法进行处理。用过量氨水吸收 的离子方程式为
的离子方程式为_______ 。
 又称莫尔盐,是一种重要的化工原料,用途十分广泛。可用黄铁矿(主要含
又称莫尔盐,是一种重要的化工原料,用途十分广泛。可用黄铁矿(主要含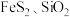 等)制备莫尔盐,该过程中产生的废气同时也可用于工业制硫酸,流程如下:
等)制备莫尔盐,该过程中产生的废气同时也可用于工业制硫酸,流程如下:
 中S元素的化合价为
中S元素的化合价为(2)在焙烧前通常将黄铁矿粉碎,其目的是
(3)滤渣1的主要成分是
(4)为证实所得莫尔盐样品中不含
 ,实验方案为:取其少量样品溶于试管中,加入
,实验方案为:取其少量样品溶于试管中,加入 ;
;(5)吸收
 气体时用98.3%的浓硫酸而不用水,原因是
气体时用98.3%的浓硫酸而不用水,原因是(6)硫酸工厂的尾气中仍含有一定量
 ,可用氨碱法进行处理。用过量氨水吸收
,可用氨碱法进行处理。用过量氨水吸收 的离子方程式为
的离子方程式为
您最近一年使用:0次
4 . 二氧化碳催化加氢制甲醇是一种重要的碳中和方式。回答下列问题:
(1)二氧化碳加氢制甲醇的热化学方程式为
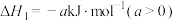 。
。
①此反应在___________ (填“高温”“常温”或“低温”)条件下容易自发进行。
②有利于提高 平衡转化率的是
平衡转化率的是___________ (填序号)。
A.降低温度 B.继续通入 C.及时将
C.及时将 分离 D.使用合适催化剂
分离 D.使用合适催化剂
③根据下表中的键能数据计算 的键能
的键能___________ 。
(2)398K时,在某刚性容器中,投入2mol 和6mol
和6mol  发生上述反应,初始压强为8MPa,反应经过5min达到平衡时
发生上述反应,初始压强为8MPa,反应经过5min达到平衡时 的物质的量等于其余三种物质的物质的量之和,用
的物质的量等于其余三种物质的物质的量之和,用 表示此反应的速率为
表示此反应的速率为___________  ,计算该温度下的
,计算该温度下的
___________  。
。
(3)①研究表明,在酸性电解质中, 气体可被电化学还原为
气体可被电化学还原为 和CO等产品。请写出
和CO等产品。请写出 被电化学还原为
被电化学还原为 的电极反应式:
的电极反应式:___________ 。
②实验证明,此电解过程中阴极产物只有 和CO,且电化学还原44g
和CO,且电化学还原44g  时转移电子的物质的量为5mol,则产物中
时转移电子的物质的量为5mol,则产物中 和CO的物质的量之比为
和CO的物质的量之比为___________ 。
(1)二氧化碳加氢制甲醇的热化学方程式为

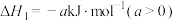 。
。①此反应在
②有利于提高
 平衡转化率的是
平衡转化率的是A.降低温度 B.继续通入
 C.及时将
C.及时将 分离 D.使用合适催化剂
分离 D.使用合适催化剂③根据下表中的键能数据计算
 的键能
的键能| 化学键 |  |  |  |  |
键能 | b | c | d | e |
(2)398K时,在某刚性容器中,投入2mol
 和6mol
和6mol  发生上述反应,初始压强为8MPa,反应经过5min达到平衡时
发生上述反应,初始压强为8MPa,反应经过5min达到平衡时 的物质的量等于其余三种物质的物质的量之和,用
的物质的量等于其余三种物质的物质的量之和,用 表示此反应的速率为
表示此反应的速率为 ,计算该温度下的
,计算该温度下的
 。
。(3)①研究表明,在酸性电解质中,
 气体可被电化学还原为
气体可被电化学还原为 和CO等产品。请写出
和CO等产品。请写出 被电化学还原为
被电化学还原为 的电极反应式:
的电极反应式:②实验证明,此电解过程中阴极产物只有
 和CO,且电化学还原44g
和CO,且电化学还原44g  时转移电子的物质的量为5mol,则产物中
时转移电子的物质的量为5mol,则产物中 和CO的物质的量之比为
和CO的物质的量之比为
您最近一年使用:0次
名校
5 . 现有未知固体粉末,含有K+、Fe3+、Ba2+、 、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:
、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:
(1)取少量固体粉末溶于水中,固体完全溶解且溶液无色透明,证明该固体粉末中无___________ (填离子符号);
(2)有同学提出质疑,直接观察溶液颜色并不能作为判断的标准,可能含量太少观察不出来,取(1)中少量溶液于试管中加入___________ 溶液,发现溶液变为红色。
(3)另取(1)中少量溶液于试管中,滴加少量的稀硫酸,发现有白色沉淀产生,证明该固体粉末中有___________ (填离子符号),并写出离子方程式___________ 。
(4)另取(1)中少量溶液进行焰色试验,透过蓝色钴玻璃观察,火焰呈紫色,证明该固体粉末中有___________ (填离子符号);
(5)取(1)中少量溶液,加入硝酸银溶液,发现无明显现象,证明该固体粉末中无___________ (填离子符号),该固体粉末中一定有 ,原因是
,原因是___________ 。
 、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:
、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:(1)取少量固体粉末溶于水中,固体完全溶解且溶液无色透明,证明该固体粉末中无
(2)有同学提出质疑,直接观察溶液颜色并不能作为判断的标准,可能含量太少观察不出来,取(1)中少量溶液于试管中加入
(3)另取(1)中少量溶液于试管中,滴加少量的稀硫酸,发现有白色沉淀产生,证明该固体粉末中有
(4)另取(1)中少量溶液进行焰色试验,透过蓝色钴玻璃观察,火焰呈紫色,证明该固体粉末中有
(5)取(1)中少量溶液,加入硝酸银溶液,发现无明显现象,证明该固体粉末中无
 ,原因是
,原因是
您最近一年使用:0次
名校
解题方法
6 . 焦亚硫酸钠 是工业上常用的抗氧化剂。一种湿法制备
是工业上常用的抗氧化剂。一种湿法制备 的生产工艺如下:
的生产工艺如下:

回答下列问题:
(1) 中硫元素的化合价为
中硫元素的化合价为___________ 。
(2)反应1中通入NH3和CO2的顺序为___________ 。
(3)关于上述流程,下列说法正确的是___________(填字母)。
(4)工业上添加 作抗氧化剂时会放出一种有刺激性气味的气体。实验室检验该气体的常用试剂是
作抗氧化剂时会放出一种有刺激性气味的气体。实验室检验该气体的常用试剂是___________ 。
(5)溶液A中阳离子有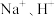 和X离子。检验X离子的操作和现象是
和X离子。检验X离子的操作和现象是___________ 。
(6)获得 需要经过多步反应,其中包括反应3制备
需要经过多步反应,其中包括反应3制备 溶液,然后加入
溶液,然后加入 溶液调
溶液调 转化为
转化为 溶液,再通入
溶液,再通入 生成
生成 ,当溶液中
,当溶液中 含量达到过饱和浓度时,析出
含量达到过饱和浓度时,析出 晶体,反应方程式为
晶体,反应方程式为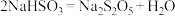 。
。
①反应3的化学方程式为___________ 。
②加入 转化为
转化为 的离子方程式为
的离子方程式为___________ 。
(7)工业上可用焦亚硫酸钠 处理含有
处理含有 的酸性废水,使其转化为毒性较低的
的酸性废水,使其转化为毒性较低的 ,理论上处理
,理论上处理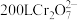 浓度为
浓度为 的废水需要焦亚硫酸钠
的废水需要焦亚硫酸钠___________ g。
 是工业上常用的抗氧化剂。一种湿法制备
是工业上常用的抗氧化剂。一种湿法制备 的生产工艺如下:
的生产工艺如下:
回答下列问题:
(1)
 中硫元素的化合价为
中硫元素的化合价为(2)反应1中通入NH3和CO2的顺序为
(3)关于上述流程,下列说法正确的是___________(填字母)。
| A.该流程中,CO2可以循环使用 |
| B.反应2为分解反应 |
| C.反应3证明硫的非金属性比碳的强 |
D.氨气溶于水使溶液呈碱性的原因是存在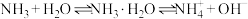 反应 反应 |
(4)工业上添加
 作抗氧化剂时会放出一种有刺激性气味的气体。实验室检验该气体的常用试剂是
作抗氧化剂时会放出一种有刺激性气味的气体。实验室检验该气体的常用试剂是(5)溶液A中阳离子有
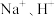 和X离子。检验X离子的操作和现象是
和X离子。检验X离子的操作和现象是(6)获得
 需要经过多步反应,其中包括反应3制备
需要经过多步反应,其中包括反应3制备 溶液,然后加入
溶液,然后加入 溶液调
溶液调 转化为
转化为 溶液,再通入
溶液,再通入 生成
生成 ,当溶液中
,当溶液中 含量达到过饱和浓度时,析出
含量达到过饱和浓度时,析出 晶体,反应方程式为
晶体,反应方程式为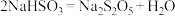 。
。①反应3的化学方程式为
②加入
 转化为
转化为 的离子方程式为
的离子方程式为(7)工业上可用焦亚硫酸钠
 处理含有
处理含有 的酸性废水,使其转化为毒性较低的
的酸性废水,使其转化为毒性较低的 ,理论上处理
,理论上处理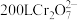 浓度为
浓度为 的废水需要焦亚硫酸钠
的废水需要焦亚硫酸钠
您最近一年使用:0次
2023-12-18更新
|
143次组卷
|
2卷引用:贵州省顶效开发区顶兴学校2023-2024学年高三第二次月考化学试题
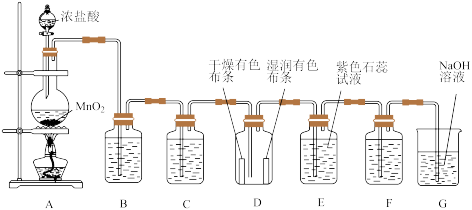
7 . 某化学兴趣小组用如图实验装置和药品制备氯气并检测氯气的相关性质,请回答问题。_______ ;该反应中氧化剂和还原剂物质的量之比为______ 。
(2)装置B中的试剂是_______ ,作用是_______ ;装置C中的试剂是_______ ,作用是_______ 。
(3)装置D中的现象是_______ ,通过这一现象能得出的结论是_______ 。
(4)若要证明氯气具有氧化性,可在装置F中盛装下列试剂中的_______ (填序号),证明氯气有氧化性的实验现象是_______ ,发生的化学方程式是_______ 。
a.酸性KMnO4溶液 b.FeCl3溶液 c.CuSO4溶液 d.淀粉碘化钾溶液
(5)装置G的作用是_______ 。
(2)装置B中的试剂是
(3)装置D中的现象是
(4)若要证明氯气具有氧化性,可在装置F中盛装下列试剂中的
a.酸性KMnO4溶液 b.FeCl3溶液 c.CuSO4溶液 d.淀粉碘化钾溶液
(5)装置G的作用是
您最近一年使用:0次
解题方法
8 . A为一种常见的金属单质,B、E、F、G是含有A元素的常见化合物。回答下列问题:

(1)写出化学式:B_______ ,F_______ 。
(2)写出E到F转化过程的化学方程式_______ 。
(3)检验G溶液中金属阳离子的常用试剂为_______ ,证明该离子存在的现象为_______ 。
(4)写出G到B转化过程的化学方程式_______ ,该反应中还原剂为_______ 。
(5)若标准状况下A与盐酸反应产生44.8L气体,则消耗A的质量为_______ g。

(1)写出化学式:B
(2)写出E到F转化过程的化学方程式
(3)检验G溶液中金属阳离子的常用试剂为
(4)写出G到B转化过程的化学方程式
(5)若标准状况下A与盐酸反应产生44.8L气体,则消耗A的质量为
您最近一年使用:0次
名校
解题方法
9 . 用甲、乙两个装置都可以制取溴苯,下列说法正确的是
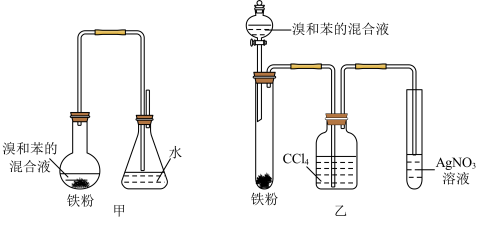

A.反应的化学方程式为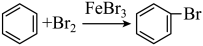 |
| B.反应后圆底烧瓶得褐色混合物,是因为溴苯有颜色 |
| C.乙装置的优点是可证明该反应是取代反应 |
| D.甲装置左侧的长导管只起到导气的作用 |
您最近一年使用:0次
名校
10 . 1962年,化学家NeilBartlett用 与Xe首次合成了Xe的第一种化合物——六氟合铂酸氙(
与Xe首次合成了Xe的第一种化合物——六氟合铂酸氙( ),实验证明
),实验证明 是一种含有
是一种含有 的离子化合物,常温下很稳定,遇水强烈水解生成
的离子化合物,常温下很稳定,遇水强烈水解生成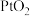 、HF、Xe、
、HF、Xe、 。下列叙述正确的是
。下列叙述正确的是
 与Xe首次合成了Xe的第一种化合物——六氟合铂酸氙(
与Xe首次合成了Xe的第一种化合物——六氟合铂酸氙( ),实验证明
),实验证明 是一种含有
是一种含有 的离子化合物,常温下很稳定,遇水强烈水解生成
的离子化合物,常温下很稳定,遇水强烈水解生成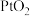 、HF、Xe、
、HF、Xe、 。下列叙述正确的是
。下列叙述正确的是A.在合成 的反应中Xe作氧化剂 的反应中Xe作氧化剂 | B. 水解过程中被还原的元素为Pt和Xe 水解过程中被还原的元素为Pt和Xe |
| C.通常情况下,Xe具有较强的还原性 | D.1 mol  完全水解,转移4 mol电子 完全水解,转移4 mol电子 |
您最近一年使用:0次
2023-10-17更新
|
258次组卷
|
6卷引用:贵州省部分中学2023-2024学年高三上学期第四次月考化学试题



