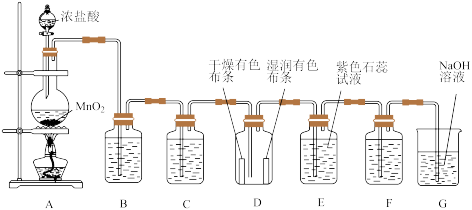
某化学兴趣小组用如图实验装置和药品制备氯气并检测氯气的相关性质,请回答问题。_______ ;该反应中氧化剂和还原剂物质的量之比为______ 。
(2)装置B中的试剂是_______ ,作用是_______ ;装置C中的试剂是_______ ,作用是_______ 。
(3)装置D中的现象是_______ ,通过这一现象能得出的结论是_______ 。
(4)若要证明氯气具有氧化性,可在装置F中盛装下列试剂中的_______ (填序号),证明氯气有氧化性的实验现象是_______ ,发生的化学方程式是_______ 。
a.酸性KMnO4溶液 b.FeCl3溶液 c.CuSO4溶液 d.淀粉碘化钾溶液
(5)装置G的作用是_______ 。
(2)装置B中的试剂是
(3)装置D中的现象是
(4)若要证明氯气具有氧化性,可在装置F中盛装下列试剂中的
a.酸性KMnO4溶液 b.FeCl3溶液 c.CuSO4溶液 d.淀粉碘化钾溶液
(5)装置G的作用是
更新时间:2024-04-10 11:31:52
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室制备Cl2O并用水吸收制备次氯酸的实验装置如图所示。
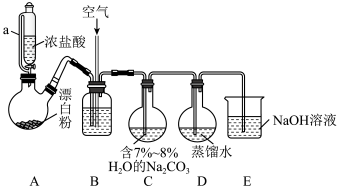
已知:25℃时Cl2O为棕黄色气体,沸点为2.0℃,易溶于水同时生成次氯酸溶液,在3.8℃时即可逐步分解,与有机物接触时会爆炸,与氧气混合时的爆炸界限为25%。
回答下列问题:
(1)双口烧瓶中发生反应的化学方程式为___ 。
(2)装置B中盛放的适宜试剂是___ ,为得到V(Cl2):V(空气)≈1:3的混合气体,可采用的方法是___ ,实验过程中通空气的目的是___ 。
(3)装置C需控温在1~10℃,合适的措施是___ ,烧瓶中生成Cl2O的化学方程式为___ 。
(4)装置D得到的是HClO或HClO与氯水的混合溶液,用滴定法测定其中有效氯的浓度。主要实验步骤如下:量取装置D中的溶液amL于碘量瓶中,用适量水稀释,然后加入足量NaI和稀硫酸,置于暗处静置一段时间后,用cmol/LNa2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液VmL。则制得的溶液有效氯的浓度为___ g/L(列出计算式即可,有效氯浓度=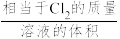 )。
)。

已知:25℃时Cl2O为棕黄色气体,沸点为2.0℃,易溶于水同时生成次氯酸溶液,在3.8℃时即可逐步分解,与有机物接触时会爆炸,与氧气混合时的爆炸界限为25%。
回答下列问题:
(1)双口烧瓶中发生反应的化学方程式为
(2)装置B中盛放的适宜试剂是
(3)装置C需控温在1~10℃,合适的措施是
(4)装置D得到的是HClO或HClO与氯水的混合溶液,用滴定法测定其中有效氯的浓度。主要实验步骤如下:量取装置D中的溶液amL于碘量瓶中,用适量水稀释,然后加入足量NaI和稀硫酸,置于暗处静置一段时间后,用cmol/LNa2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至浅黄色,再加入1mL淀粉,继续滴定至蓝色刚好消失,消耗Na2S2O3溶液VmL。则制得的溶液有效氯的浓度为
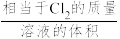 )。
)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】一氧化二氯(Cl2O)是国际公认的高效安全灭菌消毒剂,其部分性质如下:
实验室制备原理:2Na2CO3+H2O+2Cl2 2NaCl+2NaHCO3+Cl2O。
2NaCl+2NaHCO3+Cl2O。
现用如图所示装置设计实验制备少量Cl2O。
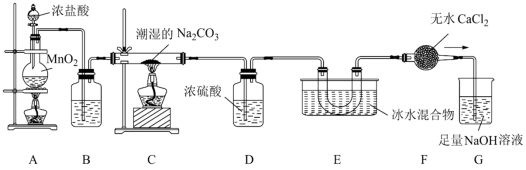
(1)盛有MnO2的仪器名称为______ 。
(2)仪器组装完成,加药品前应进行的实验操作是______ 。
(3)装置A中发生反应的离子方程式为______ 。
(4)装置F的作用是______ 。
(5)E装置中冰水混合物的作用是______ 。
(6)将Cl2O通入含NaOH的溶液中发生的化学方程式为______ 。
| 物理性质 | 化学性质 |
| 常温下,Cl2O是棕黄色、有刺激性气味的气体;熔点-120.6℃;沸点2.0℃。 | Cl2O热稳定性差,常温下即可分解;易溶于水,同时反应生成次氯酸。 |
 2NaCl+2NaHCO3+Cl2O。
2NaCl+2NaHCO3+Cl2O。现用如图所示装置设计实验制备少量Cl2O。

(1)盛有MnO2的仪器名称为
(2)仪器组装完成,加药品前应进行的实验操作是
(3)装置A中发生反应的离子方程式为
(4)装置F的作用是
(5)E装置中冰水混合物的作用是
(6)将Cl2O通入含NaOH的溶液中发生的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】图中为实验室制取氯气及性质验证的装置图:
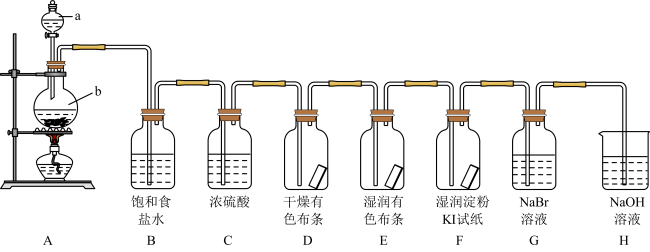
回答下列问题:
(1)仪器a的名称_______ ,写出装置A中反应的化学方程式_______ 。
(2)在装置D中可观察到的现象是_______ ,装置E中可观察到的现象是_______ ,装置F中可观察到的现象是_______ 。
(3)装置B的作用为_______ ,装置C的作用为_______ ,装置H的作用为_______ ,写出装置H的化学方程式_______ 。

回答下列问题:
(1)仪器a的名称
(2)在装置D中可观察到的现象是
(3)装置B的作用为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验是进行化学研究的重要手段之一。请回答下列问题:
(1)实验室需要450 mL 1 mol·L-1硫酸溶液。
①配制1 mol·L-1的硫酸时,下列仪器肯定不需要的是_________ (填标号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器有________________ 。
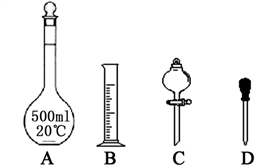
②在容量瓶的使用方法中,下列操作正确的是_______ (填写序号)。
a.使用容量瓶前检验是否漏水
b.容量瓶用水洗净后,再用待配溶液洗涤
c.配制硫酸溶液时,用量筒量取浓硫酸后用玻璃 棒引流注入容量瓶中,然后加水。
棒引流注入容量瓶中,然后加水。
(2)如图装置中,若A中盛有品红溶液,B中盛有氢氧化钠溶液。
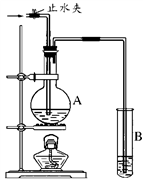
①向A中通入足量的SO2气体,然后加热,A中的现象_____________ 。
②向A中通入足量的Cl2气体,然后加热,A中的现象是_____________ 。
③若将SO2和Cl2按1:1体积比(同温同压)同时通入A中,则溶液不褪色。原因是SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化,该反应的离子方程式是______________________ 。
(3)若(2)中的A中盛的是浓硫酸,加入足量的锌后,关闭止水夹并加热,进入B溶液的气体的化学式为____________ ;B中发生反应的离子方程式__________________________________________ 。
(1)实验室需要450 mL 1 mol·L-1硫酸溶液。
①配制1 mol·L-1的硫酸时,下列仪器肯定不需要的是

②在容量瓶的使用方法中,下列操作正确的是
a.使用容量瓶前检验是否漏水
b.容量瓶用水洗净后,再用待配溶液洗涤
c.配制硫酸溶液时,用量筒量取浓硫酸后用玻璃
 棒引流注入容量瓶中,然后加水。
棒引流注入容量瓶中,然后加水。(2)如图装置中,若A中盛有品红溶液,B中盛有氢氧化钠溶液。

①向A中通入足量的SO2气体,然后加热,A中的现象
②向A中通入足量的Cl2气体,然后加热,A中的现象是
③若将SO2和Cl2按1:1体积比(同温同压)同时通入A中,则溶液不褪色。原因是SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化,该反应的离子方程式是
(3)若(2)中的A中盛的是浓硫酸,加入足量的锌后,关闭止水夹并加热,进入B溶液的气体的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】元素价一类二维图是学习元素化合物知识的重要模型,下图为铁元素的价一类二维图:

请问答下列问题:
(1)炽热的铁水注入模具前,模具必须彻底干燥,是为了避免_______ 反应的发生(写化学方程式)。
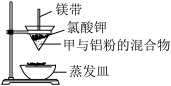
(2)高温下利用铝粉与甲反应可用来焊接钢轨。某化学兴趣小组欲用以下装置探究甲与铝粉的反应,实验发现:反应放出大量的热,并发出耀眼的光芒,纸漏斗的下部被烧穿,有熔融物落入沙中。
①铝粉与甲反应的化学方程式为_______ 。
②该小组玲玲同学欲探究该熔融物中是否含有+3价铁,进行了如下实验:取出适量的熔融物,加入稀盐酸充分溶解,滴加KSCN溶液,无明显现象,说明熔融物中无+3价铁。芳芳同学不同意此观点,原因为:_______ 。
(3)戊、己分别能与碱反应能生成丙和丁。若己为硫酸盐,向其溶液中加入NaOH溶液时,出现的现象有_______ 。
(4)将表面附有铁锈(主要成分是甲)的铁钉放入稀硫酸中,开始反应时主要离子方程式是_______ ;反应片刻后,向反应后溶液滴加KSCN溶液,溶液未出现红色,其原因为_______ (用离子方程式表示)。
(5)将1.12 g铁粉加入40 mL 2 mol·L 的戊溶液中(戊为氯化物),充分反应后,溶液中
的戊溶液中(戊为氯化物),充分反应后,溶液中 和
和 的物质的量浓度之比为
的物质的量浓度之比为_______ ,标准状况下至少通入_______ mL  才可完全除去溶液中的
才可完全除去溶液中的 。
。

请问答下列问题:
(1)炽热的铁水注入模具前,模具必须彻底干燥,是为了避免
(2)高温下利用铝粉与甲反应可用来焊接钢轨。某化学兴趣小组欲用以下装置探究甲与铝粉的反应,实验发现:反应放出大量的热,并发出耀眼的光芒,纸漏斗的下部被烧穿,有熔融物落入沙中。

①铝粉与甲反应的化学方程式为
②该小组玲玲同学欲探究该熔融物中是否含有+3价铁,进行了如下实验:取出适量的熔融物,加入稀盐酸充分溶解,滴加KSCN溶液,无明显现象,说明熔融物中无+3价铁。芳芳同学不同意此观点,原因为:
(3)戊、己分别能与碱反应能生成丙和丁。若己为硫酸盐,向其溶液中加入NaOH溶液时,出现的现象有
(4)将表面附有铁锈(主要成分是甲)的铁钉放入稀硫酸中,开始反应时主要离子方程式是
(5)将1.12 g铁粉加入40 mL 2 mol·L
 的戊溶液中(戊为氯化物),充分反应后,溶液中
的戊溶液中(戊为氯化物),充分反应后,溶液中 和
和 的物质的量浓度之比为
的物质的量浓度之比为 才可完全除去溶液中的
才可完全除去溶液中的 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其性质,做了如下实验:
(1) 不稳定,见光易分解生成
不稳定,见光易分解生成 和
和 。请设计实验证明有
。请设计实验证明有 生成:
生成:_______________________ 。
(2)氯气能使湿润的红色布条褪色。对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能。请你设计实验,得出正确结论。
(1)
 不稳定,见光易分解生成
不稳定,见光易分解生成 和
和 。请设计实验证明有
。请设计实验证明有 生成:
生成:(2)氯气能使湿润的红色布条褪色。对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能。请你设计实验,得出正确结论。
| 提出问题 | 收集资料 | 提出假设 | 验证假设 | 得出结论 |
| 氯水中哪种物质能使湿润的红色布条褪色 | ①氯气有强氧化性; ②氯气与冷水反应生成盐酸和次氯酸; ③次氯酸有强氧化性 | ① ② ③ | 实验①:把红色干布条放入充满干燥氯气的集气瓶中,布条不褪色; 实验②: 实验③:把红色布条放入稀盐酸中,布条不褪色 |
您最近一年使用:0次



