5. Ⅰ.硒(Se)是一种重要的化学元素,在医药、农业、能源和电子等领域有广泛应用。
(1)以下不能用元素周期律解释的是___________。
| A.键的极性:H−Se < H−Br | B.原子半径:Se > Br |
| C.稳定性:H2Se < HBr | D.酸性:H2SeO3 < HBrO4 |
(2)硒化铅可用作玻璃和陶瓷的着色剂,其晶胞结构如图所示:
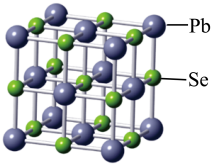
①Se的电负性2.4、Pb的电负性1.9,判断硒化铅中Se与Pb之间的化学键是
___________。
A.离子键
B.共价键
②晶体中每个Se周围与其最近的,且距离相等的Se有
___________个。
Ⅱ.工业上以精炼铜的阳极泥为原料(主要成分为Se、CuSe、Ag
2Se等)回收Se。
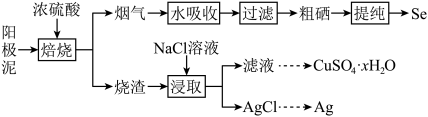
① Se难溶于水,沸点684.9℃,易于与O
2反应。
② 室温下K
sp(Ag
2SO
4)=10
−5;K
sp(AgCl)=10
−9.75。
(3)“焙烧”前,将阳极泥中大块颗粒粉碎的目的是
___________。
(4)“烟气”中含有SO
2和SeO
2,被水吸收发生反应,SO
2与和SeO
2的物质的量之比为
___________,SeO
2体现了
___________。
A.氧化性
B.还原性
(5)“提纯”步骤中用到真空蒸馏工艺,真空的作用是
___________、
___________。
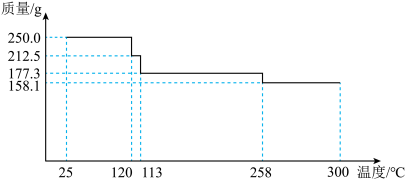
(6)小组同学测定某CuSO
4∙xH
2O晶体样品热分解的质量变化情况(如图所示),258℃失去全部结晶水,x=
___________。(结果保留2位小数)
(7)常温“浸取”步骤中,加入NaCl能否使Ag
2SO
4完全转化为AgCl?结合平衡原理和计算过程回答
___________。
Ⅲ.亚硒酸(H
2SeO
3)是主要的含硒化合物,是二元弱酸。常温下,H
2SeO
3溶液中某些微粒的物质的量分数与pH的关系如图所示:
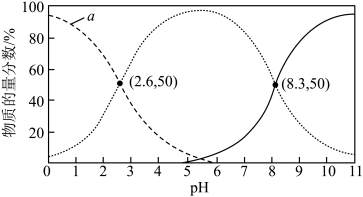
(8)下列说法正确的是___________。
A.曲线a表示的是SeO 物质的量分数随pH变化 物质的量分数随pH变化 |
| B.Ka1=10−5.5 |
C.pH=3时, =100.4 =100.4 |
D.向H2SeO3溶液中逐滴加入NaOH溶液,pH=8.3时溶液中存在:2c(Na+)=3[c(HSeO )+ c(SeO )+ c(SeO )+ c(H2SeO3)] )+ c(H2SeO3)] |
(9)向滴有酚酞的H
2SeO
3溶液中加入氨水,当溶液由粉红色变为红色时,反应的离子方程式为
___________。