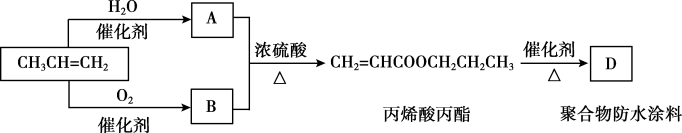
Ⅰ.对甲苯磺酸是一种白色晶体,熔点107℃,易溶于醇、醚和水,是用途广泛的化工原料。
(2)写出反应的化学方程式。___________
Ⅱ.根据对甲苯磺酸的结构,有同学推测对甲苯磺酸的性质和硫酸相似,进行了如下探究:
(3)对甲苯磺酸可能是强酸,电离方程式: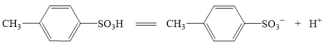 ,设计简单实验证明猜想。
,设计简单实验证明猜想。___________
(4)采用如图所示装置进行实验,观察到蔗糖迅速变黑。上述实验现象说明对甲苯磺酸具有___________ 。
(5)向吸收液中滴加一定量___________ 溶液,仍未观察到明显现象,说明对甲苯磺酸不具有强氧化性。
A.Ba(OH)2 B.NaCl C.CaCl2
Ⅲ.对甲苯磺酸可做酯化反应的催化剂,催化合成丙酸乙酯。
将0.2 mol丙酸(M=74 g∙mol−1)、1 g对甲苯磺酸和0.24 mol乙醇(M=46 g∙mol−1)加入三口瓶中,加热进行反应。反应结束后将反应液过滤,分别经水、碳酸钠溶液、饱和食盐水洗涤,干燥后进行蒸馏,蒸出17.4 g馏分。
(6)计算该反应的产率____ 。(产率= ,写出计算过程,结果保留1位小数)
,写出计算过程,结果保留1位小数)
(7)请评价用对甲苯磺酸代替浓硫酸做酯化反应催化剂的优点___________ 。
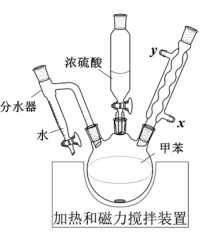
| A.当分水器中的水量不再增加时,停止加热 |
| B.分水器可将反应体系中的甲苯移除 |
| C.烧瓶中不需要添加沸石 |
| D.冷凝水从x口进入 |
Ⅱ.根据对甲苯磺酸的结构,有同学推测对甲苯磺酸的性质和硫酸相似,进行了如下探究:
(3)对甲苯磺酸可能是强酸,电离方程式:
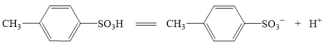 ,设计简单实验证明猜想。
,设计简单实验证明猜想。(4)采用如图所示装置进行实验,观察到蔗糖迅速变黑。上述实验现象说明对甲苯磺酸具有
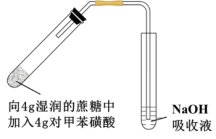
(5)向吸收液中滴加一定量
A.Ba(OH)2 B.NaCl C.CaCl2
Ⅲ.对甲苯磺酸可做酯化反应的催化剂,催化合成丙酸乙酯。
将0.2 mol丙酸(M=74 g∙mol−1)、1 g对甲苯磺酸和0.24 mol乙醇(M=46 g∙mol−1)加入三口瓶中,加热进行反应。反应结束后将反应液过滤,分别经水、碳酸钠溶液、饱和食盐水洗涤,干燥后进行蒸馏,蒸出17.4 g馏分。
(6)计算该反应的产率
 ,写出计算过程,结果保留1位小数)
,写出计算过程,结果保留1位小数)(7)请评价用对甲苯磺酸代替浓硫酸做酯化反应催化剂的优点
更新时间:2024/04/16 18:59:59
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
【推荐1】已知卤代烃A是烷烃的一氯代物,A的mol质量为64.5g/mol,B为一种常见调味剂,D为一种无机酸与一种烯烃衍生物的混合物,G是一种芳香物质。
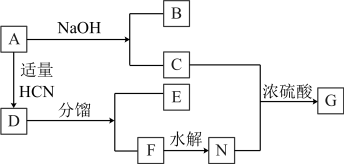
(1)已知CN-的性质和卤素离子类似,那么乙烯和HCN反应的方程式为___________ 。
(2)写出合成G的方程式___________ 。
(3)A到B,C的反应类型___________
(4)下列选项正确的是:___________

(1)已知CN-的性质和卤素离子类似,那么乙烯和HCN反应的方程式为
(2)写出合成G的方程式
(3)A到B,C的反应类型
(4)下列选项正确的是:___________
| A.C可以使酸性高锰酸钾褪色 |
| B.E具有漂白性 |
| C.生成G的过程中,浓硫酸只起到催化作用 |
| D.同H+浓度下,E与N中N的物质的量浓度更大 |
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】菠萝酯F是一种具有菠萝香味的赋香剂,其合成路线如下:
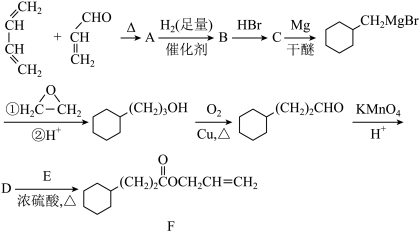
已知: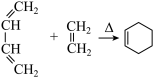 ;RMgBr
;RMgBr 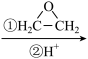 RCH2CH2OH+
RCH2CH2OH+ 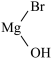
(1)A的结构简式为______ ,A中所含官能团的名称是____ 。
(2)由A生成B的反应类型是_____ ,E的某同分异构体只有一种相同化学环境的氢,该同分异构体的结构简式为________ 。
(3)写出D和E反应生成F的化学方程式______ 。
(4)结合题给信息,以溴乙烷和环氧乙烷为原料制备1-丁醇,设计合成路线(其他试剂任选)。合成路线流程图示例:CH3CH2Cl CH3CH2OH
CH3CH2OH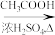 CH3COOCH2CH3
CH3COOCH2CH3___

已知:
 ;RMgBr
;RMgBr  RCH2CH2OH+
RCH2CH2OH+ 
(1)A的结构简式为
(2)由A生成B的反应类型是
(3)写出D和E反应生成F的化学方程式
(4)结合题给信息,以溴乙烷和环氧乙烷为原料制备1-丁醇,设计合成路线(其他试剂任选)。合成路线流程图示例:CH3CH2Cl
 CH3CH2OH
CH3CH2OH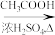 CH3COOCH2CH3
CH3COOCH2CH3
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】下图为学生设计的制取溴苯的装置。
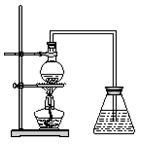
(1)图中的错误之处有____________ 处。
(2)往烧瓶中依次加入铁粉、苯和_______________ 。
(3)与烧瓶中连接的垂直向上的导管的作用是___________________ 。
(4)烧瓶中发生反应的化学方程式为_______________ 。
(5)反应完毕后,向锥形瓶中的溶液中滴入AgNO3溶液,现象为__________________ 。
(6)反应完毕后,将烧瓶中橙红色的液体倒入盛有足量Na OH的烧杯中,充分振荡,静置,分液得无色油状产品,写出离子方程式__________________________ 。

(1)图中的错误之处有
(2)往烧瓶中依次加入铁粉、苯和
(3)与烧瓶中连接的垂直向上的导管的作用是
(4)烧瓶中发生反应的化学方程式为
(5)反应完毕后,向锥形瓶中的溶液中滴入AgNO3溶液,现象为
(6)反应完毕后,将烧瓶中橙红色的液体倒入盛有足量Na OH的烧杯中,充分振荡,静置,分液得无色油状产品,写出离子方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
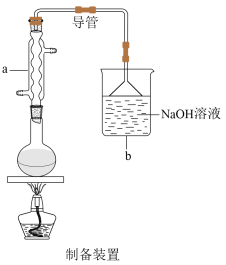
【推荐2】1-溴丁烷可用于合成麻醉药盐酸丁卡因,也用于生产染料和香料,是稀有元素萃取的溶剂及有机合成的中间体,其制备如图(夹持装置略): (浓)
(浓)
ⅱ.
ⅲ. (浓)
(浓)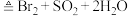
请回答下列问题:
(1)在反应时,若选用较浓的硫酸作为反应物,得到的产品会呈黄色,为除去颜色,最好选择下列的_______ (填标号)溶液来洗涤产品。
A.四氯化碳 B.硫酸钠 C.氢氧化钠 D.亚硫酸钠
产品选择上述溶液洗涤后,还需要用蒸馏水洗涤一次,洗涤液与产品分离的操作是_______ (填操作名称)。
(2)分离得到的有机层依次用适量的水、饱和 溶液、水洗涤、用无水
溶液、水洗涤、用无水 干燥,蒸馏,得到最终产品。若投入正丁醇
干燥,蒸馏,得到最终产品。若投入正丁醇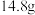 ,得到产物
,得到产物 ,则1-溴丁烷的产率为
,则1-溴丁烷的产率为______ %(保留一位小数)。
(3)探究小组为研究1-溴丁烷的水解反应和消去反应,设计如下探究实验:_______ 。
②实验ⅲ的有机化学反应方程式是_______ 。
③为深入研究1-溴丁烷与 溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):
溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):
Ⅰ.甲同学认为不能依据酸性高锰酸钾溶液褪色,判断A中发生消去反应,理由是_______ 。
Ⅱ.乙同学对实验进行了改进,依据实验现象可判断是否发生消去反应,改进的方案是_______ 。
 (浓)
(浓)
ⅱ.

ⅲ.
 (浓)
(浓)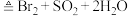
请回答下列问题:
(1)在反应时,若选用较浓的硫酸作为反应物,得到的产品会呈黄色,为除去颜色,最好选择下列的
A.四氯化碳 B.硫酸钠 C.氢氧化钠 D.亚硫酸钠
产品选择上述溶液洗涤后,还需要用蒸馏水洗涤一次,洗涤液与产品分离的操作是
(2)分离得到的有机层依次用适量的水、饱和
 溶液、水洗涤、用无水
溶液、水洗涤、用无水 干燥,蒸馏,得到最终产品。若投入正丁醇
干燥,蒸馏,得到最终产品。若投入正丁醇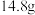 ,得到产物
,得到产物 ,则1-溴丁烷的产率为
,则1-溴丁烷的产率为(3)探究小组为研究1-溴丁烷的水解反应和消去反应,设计如下探究实验:
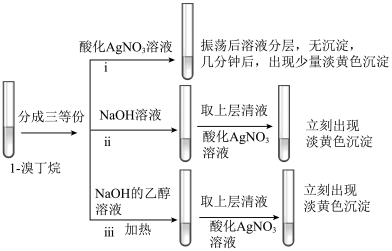
②实验ⅲ的有机化学反应方程式是
③为深入研究1-溴丁烷与
 溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):
溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):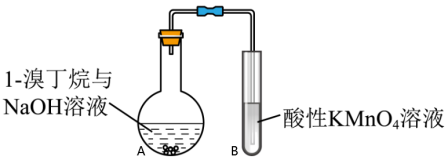
Ⅰ.甲同学认为不能依据酸性高锰酸钾溶液褪色,判断A中发生消去反应,理由是
Ⅱ.乙同学对实验进行了改进,依据实验现象可判断是否发生消去反应,改进的方案是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】已知在中性条件下(pH=5~8),甲苯可以被高锰酸钾中性溶液氧化成苯甲酸钾,实验室用下列方法制备苯甲酸。
主要实验装置和流程如图:
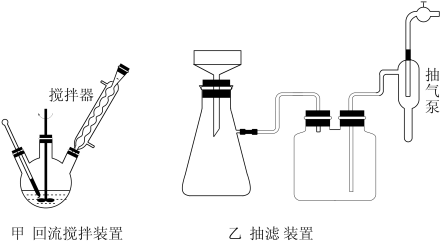
反应试剂、产物的物理性质如表:
实验方法:一定量的甲苯和KMnO4溶液置于图甲装置中,在90℃时,反应一段时间,再停止反应,按如图流程分离出苯甲酸和回收未反应的甲苯。
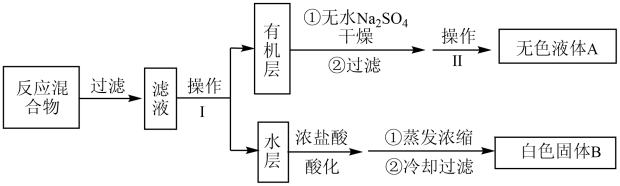
(1)已知反应混合物过滤后滤渣中含有 ,则甲中化学反应方程式为
,则甲中化学反应方程式为_______ 。
(2)无色液体A的结构简式为_______ 。操作Ⅱ为_______ 。
(3)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,加亚硫酸氢钾的目的是_______ 。
(4)下列关于仪器的组装或使用正确的是_______(填标号)。
(5)除去残留在苯甲酸中的甲苯应先加入_______ ,分液,水层再加入_______ ,然后抽滤,干燥即可得到苯甲酸。
(6)纯度测定:称取1.220g产品,配成100mL溶液,取其中25.00mL溶液,用0.1mol/L的KOH标准溶液进行滴定,中和滴定时应该使用的指示剂为_______ (A.甲基橙;B.石蕊;C.酚酞),当滴加最后一滴标准KOH溶液,溶液由_______ 表示达到滴定终点,测得消耗KOH溶液的体积为24.00mL,则产品中苯甲酸的质量分数为_______ 。
主要实验装置和流程如图:

反应试剂、产物的物理性质如表:
| 名称 | 相对分子质量 | 性状 | 熔点/℃ | 沸点/℃ | 密度/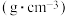 | 溶解性 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 甲苯 | 92 | 无色液体、易燃、易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 易溶 | 易溶 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |

(1)已知反应混合物过滤后滤渣中含有
 ,则甲中化学反应方程式为
,则甲中化学反应方程式为(2)无色液体A的结构简式为
(3)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,加亚硫酸氢钾的目的是
(4)下列关于仪器的组装或使用正确的是_______(填标号)。
| A.抽滤可以加快过滤速率,得到较干燥的沉淀 |
| B.安装电动搅拌器时,搅拌器下端不能与三颈烧瓶底、温度计等接触 |
| C.图甲回流搅拌装置应采用直接加热的方法 |
| D.冷凝管中水的流向是下进上出 |
(6)纯度测定:称取1.220g产品,配成100mL溶液,取其中25.00mL溶液,用0.1mol/L的KOH标准溶液进行滴定,中和滴定时应该使用的指示剂为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】将SO2分别通入下列4种溶液中,请回答下列问题:
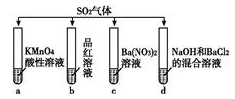
(1)试管a出现溶液褪色的现象,说明SO2具有________ 性;试管b出现溶液褪色的现象,说明SO2具有________ 性。
(2)试管d出现白色沉淀,该沉淀能够溶解在稀盐酸中,写出生成该沉淀的离子方程式:________________ 。
(3)如果将试管d中的NaOH更换为Br2和BaCl2的混合溶液,可以得到一种难溶于强酸的白色沉淀;写出该过程中发生氧化还原反应的离子方程式:________ 。
(4)试管c中也可得到难溶于强酸的白色沉淀,请你简述该沉淀的生成原因:________ 。

(1)试管a出现溶液褪色的现象,说明SO2具有
(2)试管d出现白色沉淀,该沉淀能够溶解在稀盐酸中,写出生成该沉淀的离子方程式:
(3)如果将试管d中的NaOH更换为Br2和BaCl2的混合溶液,可以得到一种难溶于强酸的白色沉淀;写出该过程中发生氧化还原反应的离子方程式:
(4)试管c中也可得到难溶于强酸的白色沉淀,请你简述该沉淀的生成原因:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ.以下是有关SO2、Cl2的性质实验。
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。
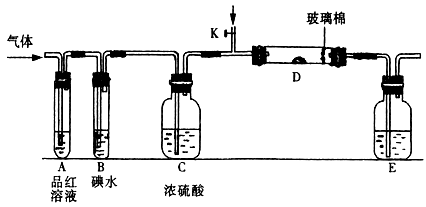
若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?______ (填“相同”或“不相同”);若装置D中装的是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为______ 。
②SO2通入B中,溶液颜色退去,则该反应的离子方程式为______ 。
(2) 某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母)______ ,仍然无法观察到沉淀产生。
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成–2价酸根离子X,X中S和O的质量比为2∶3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式______ 。
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如图
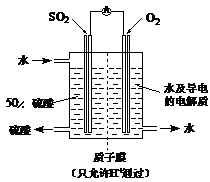
含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。通入SO2的电极为______ 极,其电极反应式为______ ;电池的总反应式______
Ⅱ.实验是化学研究的基础,关于下列各装置图的叙述正确的是______ (填序号)
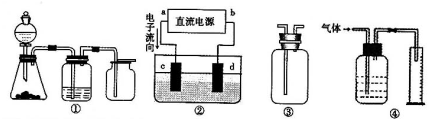
A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正极,d为阳极
C.装置③可用于收集H2、NH3、Cl2,、HCl、NO2等
D.装置④能用于测量气体体积
Ⅲ .用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。下列说法中正确的是______ (填序号)

A.铅蓄电池负极的反应式为:Pb-2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。

若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?
②SO2通入B中,溶液颜色退去,则该反应的离子方程式为
(2) 某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母)
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成–2价酸根离子X,X中S和O的质量比为2∶3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如图

含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。通入SO2的电极为
Ⅱ.实验是化学研究的基础,关于下列各装置图的叙述正确的是

A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正极,d为阳极
C.装置③可用于收集H2、NH3、Cl2,、HCl、NO2等
D.装置④能用于测量气体体积
Ⅲ .用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。下列说法中正确的是

A.铅蓄电池负极的反应式为:Pb-2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-
您最近半年使用:0次
【推荐3】硫酸亚铁(FeSO4)加热至高温会分解,生成Fe2O3和非金属氧化物。
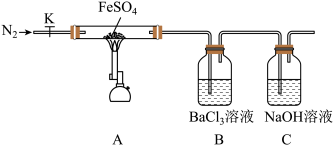
(1)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置进行实验。
①实验开始时通入氮气的目的是_______ 。
②B中现象证明分解产物中含有_______ (写化学式)。
(2)某同学欲验证分解产物中含有的另一种非金属氧化物。

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A →_______ →_______ 。
②能证明生成了另一种非金属氧化物的现象是_______ 。
(3)写出该条件下硫酸亚铁受热分解的化学方程式_______ 。

(1)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置进行实验。
| 操作步骤 | 实验现象 |
| 打开K,通入一段时间的N2,关闭活塞K,加热A中的玻璃管一段时间 | B中产生大量白色沉淀 |
| A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却 | 硬质玻璃管中最终可以看到红棕色固体 |
②B中现象证明分解产物中含有
(2)某同学欲验证分解产物中含有的另一种非金属氧化物。

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A →
②能证明生成了另一种非金属氧化物的现象是
(3)写出该条件下硫酸亚铁受热分解的化学方程式
您最近半年使用:0次