将SO2分别通入下列4种溶液中,请回答下列问题:
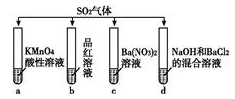
(1)试管a出现溶液褪色的现象,说明SO2具有________ 性;试管b出现溶液褪色的现象,说明SO2具有________ 性。
(2)试管d出现白色沉淀,该沉淀能够溶解在稀盐酸中,写出生成该沉淀的离子方程式:________________ 。
(3)如果将试管d中的NaOH更换为Br2和BaCl2的混合溶液,可以得到一种难溶于强酸的白色沉淀;写出该过程中发生氧化还原反应的离子方程式:________ 。
(4)试管c中也可得到难溶于强酸的白色沉淀,请你简述该沉淀的生成原因:________ 。

(1)试管a出现溶液褪色的现象,说明SO2具有
(2)试管d出现白色沉淀,该沉淀能够溶解在稀盐酸中,写出生成该沉淀的离子方程式:
(3)如果将试管d中的NaOH更换为Br2和BaCl2的混合溶液,可以得到一种难溶于强酸的白色沉淀;写出该过程中发生氧化还原反应的离子方程式:
(4)试管c中也可得到难溶于强酸的白色沉淀,请你简述该沉淀的生成原因:
更新时间:2018-02-23 09:35:00
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】一种由氯气与熔化的硫反应制取 的装置(夹持和加热装置已省略)如图所示:
的装置(夹持和加热装置已省略)如图所示:

已知:① 和
和 反应生成
反应生成 ,同时有少量
,同时有少量 及其他氯化物生成。
及其他氯化物生成。
②常温下, 是一种浅黄色的油状液体,极易水解。
是一种浅黄色的油状液体,极易水解。
③ 的沸点为
的沸点为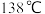 ,
, 的沸点为
的沸点为 ,硫的熔点为
,硫的熔点为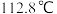 、沸点为
、沸点为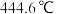 。
。
回答下列问题:
(1)实验过程中,从装置 中逸出的气体为
中逸出的气体为___________ (填化学式),装置 中盛放的试剂是
中盛放的试剂是___________ 。
(2)对装置 进行加热的合适方式是
进行加热的合适方式是___________ (填标号)。
(3)装置D中的错误之处是___________ (写一处即可)。
(4)装置F的作用是___________ (写一点即可)。
(5)纯化 :向粗产品中加入
:向粗产品中加入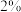 的单质硫和
的单质硫和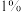 的活性炭,后续操作是
的活性炭,后续操作是________ 。
(6)取约 于试管中,滴入少量水,试管口放湿润的品红试纸,发现试管口有白雾,品红试纸褪色,试管中有淡黄色固体生成,该反应的化学方程式为
于试管中,滴入少量水,试管口放湿润的品红试纸,发现试管口有白雾,品红试纸褪色,试管中有淡黄色固体生成,该反应的化学方程式为___________ 。
(7)实验结束时,装置C中烧瓶底部有少量硫附着,可用热的NaOH浓溶液洗涤,已知产物之一为Na2S2O3,该反应的离子方程式为___________________________ 。
 的装置(夹持和加热装置已省略)如图所示:
的装置(夹持和加热装置已省略)如图所示:
已知:①
 和
和 反应生成
反应生成 ,同时有少量
,同时有少量 及其他氯化物生成。
及其他氯化物生成。②常温下,
 是一种浅黄色的油状液体,极易水解。
是一种浅黄色的油状液体,极易水解。③
 的沸点为
的沸点为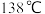 ,
, 的沸点为
的沸点为 ,硫的熔点为
,硫的熔点为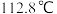 、沸点为
、沸点为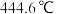 。
。回答下列问题:
(1)实验过程中,从装置
 中逸出的气体为
中逸出的气体为 中盛放的试剂是
中盛放的试剂是(2)对装置
 进行加热的合适方式是
进行加热的合适方式是| 选项 | A | B | C | D |
| 加热方式 | 水浴 | 甘油浴 | 沙浴 | 锡浴 |
极限温度/ | 98 | 220 | 400 | 600 |
(4)装置F的作用是
(5)纯化
 :向粗产品中加入
:向粗产品中加入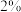 的单质硫和
的单质硫和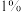 的活性炭,后续操作是
的活性炭,后续操作是(6)取约
 于试管中,滴入少量水,试管口放湿润的品红试纸,发现试管口有白雾,品红试纸褪色,试管中有淡黄色固体生成,该反应的化学方程式为
于试管中,滴入少量水,试管口放湿润的品红试纸,发现试管口有白雾,品红试纸褪色,试管中有淡黄色固体生成,该反应的化学方程式为(7)实验结束时,装置C中烧瓶底部有少量硫附着,可用热的NaOH浓溶液洗涤,已知产物之一为Na2S2O3,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】.下列转化关系图中,A、B、C、D、E常温下为气体,B、E、F、K为单质,其中F为黑色固体;C、D均能使澄清的石灰水变浑浊,D、E均能使品红溶液褪色;I是一种红棕色固体氧化物。
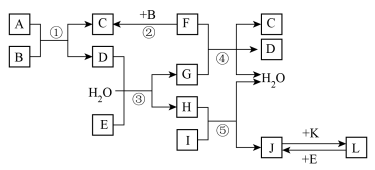
请回答下列问题:
⑴C的电子式为。
⑵检验溶液L中金属阳离子的方法是。
⑶反应③的离子方程式为。
⑷F与G的浓溶液反应的化学方程式为。
⑸气体A的密度为2.68g·L-1(标准状况),通过计算、推理,可确定A的分子式为。

请回答下列问题:
⑴C的电子式为。
⑵检验溶液L中金属阳离子的方法是。
⑶反应③的离子方程式为。
⑷F与G的浓溶液反应的化学方程式为。
⑸气体A的密度为2.68g·L-1(标准状况),通过计算、推理,可确定A的分子式为。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组为探究浓硫酸的相关性质,进行了如下几个实验:
实验I:在一个白色点滴板的两个孔穴中先分别放入一张小纸片、少量胆矾晶体;然后再分别滴加几滴浓硫酸,观察现象。回答下列问题:
(1)浓硫酸滴入小纸片上,小纸片变黑,说明浓硫酸具有___ 性;
硫酸滴入胆矾晶体中,胆矾变________ (填颜色变化),说明浓硫酸具有吸水性。
实验II:该小组同学还设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。
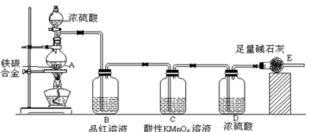
(2) mg铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A中无明显现象,其原因是:①常温下碳与浓硫酸不反应;②________________ ;
(3)写出加热时A中碳与浓硫酸发生反应的化学方程式________________ ;
(4)B中(盛放品红溶液)的现象是____________ ,C(盛放酸性KMnO4溶液)的作用是_________ ;
(5)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg,可据此求算铁的质量分数。但本套装置在设计上存在缺陷,其中导致测得铁的质量分数偏低的是(答一条即可)_________________ 。
实验I:在一个白色点滴板的两个孔穴中先分别放入一张小纸片、少量胆矾晶体;然后再分别滴加几滴浓硫酸,观察现象。回答下列问题:
(1)浓硫酸滴入小纸片上,小纸片变黑,说明浓硫酸具有
硫酸滴入胆矾晶体中,胆矾变
实验II:该小组同学还设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。

(2) mg铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A中无明显现象,其原因是:①常温下碳与浓硫酸不反应;②
(3)写出加热时A中碳与浓硫酸发生反应的化学方程式
(4)B中(盛放品红溶液)的现象是
(5)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg,可据此求算铁的质量分数。但本套装置在设计上存在缺陷,其中导致测得铁的质量分数偏低的是(答一条即可)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氮氧化物(NOX)是大气污染物之一,处理工业废气中的NOx对于环境保护具有重要的意义。
(1)在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
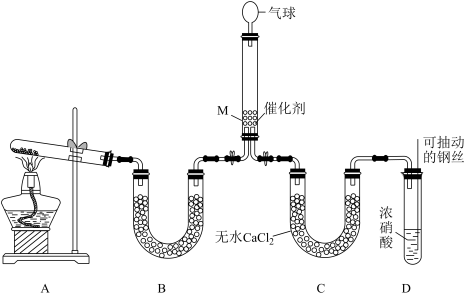
①用装置A制备NH3,其中发生反应的化学方程式为_______ ;装置B中的试剂是_______ 。
②装置D中发生反应的离子方程式是_______ ,铜丝可抽动的优点是_______ 。
(2)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O,不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图:
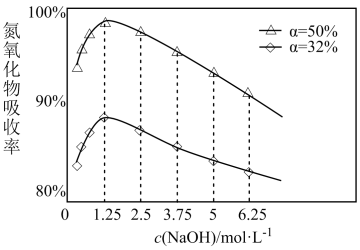
(α表示NOx中NO2的含量)
①用NaOH溶液吸收氮氧化物的最佳条件为:α=_______ ,c(NaOH)=_______ 。
②若一定体积的NOx被250mL2mol·L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为_______ 。
(1)在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。

①用装置A制备NH3,其中发生反应的化学方程式为
②装置D中发生反应的离子方程式是
(2)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O,不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图:

(α表示NOx中NO2的含量)
①用NaOH溶液吸收氮氧化物的最佳条件为:α=
②若一定体积的NOx被250mL2mol·L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如图是一套制取并验证氯气部分化学性质的实验装置。已知:I2遇淀粉变蓝色。
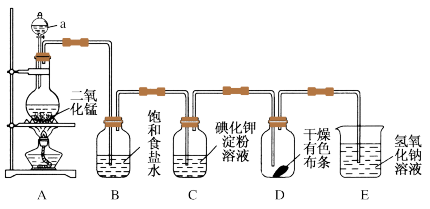
(1)写出A装置发生反应的离子方程式:___________ 。
(2)当有少量Cl2通过后,观察到装置C中溶液变成蓝色,反应的离子方程式为:___________ 。说明非金属性Cl___________ I(填“>”或“<”)。
(3)当Cl2持续通过时,装置D中干燥的有色布条能不能褪色?___________ 。(填能或者不能)
(4)装置E的作用是尾气处理,该反应的离子方程式为___________ 。
(5)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:___________ 。

(1)写出A装置发生反应的离子方程式:
(2)当有少量Cl2通过后,观察到装置C中溶液变成蓝色,反应的离子方程式为:
(3)当Cl2持续通过时,装置D中干燥的有色布条能不能褪色?
(4)装置E的作用是尾气处理,该反应的离子方程式为
(5)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
| 注意事项: 1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用。 2.密封保存,请勿与洁厕灵同时使用。 3.保质期为一年 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组对物质的性质进行相关探究。
【提出问题】氯化氢(HCl)气体显酸性吗?
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵由紫甘蓝的汁液染成蓝紫色的纸质干燥小花进行如图1的三个实验:
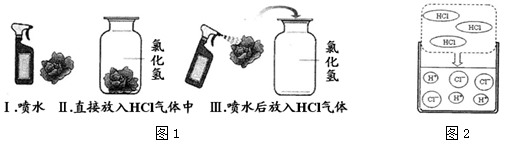
实验现象:I和Ⅱ中小花不变色;Ⅲ中小花变红色。
【查阅资料】图2是同学们查阅的氯化氢气体溶于水的微观示意图。
【实验结论】氯化氢气体不显酸性。
【交流反思】
(1)从微观角度分析氯化氢气体不显酸性的原因是________________ 。
(2)小明向实验Ⅲ中变红的小花上喷适当过量的稀氢氧化钠溶液,发现小花最后变成黄绿色,写出相关反应的化学方程式___________ 。
(3)紫甘蓝的汁液在酸性溶液中显__________ 色,在碱性溶液中显_________ 色。
(4)下列实验可以用来说明氯化氢气体不显酸性的是____________ 。
A.测试盐酸的导电性,盐酸能导电
B.干燥的碳酸钠粉末放入氯化氢气体中,不反应
C.氢气与氯气反应,生成氯化氢气体
D.干燥的碳酸钠粉末放入盐酸中,能反应
【提出问题】氯化氢(HCl)气体显酸性吗?
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵由紫甘蓝的汁液染成蓝紫色的纸质干燥小花进行如图1的三个实验:

实验现象:I和Ⅱ中小花不变色;Ⅲ中小花变红色。
【查阅资料】图2是同学们查阅的氯化氢气体溶于水的微观示意图。
【实验结论】氯化氢气体不显酸性。
【交流反思】
(1)从微观角度分析氯化氢气体不显酸性的原因是
(2)小明向实验Ⅲ中变红的小花上喷适当过量的稀氢氧化钠溶液,发现小花最后变成黄绿色,写出相关反应的化学方程式
(3)紫甘蓝的汁液在酸性溶液中显
(4)下列实验可以用来说明氯化氢气体不显酸性的是
A.测试盐酸的导电性,盐酸能导电
B.干燥的碳酸钠粉末放入氯化氢气体中,不反应
C.氢气与氯气反应,生成氯化氢气体
D.干燥的碳酸钠粉末放入盐酸中,能反应
您最近一年使用:0次



