1 . 利用下图装置制取 并验证
并验证 的性质。下列说法错误的是
的性质。下列说法错误的是
 并验证
并验证 的性质。下列说法错误的是
的性质。下列说法错误的是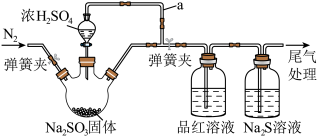
| A.导管a的作用是保证浓硫酸顺利滴下 |
B.品红溶液褪色,说明 可能具有漂白性 可能具有漂白性 |
C. 溶液中出现浑浊,证明 溶液中出现浑浊,证明 具有氧化性 具有氧化性 |
D.三颈烧瓶内反应开始前通 与反应结束后通 与反应结束后通 目的相同 目的相同 |
您最近一年使用:0次
名校
2 . 下列针对有机实验的说法正确的是
| 实验目的 | 实验操作、现象或结论 | 实验解释 | |
| A | 检验电石和水反应可产生乙炔 | 将产生的气体通过饱和食盐水后,再通入酸性 溶液中;若酸性 溶液中;若酸性 溶液褪色,说明有乙炔生成 溶液褪色,说明有乙炔生成 | 因为用饱和食盐水可以除去乙炔中混有的还原性杂质,所以证明有乙炔生成 |
| B | 探究光照条件下甲烷与氯气反应产物的种类 | 当氯气少量时,生成物中含有 、 、 、 、 、 、 等 等 | 因为 、 、 、 、 、 、 中碳氢键极性逐渐增强,所以与氯气发生取代反应的能力逐渐增强 中碳氢键极性逐渐增强,所以与氯气发生取代反应的能力逐渐增强 |
| C | 比较钠与水、钠与乙醇两个反应速率的大小 | 向两只分别盛有水和无水乙醇的烧杯中,各加入相同大小的钠,发现钠与水反应更剧烈 | 因为钠与水反应放出热量更多,温度升高更快,所以反应更剧烈 |
| D | 检验苯和液溴在 催化剂作用下生成的气体 催化剂作用下生成的气体 | 将苯、液溴、铁粉混合物反应产生的气体通入到 溶液中有淡黄色沉淀产生 溶液中有淡黄色沉淀产生 | 因为产生了淡黄色沉淀,所以证明有HBr气体生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 验证FeSO4的性质,进行如下实验。
实验序号 | 验证性质 | 实验装置 | 试剂X | 实验现象 |
① | 能与某些盐反应 |
| BaCl2溶液 | 产生白色沉淀 |
② | 能与碱反应 | NaOH溶液 | 产生白色絮状沉淀,迅速变为灰绿色,一段时间后变成红褐色 | |
③ | 具有氧化性 | 锌粒 | 锌粒表面变黑,溶液浅绿色褪去 | |
④ | 具有还原性 | KSCN溶液氯水 | 滴加KSCN溶液,无明显现象,再滴加氯水,溶液变为红色 |
下列关于该实验的说法不正确的是
A.①中产生白色沉淀的原因: |
B.②中沉淀变成红褐色的原因: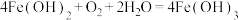 |
| C.③中用镁条(已打磨)替换锌粒,也可以证明FeSO4具有氧化性 |
| D.④中调换试剂的加入顺序,也可以证明FeSO4具有还原性 |
您最近一年使用:0次
名校
解题方法
4 . 某小组同学探究SO2与新制Cu(OH)2悬浊液反应的实验装置图如下所示:
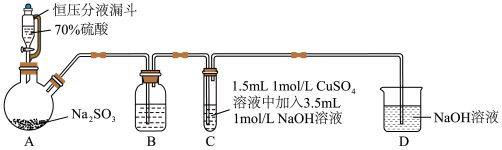
| A.配制70%硫酸溶液需要用到的仪器有烧杯、量筒、玻璃棒、胶头滴管 |
| B.装置B的作用是监控SO2流速,其中试剂可以用饱和NaHSO4溶液 |
| C.反应开始时C中出现砖红色沉淀,氧化剂和还原剂的物质的量之比为2:1 |
| D.反应后向C的溶液中加入稀盐酸酸化后,再滴加BaCl2溶液、有白色沉淀生成,证明反应中SO2作还原剂 |
您最近一年使用:0次
2024-03-16更新
|
442次组卷
|
3卷引用:2024届甘肃省兰州市高三下学期诊断考试化学试卷
2024届甘肃省兰州市高三下学期诊断考试化学试卷湖南省常德市汉寿县第一中学2023-2024学年高一下学期3月月考化学试题(已下线)高二化学下学期期末押题卷02-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(江苏专用)
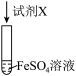
5 . 关于如图所示实验的说法,正确的是
|
|
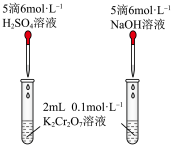
| i.推测CH3COOH的Ka和H2CO3的Ka1的大小 | ii.研究c(H+)对Cr2O 、CrO 、CrO 相互转化的影响 相互转化的影响 |
|
|
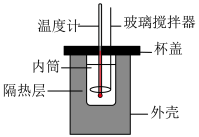
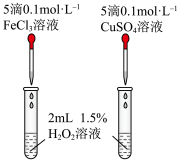
| iii.测定稀盐酸与NaOH溶液中和的反应热 | iv.比较Fe3+与Cu2+对H2O2分解反应的催化效果 |
A.图i反应的离子方程式为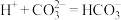 |
B.图ii证明增大 有利于增大 有利于增大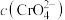 ,减小 ,减小 |
| C.图iii中去隔热层不保温,测得的反应热偏小 |
D.图iv中将 溶液换为 溶液换为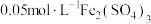 溶液更为合理 溶液更为合理 |
您最近一年使用:0次
名校
解题方法
6 . 硫酸渣是硫酸生产过程中产生的固体废料,主要化学成分有 、
、 、
、 等。
等。
I.研究人员可利用硫酸渣制备高纯度硫酸亚铁晶体,流程如下图所示:
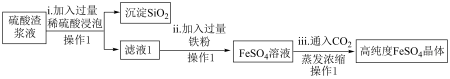
已知: 是难溶于水的酸性氧化物。
是难溶于水的酸性氧化物。
(1)操作1是______ 。
(2)步骤ii中涉及反应的离子方程式有_______ 、_________ 。
(3)步骤iii中的 的作用是
的作用是______ 。
(4)取少量高纯度 晶体配成溶液,
晶体配成溶液,_______ (操作和现象),证明该晶体中不含 。
。
Ⅱ.研究人员还可利用硫酸渣与含氯废气( 和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
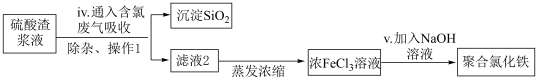
已知:聚合氯化铁的一种形式为 。
。
(5)写出以下物质中加点元素 的化合价: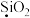
_____ ,
_____ 。
(6)下列关于步骤iv中含氯废气作用的说法中,不正确的是___________ 。
a.盐酸中 作用是使FeO、
作用是使FeO、 溶解
溶解
b.氯气参与反应的离子方程式为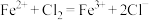
c.盐酸与氯气中的氯元素均转移到 中
中
(7)补全步骤v中涉及到反应的化学方程式______ 。
 。
。
 、
、 、
、 等。
等。I.研究人员可利用硫酸渣制备高纯度硫酸亚铁晶体,流程如下图所示:

已知:
 是难溶于水的酸性氧化物。
是难溶于水的酸性氧化物。(1)操作1是
(2)步骤ii中涉及反应的离子方程式有
(3)步骤iii中的
 的作用是
的作用是(4)取少量高纯度
 晶体配成溶液,
晶体配成溶液, 。
。Ⅱ.研究人员还可利用硫酸渣与含氯废气(
 和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
已知:聚合氯化铁的一种形式为
 。
。(5)写出以下物质中
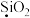

(6)下列关于步骤iv中含氯废气作用的说法中,不正确的是
a.盐酸中
 作用是使FeO、
作用是使FeO、 溶解
溶解b.氯气参与反应的离子方程式为
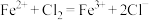
c.盐酸与氯气中的氯元素均转移到
 中
中(7)补全步骤v中涉及到反应的化学方程式
 。
。
您最近一年使用:0次
7 . 短周期主族元素X、Y、Z、W、M、T的原子序数依次增大,X的周期序数等于核外电子总数,Y与Z相邻且Z的最外层电子数是次外层的3倍,Z、W的最外层电子数之和与T的最外层电子数相等,M是地壳中含量最多的金属元素。回答下列问题:
(1)Y的元素符号是___________ ,W在元素周期表中的位置___________ 。
(2)Z、W、M、T的简单离子半径从大到小的顺序为___________ (用离子符号表示)。
(3)X、Z、W可形成多种二元化合物,下列说法不正确的是___________(填字母)。
(4)M的氧化物与W的最高价氧化物对应水化物的溶液反应的离子方程式是___________ 。
(5)由X和Y组成的18电子分子Y2X4,该分子的结构式为___________ 。
(6)不能证明T元素的非金属性比碘元素的非金属性强的事实是___________(填序号)。
(1)Y的元素符号是
(2)Z、W、M、T的简单离子半径从大到小的顺序为
(3)X、Z、W可形成多种二元化合物,下列说法不正确的是___________(填字母)。
| A.X2Z2和W2Z2中都含有非极性共价键 |
| B.X、W可形成离子化合物WX,其电子式为:Na+[:H]- |
| C.W2Z、W2Z2溶于X2Z中时,都发生化合反应 |
| D.W2Z2常用于呼吸面具中作为氧气的来源 |
(5)由X和Y组成的18电子分子Y2X4,该分子的结构式为
(6)不能证明T元素的非金属性比碘元素的非金属性强的事实是___________(填序号)。
| A.T的气态氢化物比碘的气态氢化物稳定 |
| B.T的氧化物对应水化物的酸性强于碘的氧化物对应水化物的酸性 |
| C.T的单质能将碘从其钠盐溶液中置换出来 |
| D.T的单质比碘单质更容易与H2反应 |
您最近一年使用:0次
名校
8 . 对下列图示的说法错误的是
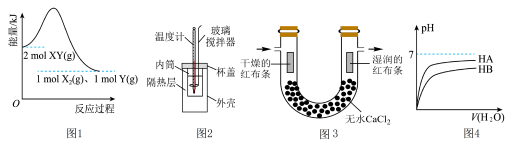

| A.图1中反应物的总键能大于生成物的总键能 |
| B.用图2进行中和热的测定实验时,氢氧化钠一次性快速加入,测定的中和热数值误差更小 |
C.图3中通入干燥的 可验证干燥的氯气是否有漂白性 可验证干燥的氯气是否有漂白性 |
D.由图4可证明图示条件下 |
您最近一年使用:0次
名校
解题方法
9 . 完成下列问题
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
(3)关于新制饱和氯水,下列叙述正确的是_______
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2O
ii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是___________
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)_________
③配平反应i的化学方程式_________ 。
④标出反应ii中电子转移的方向和数目_________ 。
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾___________ 吨。
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
| A.钝化 | B.漂白 | C.固氮 | D.燃烧 |
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
| A.工业合成氨的过程是固氮的过程 |
| B.自然界中,氨是动物体特别是蛋白质腐败后的产物 |
| C.为防止粮食、罐头、水果等食品腐烂,常用氮气作保护气 |
| D.在雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收 |
(3)关于新制饱和氯水,下列叙述正确的是_______
| A.加入适量NaOH,溶液黄绿色褪去,说明氯水中含有Cl2分子 |
| B.加入少量NaCl粉末,溶液漂白性增强 |
| C.加入少量的碳酸钠粉末,pH增大,溶液漂白性一定减弱 |
| D.光照过程中,有气泡冒出,溶液的导电性减弱 |
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
| A.向含足量NaOH的Na2S溶液中加入Na2SO3 |
| B.常温下,向试管中加入1mL浓硫酸和一小块铜片 |
| C.将0.5g硫粉和1.0g铁粉均匀混合,在石棉网上用红热玻璃棒触及粉末一端至粉末红热 |
| D.向Na2SO3固体中加入70%的浓硫酸制备SO2 |
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

| A.O2氧化HBr生成Br2的总反应为:O2+4HBr=2Br2+2H2O |
| B.中间体HOOBr和HOBr中Br的化合价相同 |
| C.发生步骤②时,断裂的化学键既有极性键又有非极性键 |
| D.步骤③中,每生成1molBr2转移2mol电子 |
(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3
 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2Oii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)
③配平反应i的化学方程式
④标出反应ii中电子转移的方向和数目
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾
您最近一年使用:0次
名校
解题方法
10 . 1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中①~⑧代表8种元素。
回答下列问题:
(1)②的元素名称是______ 。
(2)画出⑥的原子结构示意图______ ,写出③与⑦形成的离子化合物的电子式______ 。
(3)③④⑧对应的简单离子半径最小的是______ (用离子符号表示)。
(4)写出⑤的单质与③的最高价氧化物对应水化物反应的离子方程式______ 。
(5)下列说法能证明非金属性⑧强于⑦的是______ (填字母)。
a.简单阴离子的还原性:⑧>⑦ b.简单氢化物的稳定性:⑧>⑦
c.氧化物对应的水化物的酸性:⑧>⑦
(6)由①⑧组成的化合物是______ (填“离子化合物”或“共价化合物”),该化合物的某浓溶液的密度为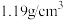 ,溶质质量分数为36.5%,其物质的量浓度为
,溶质质量分数为36.5%,其物质的量浓度为______ mol/L。
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
(1)②的元素名称是
(2)画出⑥的原子结构示意图
(3)③④⑧对应的简单离子半径最小的是
(4)写出⑤的单质与③的最高价氧化物对应水化物反应的离子方程式
(5)下列说法能证明非金属性⑧强于⑦的是
a.简单阴离子的还原性:⑧>⑦ b.简单氢化物的稳定性:⑧>⑦
c.氧化物对应的水化物的酸性:⑧>⑦
(6)由①⑧组成的化合物是
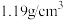 ,溶质质量分数为36.5%,其物质的量浓度为
,溶质质量分数为36.5%,其物质的量浓度为
您最近一年使用:0次
2024-01-22更新
|
109次组卷
|
2卷引用:四川省眉山市2023-2024学年高一上学期期末教学质量检测化学试题