1 . 由废铁屑(含Fe、Fe2O3、Al、Al2O3)制备FeSO4·7H2O,操作流程如图:___________ ,写出试剂a与Al反应的离子方程式___________ 。
(2)溶液C含有的金属阳离子有Fe2+、Fe3+,请设计实验证明存在Fe2+:___________ 。
(3)下列说法不正确 的是___________。
(4)用FeSO4·7H2O配制成FeSO4;溶液后,需加入少量___________ 密封保存。
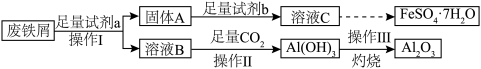
(2)溶液C含有的金属阳离子有Fe2+、Fe3+,请设计实验证明存在Fe2+:
(3)下列说法
| A.试剂b可选择H2SO4或HCl |
| B.溶液B中通入少量CO2出现白色沉淀 |
| C.将FeSO4·7H2O在空气中加热生成FeSO4 |
| D.操作Ⅲ为灼烧,在坩埚中完成 |
(4)用FeSO4·7H2O配制成FeSO4;溶液后,需加入少量
您最近一年使用:0次
2 . 某同学用如图所示装置制备溴苯并验证其反应类型,下列说法错误的是
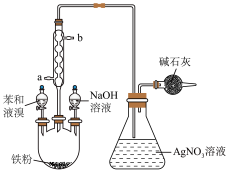
| A.将苯和液溴加入三颈烧瓶后,可观察到瓶内有红棕色气体产生 |
| B.冷凝管中冷凝水的流向为a口进,b口出 |
| C.AgNO3溶液中产生黄色沉淀即可证明该反应为取代反应 |
| D.实验结束后,应先向三颈烧瓶中加入NaOH溶液再拆卸装置 |
您最近一年使用:0次
2024-05-23更新
|
64次组卷
|
3卷引用:河南省周口市西华县第一高级中学2023-2024学年高二下学期期中测试化学试题
名校
3 . 硫酸亚铁铵 是分析化学中的重要试剂。隔绝空气加热至
是分析化学中的重要试剂。隔绝空气加热至 时硫酸亚铁铵能完全分解,分解产物中含有铁的氧化物、硫的氧化物、氨气和水蒸气等。
时硫酸亚铁铵能完全分解,分解产物中含有铁的氧化物、硫的氧化物、氨气和水蒸气等。
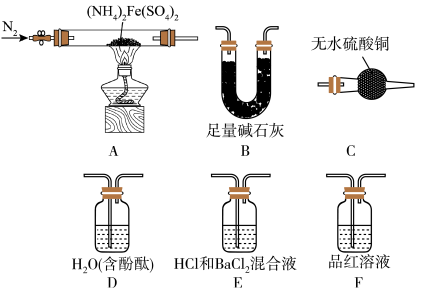
[实验探究]某化学小组选用如图所示部分装置进行实验(夹持装置略)
(2)有关硫酸亚铁铵所含的元素,下列说法正确的是___________。
实验I:探究分解产物中硫的氧化物,连接装置A-E-F-B进行实验。
(3)实验现象:E中没有明显现象,F中溶液褪色,据此得出的结论是___________ 。
实验Ⅱ:验证分解产物中含有氨气和水蒸气、探究残留固体成分。连接A-C-B-D进行实验。
(4)关于氨气和水,下列说法错误的是___________。
(5)装置B在实验Ⅱ中的作用是___________ 。
(6)A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3
,而不含 或
或 :
:___________ 。
(7)实验证明 受热分解除生成上述两个实验中的产物外,还有
受热分解除生成上述两个实验中的产物外,还有 产生,写出A中反应的化学方程式
产生,写出A中反应的化学方程式___________ 。
实验Ⅲ:为测定硫酸亚铁铵 晶体纯度,某同学取m克硫酸亚铁铵晶体样品配成
晶体纯度,某同学取m克硫酸亚铁铵晶体样品配成 溶液,取
溶液,取 硫酸亚铁铵溶液进行如下实验:
硫酸亚铁铵溶液进行如下实验:___________ (用含w、m的式子表示)。
(9)若缺少“洗涤”步骤,最终结果会___________ (填偏大、偏小或不变)。
 是分析化学中的重要试剂。隔绝空气加热至
是分析化学中的重要试剂。隔绝空气加热至 时硫酸亚铁铵能完全分解,分解产物中含有铁的氧化物、硫的氧化物、氨气和水蒸气等。
时硫酸亚铁铵能完全分解,分解产物中含有铁的氧化物、硫的氧化物、氨气和水蒸气等。[实验探究]某化学小组选用如图所示部分装置进行实验(夹持装置略)
| A.溶于水部分电离 | B.固体中只有离子键 |
| C.固体中既含离子键又含共价键 | D.能发生复分解反应或氧化还原反应 |
(2)有关硫酸亚铁铵所含的元素,下列说法正确的是___________。
| A.都位于短周期 | B.只有一个副族元素 |
C.同主族元素非金属性: | D.同周期元素原子半径: |
实验I:探究分解产物中硫的氧化物,连接装置A-E-F-B进行实验。
(3)实验现象:E中没有明显现象,F中溶液褪色,据此得出的结论是
实验Ⅱ:验证分解产物中含有氨气和水蒸气、探究残留固体成分。连接A-C-B-D进行实验。
(4)关于氨气和水,下列说法错误的是___________。
| A.都是弱电解质 | B.都是共价化合物 | C.都是以分子构成物质 | D.氨水中只有两种离子 |
(5)装置B在实验Ⅱ中的作用是
(6)A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3
,而不含
 或
或 :
:(7)实验证明
 受热分解除生成上述两个实验中的产物外,还有
受热分解除生成上述两个实验中的产物外,还有 产生,写出A中反应的化学方程式
产生,写出A中反应的化学方程式实验Ⅲ:为测定硫酸亚铁铵
 晶体纯度,某同学取m克硫酸亚铁铵晶体样品配成
晶体纯度,某同学取m克硫酸亚铁铵晶体样品配成 溶液,取
溶液,取 硫酸亚铁铵溶液进行如下实验:
硫酸亚铁铵溶液进行如下实验:
(9)若缺少“洗涤”步骤,最终结果会
您最近一年使用:0次
解题方法
4 . 利用下图所示的装置( 、
、 、
、 活塞均关闭),既可以验证
活塞均关闭),既可以验证 和
和 的相关性质,又可以形成漂亮的喷泉现象。下列说法错误的是
的相关性质,又可以形成漂亮的喷泉现象。下列说法错误的是
 、
、 、
、 活塞均关闭),既可以验证
活塞均关闭),既可以验证 和
和 的相关性质,又可以形成漂亮的喷泉现象。下列说法错误的是
的相关性质,又可以形成漂亮的喷泉现象。下列说法错误的是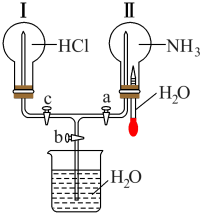
A.该装置可证明 和 和 均易溶于水 均易溶于水 |
| B.该装置不能让Ⅰ、Ⅱ中同时产生喷泉 |
C.打开 、 、 活塞,再挤压胶头滴管,烧瓶Ⅱ中导管口处会产生白烟 活塞,再挤压胶头滴管,烧瓶Ⅱ中导管口处会产生白烟 |
D.向烧杯中滴入几滴酚酞溶液,打开 、 、 活塞,再挤压胶头滴管,Ⅱ中产生“红色喷泉” 活塞,再挤压胶头滴管,Ⅱ中产生“红色喷泉” |
您最近一年使用:0次
名校
5 . 甲烷水蒸气催化重整是制备高纯氢的方法之一。反应如下:
反应ⅰ.
 ;
;
反应ⅱ.
 kJ⋅mol
kJ⋅mol ;
;
反应ⅲ.
 kJ⋅mol
kJ⋅mol 。
。
回答下列问题:
(1)
______ kJ⋅mol 。
。
(2)一定温度下,在一恒容密闭容器中进行反应ⅱ,下列说法可以证明该反应已达到平衡状态的是______ (填标号)。
a.断裂2mol 键时形成4mol
键时形成4mol  键
键
b.容器内气体压强不再改变
c.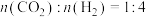
d. 的物质的量分数不再改变
的物质的量分数不再改变
(3)向恒容密闭容器中,按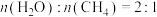 投料,发生上述三个反应。
投料,发生上述三个反应。
①下列措施能提高 平衡转化率的是
平衡转化率的是______ (填标号)。
A.增大 的浓度 B.适当地减小体系压强
的浓度 B.适当地减小体系压强
C.及时分离出 D.选择高效催化剂
D.选择高效催化剂
②其他条件相同时,在不同催化剂(Ⅰ、Ⅱ)作用下,反应相同时间, 的转化率随反应温度的变化如图所示。a点
的转化率随反应温度的变化如图所示。a点______ (填“是”或“不是”)化学平衡状态,温度高于 ℃时,在催化剂Ⅰ作用下,
℃时,在催化剂Ⅰ作用下, 的转化率下降的原因可能是
的转化率下降的原因可能是____________ 。 和
和 .可用来制备甲醇,反应方程式为
.可用来制备甲醇,反应方程式为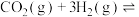
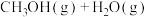
 ,某温度下,将1 mol
,某温度下,将1 mol  和1 mol
和1 mol 充入体积为2 L的恒容密闭容器中,初始总压为8 MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:
充入体积为2 L的恒容密闭容器中,初始总压为8 MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:
①用 表示前3 h的平均反应速率
表示前3 h的平均反应速率
______ mol⋅L ⋅h
⋅h 。
。
②该温度下,该反应的平衡常数
______ (用分数表示)。
③该温度下达到平衡后再向容器中投入0.75mol ,0.25mol
,0.25mol  ,此时
,此时
______ (填“>”“<”或“=”) 。
。
反应ⅰ.

 ;
;反应ⅱ.

 kJ⋅mol
kJ⋅mol ;
;反应ⅲ.

 kJ⋅mol
kJ⋅mol 。
。回答下列问题:
(1)

 。
。(2)一定温度下,在一恒容密闭容器中进行反应ⅱ,下列说法可以证明该反应已达到平衡状态的是
a.断裂2mol
 键时形成4mol
键时形成4mol  键
键b.容器内气体压强不再改变
c.
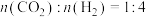
d.
 的物质的量分数不再改变
的物质的量分数不再改变(3)向恒容密闭容器中,按
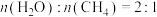 投料,发生上述三个反应。
投料,发生上述三个反应。①下列措施能提高
 平衡转化率的是
平衡转化率的是A.增大
 的浓度 B.适当地减小体系压强
的浓度 B.适当地减小体系压强C.及时分离出
 D.选择高效催化剂
D.选择高效催化剂②其他条件相同时,在不同催化剂(Ⅰ、Ⅱ)作用下,反应相同时间,
 的转化率随反应温度的变化如图所示。a点
的转化率随反应温度的变化如图所示。a点 ℃时,在催化剂Ⅰ作用下,
℃时,在催化剂Ⅰ作用下, 的转化率下降的原因可能是
的转化率下降的原因可能是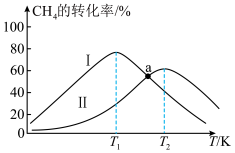
 和
和 .可用来制备甲醇,反应方程式为
.可用来制备甲醇,反应方程式为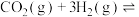
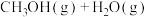
 ,某温度下,将1 mol
,某温度下,将1 mol  和1 mol
和1 mol 充入体积为2 L的恒容密闭容器中,初始总压为8 MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:
充入体积为2 L的恒容密闭容器中,初始总压为8 MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:| 时间/h | 1 | 2 | 3 | 4 | 5 |
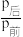 | 0.92 | 0.85 | 0.80 | 0.75 | 0.75 |
 表示前3 h的平均反应速率
表示前3 h的平均反应速率
 ⋅h
⋅h 。
。②该温度下,该反应的平衡常数

③该温度下达到平衡后再向容器中投入0.75mol
 ,0.25mol
,0.25mol  ,此时
,此时
 。
。
您最近一年使用:0次
2024-06-24更新
|
116次组卷
|
2卷引用:山西省临汾市2023-2024学年高二下学期期中考试化学试题
6 . 秸秆是成熟农作物茎叶的总称。农作物光合作用的产物有一半以上存在于秸秆中,秸秆富含氮、磷、钾、钙、镁和有机质。秸秆(含多糖类物质)的综合利用具有重要意义。
(1)下列关于糖类的说法正确的是_______ 。
A.糖类都有甜味,具有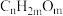 的通式
的通式
B.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
C.用银镜反应不能判断淀粉水解是否完全
D.淀粉和纤维素都属于多糖,是同分异构体
E.糖类是多羟基的醛类化合物
(2)下列关于糖类、油脂、蛋白质的说法中正确的是_______ 。
A.蛋白质、植物油、纤维素、淀粉都属于高分子化合物
B.葡萄糖和果糖都能进一步水解
C.油脂在酸性条件下水解与在碱性条件下水解产物完全相同
D.纤维素在人体消化过程中起着重要作用,但纤维素不能作为人类的营养物质
E.蛋白质在酶的作用下最终水解为氨基酸,氨基酸既具有酸性又具有碱性
(3)下列检验或除杂方法正确的是_______。
(4)我国于2008年起禁止农民焚烧秸秆,焚烧秸秆的危害有_______。
(1)下列关于糖类的说法正确的是
A.糖类都有甜味,具有
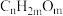 的通式
的通式 B.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
C.用银镜反应不能判断淀粉水解是否完全
D.淀粉和纤维素都属于多糖,是同分异构体
E.糖类是多羟基的醛类化合物
(2)下列关于糖类、油脂、蛋白质的说法中正确的是
A.蛋白质、植物油、纤维素、淀粉都属于高分子化合物
B.葡萄糖和果糖都能进一步水解
C.油脂在酸性条件下水解与在碱性条件下水解产物完全相同
D.纤维素在人体消化过程中起着重要作用,但纤维素不能作为人类的营养物质
E.蛋白质在酶的作用下最终水解为氨基酸,氨基酸既具有酸性又具有碱性
(3)下列检验或除杂方法正确的是_______。
A.向 中加入少量 中加入少量 溶液有淡黄色沉淀生成说明 溶液有淡黄色沉淀生成说明 含有溴原子 含有溴原子 |
B.向淀粉溶液量加入稀硫酸,加热几分钟,冷却后先加入NaOH中和稀硫酸再加入新制 悬浊液,加热,若没有砖红色沉淀生成,说明淀粉没有水解成葡萄糖 悬浊液,加热,若没有砖红色沉淀生成,说明淀粉没有水解成葡萄糖 |
C.欲证明 中含有碳碳双键滴入酸性 中含有碳碳双键滴入酸性 溶液,若紫色褪去,说明其中含有碳碳双键 溶液,若紫色褪去,说明其中含有碳碳双键 |
| D.欲除去苯中混有的苯酚,向混合液中加入浓溴水,充分反应后过滤 |
(4)我国于2008年起禁止农民焚烧秸秆,焚烧秸秆的危害有_______。
| A.温室效应 | B.酸雨 | C.可吸入颗粒物超标 | D.臭氧空洞 |
您最近一年使用:0次
名校
解题方法
7 . 土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下:
 (条件略)
(条件略)
1.写出 的电子式
的电子式___________ 。
2.能证明 是离子化合物的事实是___________。
是离子化合物的事实是___________。
3.下列说法正确的是___________。
4.下列说法中正确的是___________。
 (条件略)
(条件略)1.写出
 的电子式
的电子式2.能证明
 是离子化合物的事实是___________。
是离子化合物的事实是___________。| A.常温下是固体 | B.易溶于水 | C.水溶液能导电 | D.熔融态能导电 |
A. 和 和 溶于水时都会破坏离子键 溶于水时都会破坏离子键 |
B. 能电离出 能电离出 和 和 ,所以 ,所以 是离子化合物 是离子化合物 |
C. 中每个原子的最外层都具有8电子的稳定结构 中每个原子的最外层都具有8电子的稳定结构 |
D. 是共价分子,液氮汽化时破坏共价键和分子间作用力 是共价分子,液氮汽化时破坏共价键和分子间作用力 |
| A.离子化合物中一定只有离子键 | B.共价化合物中一定只有共价键 |
| C.氯化氢溶于水时会破坏离子键 | D.蔗糖溶于水时破坏分子间作用力 |
您最近一年使用:0次
解题方法
8 . 根据分散质粒子的大小,可将分散系分为溶液、胶体、浊液等.胶体的微粒大小使其具有一些特殊性质,在生产生活中广泛存在。
(1)气溶胶是新型冠状病毒传播的重要途径。气溶胶属于胶体的一种,下列关于胶体的说法不正确的是_____ 。
(2)已知土壤胶体粒子带负电,在使用下列化肥时,农作物对氮肥的吸收效果最差的是_____ 。
(3)下列应用或事实与胶体的性质无关的是_____ 。
生活中许多物质能构成胶体分散系,比如将淀粉分散在水中能形成胶体分散系,如图是小李同学设计的提纯淀粉胶体的实验:在半透膜里盛有淀粉胶体和KI溶液混合液体,将半透膜悬挂在盛有蒸馏水的烧杯中,回答下列问题:
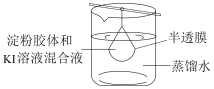
(4)淀粉胶体______ (选填“透过”或“未透过”),试设计简单实验证明你的结论:_____ 。
(5)半透膜的实验原理在我们日常生活中及医疗、工业等领域有广泛应用,试举一例:_____ 。
(1)气溶胶是新型冠状病毒传播的重要途径。气溶胶属于胶体的一种,下列关于胶体的说法不正确的是
| A.胶体是一种分散系,属于混合物 |
| B.胶体分散质粒子直径介于10-9-10-7m之间 |
| C.胶体的本质特征是能发生丁达尔效应 |
| D.利用丁达尔现象是区分胶体和溶液的一种常用方法 |
| A.碳酸氢铵 | B.硝酸钾 | C.氯化铵 | D.硫酸铵 |
| A.用明矾净化饮用水 |
| B.在氯化铁溶液中滴加氯氧化钠溶液出现红褐色沉淀 |
| C.用石膏或盐卤点制豆腐 |
| D.清晨的阳光穿过茂密的林木枝叶所产生的美丽光线 |
生活中许多物质能构成胶体分散系,比如将淀粉分散在水中能形成胶体分散系,如图是小李同学设计的提纯淀粉胶体的实验:在半透膜里盛有淀粉胶体和KI溶液混合液体,将半透膜悬挂在盛有蒸馏水的烧杯中,回答下列问题:

(4)淀粉胶体
(5)半透膜的实验原理在我们日常生活中及医疗、工业等领域有广泛应用,试举一例:
您最近一年使用:0次
名校
9 . 以下说法错误的是
| A.苯的邻二氯代物只有一种证明苯没有单双键交替的结构 |
| B.甲苯使高锰酸钾溶液褪色说明苯环对甲基有影响 |
C.CH3CHBrCH2CH3与 的醇溶液共热反应有机产物有2种(不考虑顺反异构) 的醇溶液共热反应有机产物有2种(不考虑顺反异构) |
| D.甲苯在一定条件下发生硝化反应产物只有TNT一种 |
您最近一年使用:0次
2024-06-20更新
|
341次组卷
|
2卷引用:黑龙江省哈尔滨市第九中学校2023-2024学年高二下学期期中考试化学试卷
名校
10 . 下列说法不正确 的是
| A.向乙醇中加入金属钠,钠浮在乙醇表面剧烈反应 |
B.某烷烃完全燃烧生成17.6g 和9.0g 和9.0g ,则该烃有2种同分异构体 ,则该烃有2种同分异构体 |
C.二氯二氟甲烷( )只有一种结构,可证明甲烷是正四面体结构 )只有一种结构,可证明甲烷是正四面体结构 |
| D.烷烃分子中可能有非极性键,一定有极性键 |
您最近一年使用:0次



