名校
1 . 下列实验操作及现象正确,且与解释或结论存在对应关系是
| 选项 | 实验操作及现象 | 解释或结论 |
| A | 向双氧水中滴加酸性 溶液,迅速有气泡生成 溶液,迅速有气泡生成 |  对 对 分解具有催化作用 分解具有催化作用 |
| B | 向 溶液中滴入足量氯水和 溶液中滴入足量氯水和 ,振荡、静置、分层;再向上层溶液中加入KSCN溶液,下层溶液呈紫红色,上层溶液变为血红色。 ,振荡、静置、分层;再向上层溶液中加入KSCN溶液,下层溶液呈紫红色,上层溶液变为血红色。 | 证明还原性: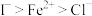 |
| C | 向硫酸酸化的食盐溶液中加入KI溶液和几滴淀粉溶液,溶液未变蓝色 | 该食盐不是含碘盐 |
| D | 向 溶液中滴入稀盐酸,出现白色凝胶 溶液中滴入稀盐酸,出现白色凝胶 | 非金属性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-30更新
|
82次组卷
|
2卷引用:山东省滨州市部分学校2022-2023学年高一下学期5月联考化学试题
解题方法
2 . X、Y、Z、R、Q是元素周期表中原子序数依次增大的前四周期元素。X元素中的一种核素没有中子;基态Y原子核外电子占据了3种能量不同的原子轨道,且成对电子数是未成对电子数的2倍;Z与R同主族,二者核电荷数之比为1∶2;Q元素基态原子最外层只有一个电子,且内层电子全部充满。
请用化学用语回答下列问题:
(1)元素Q的名称为______ ,其基态价电子轨道表示式为______ 。
(2)元素Y、R得电子能力:_______>______(填元素符号)_______ ,请设计一个简易可行的实验方案予以证明______ 。
(3)Z、R分别与X形成18e-分子A、B,写出A的电子式______ ;已知A、B混合有淡黄色物质产生,则该反应的化学方程式为______ 。
(4)D-青霉胺治疗Wilson氏病症的原理是与Q2+生成无毒螯合物M,从而排除体内Q元素。反应如图:

①D-青霉胺中S的孤电子对数为_______ 。
②含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。1molM中通过螯合作用形成的配位键有______ mol。
请用化学用语回答下列问题:
(1)元素Q的名称为
(2)元素Y、R得电子能力:_______>______(填元素符号)
(3)Z、R分别与X形成18e-分子A、B,写出A的电子式
(4)D-青霉胺治疗Wilson氏病症的原理是与Q2+生成无毒螯合物M,从而排除体内Q元素。反应如图:

①D-青霉胺中S的孤电子对数为
②含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。1molM中通过螯合作用形成的配位键有
您最近一年使用:0次
3 . 某研究小组对甲醛的性质进行推测和验证。
Ⅰ.性质推测:
同学甲认为,甲醛的性质应该与乙醛类似,在加热的条件下甲醛可以与新制Cu(OH)2悬浊液反应,且产物是Cu2O和甲酸钠。
(1)写出同学甲所预期的该反应的化学方程式___________ 。
Ⅱ.实验验证:
向3.5 mL新制氢氧化铜碱性悬浊液中加40%福尔马林溶液2mL,加热,有较多无色气
泡逸出。最终试管内所得红色沉淀与乙醛跟氢氧化铜悬浊液反应所得的固体颜色有所不同,试管内壁沉积了一层紫红色的固体物质。
同学甲分别对实验过程中产生的红色沉淀及气体的成分进行探究。
(2)取少量实验中所得的红色沉淀于试管中,加入适量浓氨水,振荡,溶液颜色无明显变化,静置数小时后,溶液颜色略呈浅蓝色,但试管底部红色沉淀的量变化不大。由此判断红色沉淀可能是___________ (写化学式)。用离子方程式解释溶液略呈浅蓝色的原因___________ 。
(3)为进一步验证上述结论,另取少量实验中所得的红色沉淀于试管,加入___________ 。
a.稀硫酸 b.稀硝酸 c.浓硝酸
若观察到___________ 的现象,可证明前面判断正确。
(4)同学甲认为无色气体可能是二氧化碳、甲醛或两者的混合气体。同学乙认为该气体中不可能含有二氧化碳,理由是___________ ,乙同学将产生的无色气体通入银氨溶液,水浴加热,试管壁上很快就有银镜形成。
同学们据此实验现象判断:无色气体的成分是甲醛。
(5)甲乙两同学进一步查阅资料,发现无色气体的主要成分也可能是CO。设计如下实验方案,进一步探究:

实验现象:氧化铜由黑变红、澄清石灰水变浑浊。
方案中水洗的目的是___________ 。
Ⅰ.性质推测:
同学甲认为,甲醛的性质应该与乙醛类似,在加热的条件下甲醛可以与新制Cu(OH)2悬浊液反应,且产物是Cu2O和甲酸钠。
(1)写出同学甲所预期的该反应的化学方程式
Ⅱ.实验验证:
向3.5 mL新制氢氧化铜碱性悬浊液中加40%福尔马林溶液2mL,加热,有较多无色气
泡逸出。最终试管内所得红色沉淀与乙醛跟氢氧化铜悬浊液反应所得的固体颜色有所不同,试管内壁沉积了一层紫红色的固体物质。
| 【资料】 ① 甲醛属于强还原剂,在碱性条件下还原性更强,在空气中能缓慢氧化成甲酸。 ② CO也能还原银氨溶液产生银镜。 ③ Cu2O在酸性溶液中能转化为Cu2+、Cu。 ④ Cu2O能溶于浓氨水形成无色配合物离子[Cu(NH3)2]+,并在空气中立即被氧化为蓝色的[Cu(NH3)4]2+。置于空气中,Cu也能缓慢溶于浓氨水生成蓝色的[Cu(NH3)4]2+。 |
(2)取少量实验中所得的红色沉淀于试管中,加入适量浓氨水,振荡,溶液颜色无明显变化,静置数小时后,溶液颜色略呈浅蓝色,但试管底部红色沉淀的量变化不大。由此判断红色沉淀可能是
(3)为进一步验证上述结论,另取少量实验中所得的红色沉淀于试管,加入
a.稀硫酸 b.稀硝酸 c.浓硝酸
若观察到
(4)同学甲认为无色气体可能是二氧化碳、甲醛或两者的混合气体。同学乙认为该气体中不可能含有二氧化碳,理由是
同学们据此实验现象判断:无色气体的成分是甲醛。
(5)甲乙两同学进一步查阅资料,发现无色气体的主要成分也可能是CO。设计如下实验方案,进一步探究:

实验现象:氧化铜由黑变红、澄清石灰水变浑浊。
方案中水洗的目的是
您最近一年使用:0次
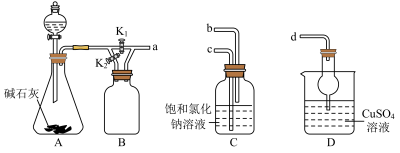
4 . 利用如图装置进行 的制备及性质探究实验。下列说法正确的是
的制备及性质探究实验。下列说法正确的是
 的制备及性质探究实验。下列说法正确的是
的制备及性质探究实验。下列说法正确的是
A.使用A装置制备 时,分液漏斗中应盛放浓氨水,利用了氨水的碱性弱于NaOH 时,分液漏斗中应盛放浓氨水,利用了氨水的碱性弱于NaOH |
B.装置B中盛放湿润蓝色石蕊试纸,打开 ,关闭 ,关闭 ,可证明 ,可证明 为碱性气体 为碱性气体 |
| C.利用C装置模拟候氏制碱法时,可将a和c连接 |
D.将a和d连接验证 与 与 的配位能力强于 的配位能力强于 |
您最近一年使用:0次
2023-04-29更新
|
495次组卷
|
3卷引用:河北省部分学校2023届高三下学期大数据应用调研联合测评化学试题
河北省部分学校2023届高三下学期大数据应用调研联合测评化学试题河北省石家庄部分重点高中2022-2023学年高三下学期4月期中化学试题(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
5 . 为探究影响化学反应速率的因素与化学反应限度的存在,某中学实验小组进行以下两组实验。
(Ⅰ)探究影响化学反应速率的因素,结合表中信息,回答问题:
(1)探究温度对反应速率的影响,应选择的实验组号是_______ ;实验组①②对比的实验目的是_______ 。
(2)实验过程中,需要观察和记录_______ ,比较化学反应速率的快慢。
(3)上述四组实验中,反应速率最慢的是_______ 。
(Ⅱ)验证铁离子与碘离子反应存在限度,结合相关实验,回答问题:
药品选择: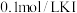 溶液、
溶液、 溶液、淀粉溶液、试剂N
溶液、淀粉溶液、试剂N
实验步骤:①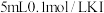 溶液中滴入5~6滴
溶液中滴入5~6滴 溶液,充分反应后,将所得溶液分成甲、乙两等份;
溶液,充分反应后,将所得溶液分成甲、乙两等份;
②向甲中滴加2滴淀粉,充分振荡;
③向乙中滴加试剂N。回答下列问题:
(4)步骤②甲试管中出现_______ 现象,证明反应有 的生成。
的生成。
(5)若实验①中的反应存在限度,可用试剂N的溶液检验 ,则试剂N是
,则试剂N是_______ ;乙试管中的现象是_______ 。
(6)写出实验步骤①的化学方程式_______ 。
(Ⅰ)探究影响化学反应速率的因素,结合表中信息,回答问题:
| 组号 | 反应温度/℃ | 参加反应的物质 | ||||
 |  |  | ||||
 | 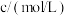 |  | 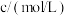 |  | ||
| ① | 10 | 2 | 0.1 | 2 | 0.1 | 2 |
| ② | 10 | 2 | 0.1 | 2 | 0.1 | 4 |
| ③ | 30 | 2 | 0.1 | 2 | 0.1 | 4 |
| ④ | 30 | 2 | 0.2 | 2 | 0.2 | 4 |
(2)实验过程中,需要观察和记录
(3)上述四组实验中,反应速率最慢的是
(Ⅱ)验证铁离子与碘离子反应存在限度,结合相关实验,回答问题:
药品选择:
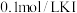 溶液、
溶液、 溶液、淀粉溶液、试剂N
溶液、淀粉溶液、试剂N实验步骤:①
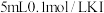 溶液中滴入5~6滴
溶液中滴入5~6滴 溶液,充分反应后,将所得溶液分成甲、乙两等份;
溶液,充分反应后,将所得溶液分成甲、乙两等份;②向甲中滴加2滴淀粉,充分振荡;
③向乙中滴加试剂N。回答下列问题:
(4)步骤②甲试管中出现
 的生成。
的生成。(5)若实验①中的反应存在限度,可用试剂N的溶液检验
 ,则试剂N是
,则试剂N是(6)写出实验步骤①的化学方程式
您最近一年使用:0次
名校
解题方法
6 . 下列实验方案能达到目的的是
| 选项 | 实验方案 | 目的 |
| A | 淀粉溶液加入稀硫酸,加热,冷却后滴入碘水,观察溶液颜色变化 | 探究淀粉是否发生水解 |
| B | 向滴有酚酞的 溶液中逐滴加入 溶液中逐滴加入 溶液,观察溶液颜色的变化 溶液,观察溶液颜色的变化 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| C | 分别取50mL 硫酸、50mL 硫酸、50mL 氢氧化钡,两溶液在量热器中充分反应,测定反应前后最大温度差 氢氧化钡,两溶液在量热器中充分反应,测定反应前后最大温度差 | 测定中和热 |
| D | 向5mL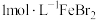 溶液中加入1mL 溶液中加入1mL 氯水,振荡,再加 氯水,振荡,再加 萃取,观察 萃取,观察 层颜色变化 层颜色变化 | 证明 的还原性强于 的还原性强于 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-28更新
|
220次组卷
|
2卷引用:山东省济宁市2023届高三下学期三模化学试题
名校
7 . 下列有关实验的描述正确的是
A.实验室制备 的实验中,可在液面上方加入适量植物油,以便隔绝空气 的实验中,可在液面上方加入适量植物油,以便隔绝空气 |
| B.向铜和浓硫酸反应后的混合物中加水,若溶液呈蓝色,则证明有硫酸铜生成 |
| C.未打磨过的铝片投入NaOH溶液中,因表面有氧化膜,即便长时间放置也不能产生氢气 |
| D.容量瓶在洗净后,若瓶底有少量水残留则必须烘干,否则所配溶液浓度偏低 |
您最近一年使用:0次
解题方法
8 . 高纯氧化铁(Fe2O3)是制造软磁铁氧体主要原料,而后者广泛应用于电工电信设备。以窑尾灰为原料制造高纯氧化铁工艺流程图如下(已知窑尾灰的主要成分为Fe、C、FeO、Fe2O3、CaO、Al2O3、MgO、SiO2)

据此回答下列问题:
(1)滤渣1的主要成分为_______ ;证明滤液1中含有Fe2+的试剂可以是_______ 。
(2)“还原”过程加铁粉的目的是_______ 。
(3)若滤液2中c(Fe2+)=2mol·L-1则“调pH”范围是_______ (lg2≈0.3)。
(4)若滤渣3中既有CaF2又有MgF2,则滤液4中 =
=_______ (化为最简整数比)。
(5)写出“沉淀”过程中的离子反应方程式:_______ 。
(6)“灼烧”过程中的化学方程式为:_______ 。

| 当c(Mn+)≤10-5mol·L-1时,认定沉淀完全;25℃时,各物质的溶度积常数如下: | ||||||
| 物质 | CaSO4 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | CaF2 | MgF2 |
| Ksp | 9.0×10-6 | 8.0×10-16 | 4.0×10-38 | 1.0×10-30.5 | 5.0×10-9 | 7.5×10-11 |
(1)滤渣1的主要成分为
(2)“还原”过程加铁粉的目的是
(3)若滤液2中c(Fe2+)=2mol·L-1则“调pH”范围是
(4)若滤渣3中既有CaF2又有MgF2,则滤液4中
 =
=(5)写出“沉淀”过程中的离子反应方程式:
(6)“灼烧”过程中的化学方程式为:
您最近一年使用:0次
9 . 为研究二氧化硫的性质,某兴趣小组设计如下装置进行实验。

(1)a是___________ (填仪器名称)。
(2)在组装好装置装入药品前,需要进行的操作是___________ 。
(3)将少量 溶液缓慢推入
溶液缓慢推入 粉末处,发生反应。
粉末处,发生反应。
① 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
②随着反应的进行,c处实验现象为___________ ,b处实验现象为___________ 。
③几分钟后,发现d处气球变小,逐渐恢复至原样,说明二氧化硫具有的性质是___________ 。
④为证明二氧化硫与水反应具有可逆性,需要进行的实验操作是___________ 。
(4)这种实验设计的优点之一是___________ 。

(1)a是
(2)在组装好装置装入药品前,需要进行的操作是
(3)将少量
 溶液缓慢推入
溶液缓慢推入 粉末处,发生反应。
粉末处,发生反应。①
 与
与 反应的化学方程式为
反应的化学方程式为②随着反应的进行,c处实验现象为
③几分钟后,发现d处气球变小,逐渐恢复至原样,说明二氧化硫具有的性质是
④为证明二氧化硫与水反应具有可逆性,需要进行的实验操作是
(4)这种实验设计的优点之一是
您最近一年使用:0次
名校
解题方法
10 . 下列实验操作能达到实验目的的是
| 实验操作 | 实验目的 | |
| A | 将充满 的试管倒扣在水槽中,试管内液面高于水槽 的试管倒扣在水槽中,试管内液面高于水槽 | 证明 与水发生反应 与水发生反应 |
| B | 向 、KI的混合溶液中加入少量溴水和 、KI的混合溶液中加入少量溴水和 ,振荡 ,振荡 | 比较还原性: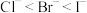 |
| C | 用pH计分别测量 盐酸和 盐酸和 醋酸的pH 醋酸的pH | 验证 为弱酸 为弱酸 |
| D | 向含琼脂和食盐水的混合物中滴加酚酞、 溶液,混合均匀后再放入裹有锌皮的铁钉 溶液,混合均匀后再放入裹有锌皮的铁钉 | 验证锌对铁的保护 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



