17. 邻硝基苯甲醛是一种重要的精细化学品,实验室可通过图1装置(夹持仪器已略去),以邻硝基苄醇为原料,利用两相反应体系(图2)实现邻硝基苯甲醛的选择性氧化合成。已知部分物质的性质如表所示。
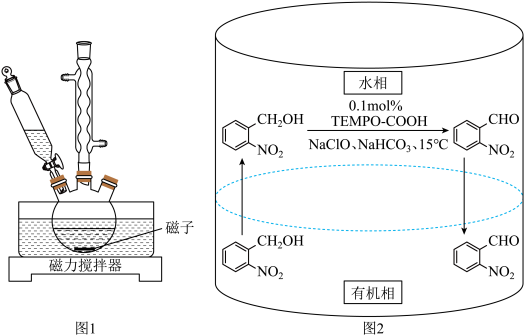
实验步骤如下:
Ⅰ.向三颈瓶中依次加入1.53g邻硝基苄醇(摩尔质量153g/mol),10.0mL二氯甲烷(沸点39.8℃)和磁子,搅拌使固体全部溶解。再依次加入1.0mLTEMPO-COOH水溶液(做催化剂)和13.0mL饱和NaHCO
3溶液。在15℃和剧烈搅拌条件下,滴加13.0mL(足量)10%NaClO水溶液后,继续反应40min。
Ⅱ.反应完全后,将反应液倒入分液漏斗,分出有机层后,水相用10.0mL二氯甲烷萃取,合并有机相,经无水硫酸钠干燥、过滤后,除去并回收滤液中的二氯甲烷,得到粗品。
Ⅲ.将粗品溶解在20.0mL二氯甲烷中,加入10.0mL饱和NaHSO
3溶液,充分作用后,分离得到水层,水层在水浴中用5%氢氧化钠溶液调节pH到10,浅黄色固体析出完全。抽滤、干燥至恒重,得1.21g产品。
(1)图1中仪器a的名称是
___________;控制反应温度为15℃的方法是
___________;滴加NaClO溶液时,需要先将漏斗上端玻璃塞打开,目的是
___________。
(2)上述利用选择性氧化合成邻硝基苯甲醛的化学方程式为
___________。
(3)配制饱和NaHCO
3溶液时,必须使用的仪器是(填写仪器名称)
___________。
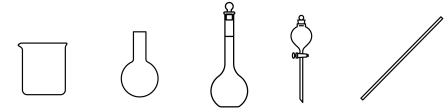
(4)相比于单相反应体系,利用两相反应体系可以大幅减少副产物的量,原因是
___________;该副产物主要成分是
___________(填结构简式)。
(5)步骤Ⅱ中除去并回收二氯甲烷的实验方法是
___________。
(6)若用一定浓度盐酸代替“步骤Ⅲ”中的5%氢氧化钠溶液调节pH,
___________(填“能”或“不能”)析出大量产品,原因是
___________。
(7)本实验产率为
___________%(计算结果保留3位有效数字)。