1 . 以镍废料(主要成分为镍铁合金,含少量铜)为原料,生产NiO的部分工艺流程如下:

“沉镍”得到的是碱式碳酸镍[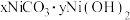 ],下列有关说法不正确的是
],下列有关说法不正确的是

“沉镍”得到的是碱式碳酸镍[
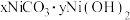 ],下列有关说法不正确的是
],下列有关说法不正确的是A.“酸溶”时,控制温度不超过80℃,有利于提高 的利用率 的利用率 |
B.“氧化”后,溶液中主要存在的阳离子有: 、 、 、 、 、 、 |
C.“除铜”时, 参加反应的离子方程式为: 参加反应的离子方程式为: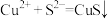 |
| D.“沉镍”时,若溶液pH增大,碱式碳酸镍中镍元素含量会增大 |
您最近一年使用:0次
2021-06-27更新
|
299次组卷
|
2卷引用:江苏省无锡市2020-2021学年期高二下学期期终教学质量抽测建议卷化学试题
解题方法
2 . 铜及其化合物在工业生产中有着广泛的用途。
(1)某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu(NO3)2的部分工艺流程如图所示:
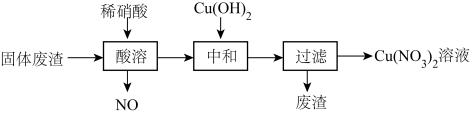
①分别写出CuO、Cu2O与稀硝酸反应的离子方程式为___________ 、___________ 。
②酸溶时,反应温度不宜超过70℃,其主要原因是___________ 。
③过滤后所得废渣的主要成分的化学式为___________ 。
④Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为___________ ,由Cu(NO3)2溶液制Cu(NO3)2晶体的操作方法是:蒸发浓缩、___________ 、过滤、冰水洗涤、___________ 。
(2)印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时用 溶液作为“腐蚀液”,得到反应后的溶液A。
溶液作为“腐蚀液”,得到反应后的溶液A。
①为了回收利用使用过的腐蚀液,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是___________ (请将答案填涂在答题卷相应位置)。
A.氯气B.铁C.双氧水D.稀硫酸
写出其中上述一种试剂将 转化为
转化为 的离子方程式:
的离子方程式:___________ 。
②为了回收金属铜和得到较纯净的 溶液,请补充完整下列实验步骤:在溶液A中加入过量的铁粉,过滤,得到滤渣B和滤液C,将滤渣B
溶液,请补充完整下列实验步骤:在溶液A中加入过量的铁粉,过滤,得到滤渣B和滤液C,将滤渣B___________ ,得到金属铜;将处理滤渣B时得到的滤液和滤液C合并,得到 溶液。
溶液。
(1)某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu(NO3)2的部分工艺流程如图所示:

①分别写出CuO、Cu2O与稀硝酸反应的离子方程式为
②酸溶时,反应温度不宜超过70℃,其主要原因是
③过滤后所得废渣的主要成分的化学式为
④Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为
(2)印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时用
 溶液作为“腐蚀液”,得到反应后的溶液A。
溶液作为“腐蚀液”,得到反应后的溶液A。①为了回收利用使用过的腐蚀液,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是
A.氯气B.铁C.双氧水D.稀硫酸
写出其中上述一种试剂将
 转化为
转化为 的离子方程式:
的离子方程式:②为了回收金属铜和得到较纯净的
 溶液,请补充完整下列实验步骤:在溶液A中加入过量的铁粉,过滤,得到滤渣B和滤液C,将滤渣B
溶液,请补充完整下列实验步骤:在溶液A中加入过量的铁粉,过滤,得到滤渣B和滤液C,将滤渣B 溶液。
溶液。
您最近一年使用:0次



