名校
解题方法
1 . 某学习小组想通过研究NO2性质,提出减少汽车尾气NO2含量的同时,降低汽车排气管中积碳的实验方案。回答下列问题:
(1)通过浓硝酸分解分析NO2能否支持燃烧:如图所示,向试管中加入浓硝酸,加热至沸腾,向试管中伸入燃烧的木条,木条熄灭。

①写出浓硝酸受热分解的化学方程式:_____ 。
②甲同学根据实验现象得出NO2不支持燃烧,不能与红热的碳反应的结论,乙同学不同意该结论,理由可能是_____ 。
③除了原理上的不合理,从环保角度考虑,该实验还有一个明显不足之处是_____ 。
(2)查阅资料发现Cu(NO3)2受热时发生反应:2Cu(NO3)2 2CuO+4NO2↑+O2↑。收集硝酸铜分解后的气体,发现该气体能使带火星的木条复燃,但空气(空气中O2的体积分数约为
2CuO+4NO2↑+O2↑。收集硝酸铜分解后的气体,发现该气体能使带火星的木条复燃,但空气(空气中O2的体积分数约为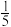 )不能使带火星的木条复燃。
)不能使带火星的木条复燃。
①结论:NO2能与碳反应,支持燃烧,理由是_____ 。
②经检验,加热时碳与NO2反应的两种产物均为空气成分,写出该反应的化学方程式:______ 。
(3)设计NO2与碳反应的条件控制实验:初始温度为280℃(汽车尾气的大致温度),其它初始条件也完全相同,分别在体积相同的绝热恒容密闭容器A和恒温恒容密闭容器B中加入等量的焦炭和NO2气体。
①反应达到平衡时,平衡转化率较高的是容器_____ (填“A”或“B”)。
②请写出工农业生产中NO2的一种用途:_____ 。
(1)通过浓硝酸分解分析NO2能否支持燃烧:如图所示,向试管中加入浓硝酸,加热至沸腾,向试管中伸入燃烧的木条,木条熄灭。

①写出浓硝酸受热分解的化学方程式:
②甲同学根据实验现象得出NO2不支持燃烧,不能与红热的碳反应的结论,乙同学不同意该结论,理由可能是
③除了原理上的不合理,从环保角度考虑,该实验还有一个明显不足之处是
(2)查阅资料发现Cu(NO3)2受热时发生反应:2Cu(NO3)2
 2CuO+4NO2↑+O2↑。收集硝酸铜分解后的气体,发现该气体能使带火星的木条复燃,但空气(空气中O2的体积分数约为
2CuO+4NO2↑+O2↑。收集硝酸铜分解后的气体,发现该气体能使带火星的木条复燃,但空气(空气中O2的体积分数约为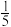 )不能使带火星的木条复燃。
)不能使带火星的木条复燃。①结论:NO2能与碳反应,支持燃烧,理由是
②经检验,加热时碳与NO2反应的两种产物均为空气成分,写出该反应的化学方程式:
(3)设计NO2与碳反应的条件控制实验:初始温度为280℃(汽车尾气的大致温度),其它初始条件也完全相同,分别在体积相同的绝热恒容密闭容器A和恒温恒容密闭容器B中加入等量的焦炭和NO2气体。
①反应达到平衡时,平衡转化率较高的是容器
②请写出工农业生产中NO2的一种用途:
您最近一年使用:0次
2022-12-17更新
|
109次组卷
|
2卷引用:广东部分名校2022-2023学年高二上学期12月联考化学试题
解题方法
2 . 铜及其化合物在工业生产中有着广泛的用途。
(1)某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu(NO3)2的部分工艺流程如图所示:
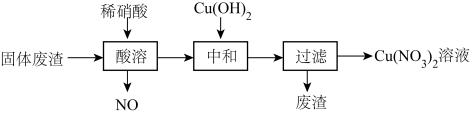
①分别写出CuO、Cu2O与稀硝酸反应的离子方程式为___________ 、___________ 。
②酸溶时,反应温度不宜超过70℃,其主要原因是___________ 。
③过滤后所得废渣的主要成分的化学式为___________ 。
④Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为___________ ,由Cu(NO3)2溶液制Cu(NO3)2晶体的操作方法是:蒸发浓缩、___________ 、过滤、冰水洗涤、___________ 。
(2)印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时用 溶液作为“腐蚀液”,得到反应后的溶液A。
溶液作为“腐蚀液”,得到反应后的溶液A。
①为了回收利用使用过的腐蚀液,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是___________ (请将答案填涂在答题卷相应位置)。
A.氯气B.铁C.双氧水D.稀硫酸
写出其中上述一种试剂将 转化为
转化为 的离子方程式:
的离子方程式:___________ 。
②为了回收金属铜和得到较纯净的 溶液,请补充完整下列实验步骤:在溶液A中加入过量的铁粉,过滤,得到滤渣B和滤液C,将滤渣B
溶液,请补充完整下列实验步骤:在溶液A中加入过量的铁粉,过滤,得到滤渣B和滤液C,将滤渣B___________ ,得到金属铜;将处理滤渣B时得到的滤液和滤液C合并,得到 溶液。
溶液。
(1)某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu(NO3)2的部分工艺流程如图所示:

①分别写出CuO、Cu2O与稀硝酸反应的离子方程式为
②酸溶时,反应温度不宜超过70℃,其主要原因是
③过滤后所得废渣的主要成分的化学式为
④Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为
(2)印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时用
 溶液作为“腐蚀液”,得到反应后的溶液A。
溶液作为“腐蚀液”,得到反应后的溶液A。①为了回收利用使用过的腐蚀液,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是
A.氯气B.铁C.双氧水D.稀硫酸
写出其中上述一种试剂将
 转化为
转化为 的离子方程式:
的离子方程式:②为了回收金属铜和得到较纯净的
 溶液,请补充完整下列实验步骤:在溶液A中加入过量的铁粉,过滤,得到滤渣B和滤液C,将滤渣B
溶液,请补充完整下列实验步骤:在溶液A中加入过量的铁粉,过滤,得到滤渣B和滤液C,将滤渣B 溶液。
溶液。
您最近一年使用:0次



