1 . 下列说法正确的是
| A.铵盐都能与碱反应,不能与酸反应 |
| B.铵盐受热分解一定都会产生NH3 |
C.NH4Cl溶液中加入NaOH浓溶液共热时反应的离子方程式为 +OH- =NH3↑+H2O +OH- =NH3↑+H2O |
| D.可以用NaOH溶液鉴别Na2SO4、NH4NO3、KCl、(NH4)2SO4四种溶液 |
您最近一年使用:0次
名校
解题方法
2 . 溶液中可能含有H+、 、Mg2+、Al3+、Fe3+、
、Mg2+、Al3+、Fe3+、 、
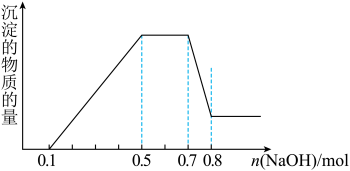
、 中的几种。①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是
中的几种。①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是
 、Mg2+、Al3+、Fe3+、
、Mg2+、Al3+、Fe3+、 、
、 中的几种。①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是
中的几种。①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是
A.溶液中一定不含 ,可能含有 ,可能含有 |
B.在滴加NaOH物质的量为0.7-0.8 mol时,发生离子反应为Al3++4OH-= +2H2O +2H2O |
| C.溶液中的阳离子只有H+、Mg2+、Al3+ |
D.n(H+):n( ):n(A13+)=1:2:1 ):n(A13+)=1:2:1 |
您最近一年使用:0次
2022-11-19更新
|
994次组卷
|
4卷引用:湖北省武汉市第一中学2022-2023学年高一上学期12月阶段性测试化学试题
名校
解题方法
3 . 下列指定反应的离子方程式书写正确的是
A.用氨水吸收少量SO2:2NH3•H2O+SO2=2NH +SO +SO +H2O +H2O |
B.向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO +OH-=CaCO3↓+H2O +OH-=CaCO3↓+H2O |
| C.向次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
| D.向酸性FeI2溶液中滴入少量H2O2稀溶液:2Fe2++H2O2+2H+=2Fe3++2H2O |
您最近一年使用:0次
名校
解题方法
4 . 对于铵盐的描述都正确的是( )
①都溶于水 ②都是白色晶体 ③都有刺激性气味 ④加热后都有氨气放出 ⑤与碱混合后加热都有氨气放出 ⑥都能使湿润的红色石蕊试纸变蓝
①都溶于水 ②都是白色晶体 ③都有刺激性气味 ④加热后都有氨气放出 ⑤与碱混合后加热都有氨气放出 ⑥都能使湿润的红色石蕊试纸变蓝
| A.全部 |
| B.①②⑤⑥ |
| C.①②⑤ |
| D.③④⑤ |
您最近一年使用:0次
2020-01-29更新
|
298次组卷
|
10卷引用:湖北省武汉市外国语学校2019-2020学年高一下学期期中考试化学试题
湖北省武汉市外国语学校2019-2020学年高一下学期期中考试化学试题云南省勐腊县一中2019-2020学年高二上学期开学考试化学试题云南省永德县第一中学2019-2020学年高一12月月考化学试题鲁科版高中化学必修1第三章《自然界中的元素》测试卷苏教版高中化学必修1专题四《硫、氮和可持续发展》测试卷贵州省安龙县第三中学2019-2020学年高一上学期期末考试化学试题河北省石家庄精英中学高一下学期第二次调研考试化学试题云南省玉溪市新平一中2020-2021学年高二上学期开学考试化学试题(已下线)练习16 生活中的含氮化合物-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)青海省西宁市海湖中学2020-2021学年高一下学期开学考试化学试题
解题方法
5 . 向一定量MgCl2、AlCl3溶液中滴加常用试剂NaOH与盐酸(t时刻之前滴加的试剂a,t时刻之后改滴试剂b),沉淀的物质的量y (mol)与试剂体积x (mL)间的关系曲线如图所示。试回答:
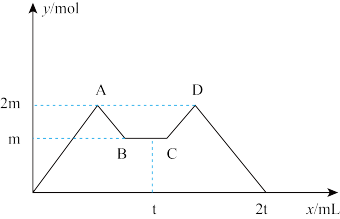
(1)AB段所表示的反应的离子方程式是________________________________________________ ;
CD段所表示的反应的离子方程式是_____________________________________ 。
(2)若向B处生成的溶液中通入足量二氧化碳气体,反应的离子方程式是________________________ 。
(3)a是______________ ,且c(a)∶c(b)=_______________
(4)原混合液中,c(Al3+)∶c(Mg2+)∶c(Cl-)=_____________________
(5)纳米氧化铝在陶瓷材料、电子工业、生物医药等方面有广阔的应用前景,它可通过硫酸铝铵晶体热分解得到。取4.53 g硫酸铝铵晶体【Al2(NH4)2(SO4)n·24H2O,相对分子质量为906】加热分解,最终剩余0.51 gAl2O3固体。加热过程中,固体质量随时间的变化如下图所示。
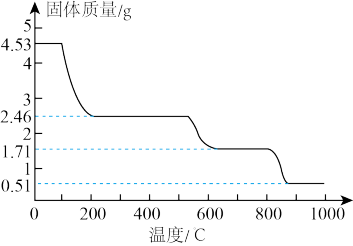
试通过计算确定400℃剩余固体成分的化学式_____________________________ 。(写出计算过程)

(1)AB段所表示的反应的离子方程式是
CD段所表示的反应的离子方程式是
(2)若向B处生成的溶液中通入足量二氧化碳气体,反应的离子方程式是
(3)a是
(4)原混合液中,c(Al3+)∶c(Mg2+)∶c(Cl-)=
(5)纳米氧化铝在陶瓷材料、电子工业、生物医药等方面有广阔的应用前景,它可通过硫酸铝铵晶体热分解得到。取4.53 g硫酸铝铵晶体【Al2(NH4)2(SO4)n·24H2O,相对分子质量为906】加热分解,最终剩余0.51 gAl2O3固体。加热过程中,固体质量随时间的变化如下图所示。

试通过计算确定400℃剩余固体成分的化学式
您最近一年使用:0次



