解题方法
1 . 已知钠放置于空气中可发生如下变化:
Na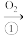 Na2O
Na2O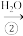 NaOH
NaOH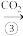 Na2CO3·10H2O→Na2CO3
Na2CO3·10H2O→Na2CO3
根据此变化回答以下问题。
(1)请写出①②步转化的化学方程式。
①_______
②_______
(2)已知钠在空气中燃烧可生成一种淡黄色物质,该物质可与CO2、H2O发生反应,根据以上叙述回答:
①该淡黄色物质的化学式为_______ 。
②该淡黄色物质与CO2、H2O反应的化学方程式分别为_______ 、_______ 。
Na
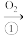 Na2O
Na2O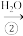 NaOH
NaOH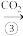 Na2CO3·10H2O→Na2CO3
Na2CO3·10H2O→Na2CO3根据此变化回答以下问题。
(1)请写出①②步转化的化学方程式。
①
②
(2)已知钠在空气中燃烧可生成一种淡黄色物质,该物质可与CO2、H2O发生反应,根据以上叙述回答:
①该淡黄色物质的化学式为
②该淡黄色物质与CO2、H2O反应的化学方程式分别为
您最近一年使用:0次
名校
解题方法
2 . 学习小组利用如下流程制备过氧化钠,并设计实验验证其相关性质。

回答下列问题:
(1)流程中由Na2O生成淡黄色固体的化学方程式为_______ 。
(2)小组同学取一定量淡黄色固体溶于冷水中。待固体全部反应后,仍可缓慢释放氧气,为探究固体溶解后溶液成分,设计如下实验方案进行验证:

①甲中产生较多气泡,证明固体溶解后溶液中有_______ (填化学式),写出甲中发生反应的化学方程式_______ 。
②向乙中滴入酚酞,溶液变红的原因是_______ (用物质的电离方程式回答)。
(3)小组同学将金属钠加热至熔化后,误通入了干燥的CO2进行反应,将反应后固体产物溶于稀盐酸,产生气泡,观察到难溶于水的黑色固体。
①产物中与盐酸反应的物质可能为_______ (填化学式)。
②经检验,黑色固体为单质碳。写出CO2与Na反应的化学方程式_______ 。

回答下列问题:
(1)流程中由Na2O生成淡黄色固体的化学方程式为
(2)小组同学取一定量淡黄色固体溶于冷水中。待固体全部反应后,仍可缓慢释放氧气,为探究固体溶解后溶液成分,设计如下实验方案进行验证:

①甲中产生较多气泡,证明固体溶解后溶液中有
②向乙中滴入酚酞,溶液变红的原因是
(3)小组同学将金属钠加热至熔化后,误通入了干燥的CO2进行反应,将反应后固体产物溶于稀盐酸,产生气泡,观察到难溶于水的黑色固体。
①产物中与盐酸反应的物质可能为
②经检验,黑色固体为单质碳。写出CO2与Na反应的化学方程式
您最近一年使用:0次
解题方法
3 . 金属钠是一种性质活泼的银白色金属,学习小组观察到金属钠在表面皿上发生的一系列变化为:银白色断面→断面变暗→断面变白色→出现小液滴伴有气泡→白色固体→白色粉末
回答下列问题:
(1)实验室少量的钠保存在___________ 中。
(2)“断面变暗”发生反应的化学方程式是___________ 。
(3)“出现小液滴”的过程属于___________ (填“物理变化”或“化学变化”),“伴有气泡”反应的离子方程式为___________ 。
(4)最终白色粉末为___________ (填化学式),该物质溶于水的电离方程式为___________ 。
回答下列问题:
(1)实验室少量的钠保存在
(2)“断面变暗”发生反应的化学方程式是
(3)“出现小液滴”的过程属于
(4)最终白色粉末为
您最近一年使用:0次
名校
解题方法
4 . 钠是很活泼的金属,在空气中燃烧的产物是Na2O2。Na2O的制取可以通过如下反应完成:
Na+NaNO3⟶Na2O+N2↑(未配平)。请回答下列问题:
(1)钠在空气中燃烧的反应方程式:_____________________ 。
(2)在上述反应中,N2有何作用?____________________________ 。
(3)制取Na2O时由于设备密封性不好而进入了少量空气,导致制得的Na2O产品中含有Na2O2杂质。某学生设计了实验来测定该样品中Na2O的质量分数,实验数据如下:24.8 g Na2O在氧气中充分灼烧后所得固体质量为28.0 g,该样品中Na2O的质量分数为____ 。
Na+NaNO3⟶Na2O+N2↑(未配平)。请回答下列问题:
(1)钠在空气中燃烧的反应方程式:
(2)在上述反应中,N2有何作用?
(3)制取Na2O时由于设备密封性不好而进入了少量空气,导致制得的Na2O产品中含有Na2O2杂质。某学生设计了实验来测定该样品中Na2O的质量分数,实验数据如下:24.8 g Na2O在氧气中充分灼烧后所得固体质量为28.0 g,该样品中Na2O的质量分数为
您最近一年使用:0次
名校
5 . (1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:

①漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式:_____________________________ ;______________ 。
②某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448 mL气体,则该漂白粉中所含有效成分的质量为___________ (假设漂白粉中的其它成分不与硝酸反应)。
(2)将14 g Na2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12 L,所得溶液的体积为400 mL。试计算:原混合物中Na2O的质量为___________ g,所得溶液中Na+的物质的量为___________ 。

①漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式:
②某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448 mL气体,则该漂白粉中所含有效成分的质量为
(2)将14 g Na2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12 L,所得溶液的体积为400 mL。试计算:原混合物中Na2O的质量为
您最近一年使用:0次



