1 . 浓硫酸是中学中常见的一种化学试剂,某学校实验小组为探究浓硫酸与金属的反应并检验生成的气体设计了相关实验。

(1)常温下,将铝片插入浓H2SO4中未发现有明显的变化,其原因为_______ 。
(2)在加热的条件下,浓H2SO4可将铜氧化,写出该反应的化学方程式:_______ 。
(3)实验中使用可抽动的铜丝,其优点是_______ 。
(4)实验中可观察到B中品红溶液的现象为_______ 。
(5)浸有NaOH溶液的棉团的作用_______

(1)常温下,将铝片插入浓H2SO4中未发现有明显的变化,其原因为
(2)在加热的条件下,浓H2SO4可将铜氧化,写出该反应的化学方程式:
(3)实验中使用可抽动的铜丝,其优点是
(4)实验中可观察到B中品红溶液的现象为
(5)浸有NaOH溶液的棉团的作用
您最近一年使用:0次
名校
2 . 氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意:
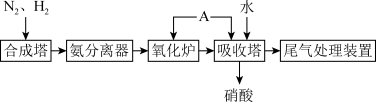
(1)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨_______ 的性质,从氨分离器中又回到合成塔中的物质是_______ 。
(2)请写出氧化炉内发生反应的化学方程式并用单线桥标出电子转移的方向和数目_______ 。
(3)向吸收塔中通入过量A是_______ ,作用是_______ 。
(4)硝酸可氧化绝大多数金属,而工业上盛装大量浓硝酸可用铝制容器,原因是_______ 。

(1)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨
(2)请写出氧化炉内发生反应的化学方程式并用单线桥标出电子转移的方向和数目
(3)向吸收塔中通入过量A是
(4)硝酸可氧化绝大多数金属,而工业上盛装大量浓硝酸可用铝制容器,原因是
您最近一年使用:0次
2022-08-18更新
|
86次组卷
|
2卷引用:广东省普宁市第二中学2021~2022学年高一下学期第一次月考化学试题



