1 . 现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为________ 热反应,且m+n______ p (填“>”、“=”或“<”) 。
(2)减压时,A的质量分数__________ 。(填“增大”、“减小”或“不变”,下同)
(3)若容积不变加入B,则B的转化率__________ 。
(4)若升高温度,则平衡时B、C的浓度之比将__________ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量__________ 。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色__________ ;而维持容器内压强不变,充入氖气时,混合物颜色 _______ 。(填“变深”、“变浅”或“不变”)。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)该反应的逆反应为
(2)减压时,A的质量分数
(3)若容积不变加入B,则B的转化率
(4)若升高温度,则平衡时B、C的浓度之比将
(5)若加入催化剂,平衡时气体混合物的总物质的量
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色
您最近一年使用:0次
2019-01-30更新
|
152次组卷
|
3卷引用:2017届湖北省恩施一中高三上学期开学考试化学试卷
名校
2 . (NH4)2Cr2O7用于有机合成催化剂,媒染剂,显影液等。某化学兴趣小组对(NH4)2Cr2O7的部分性质及组成进行探究。已知:Cr2O72-(橙色)+H2O 2CrO42-(黄色)+2H+。回答下列问题:
2CrO42-(黄色)+2H+。回答下列问题:
(1)在试管中加入少量(NH4)2Cr2O7固体,滴加足量浓KOH溶液,振荡、微热,观察到的主要现象是固体溶解、__________ 、__________ 。
(2)为探究(NH4)2Cr2O7 (摩尔质量252g/mol)的分解产物,按下图连接好装置,在A中加入5.040g样品进行实验。
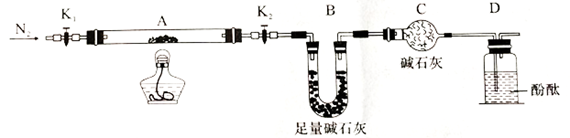
①仪器B的名称是__________ 。
②加热A至恒重,观察到D中溶液不变色,同时测得A、B中质量变化分别为2.00g、1.44g,写出重铬酸铵加热分解反应的化学方程式____________________ 。
③C的作用是__________ 。
(3)实验室常用甲醛法测定含(NH4)2Cr2O7的样品中氮的质量分数,其反应原理为:2Ba2++Cr2O72-+H2O=2BaCrO4↓+2H+、 4NH4++6HCHO =3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1molH+相当],然后用NaOH标准溶液滴定反应生成的酸。
实验步骤:称取样品2.800g,配成250mL溶液,移取25.00mL样品溶液于250mL锥形瓶中,用氯化钡溶液使Cr2O72-完全沉淀后,加入10mL20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用0.200 mol·L-1 NaOH标准溶液滴定至终点。重复上述操作3次。
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则滴定时用去NaOH标准溶液的体积__________ (填“偏大”、“偏小”或“无影响”);滴定时边滴边摇动锥形瓶,眼睛应观察__________ 。
②滴定结果如下表所示

该样品中氮的质量分数为__________ 。
 2CrO42-(黄色)+2H+。回答下列问题:
2CrO42-(黄色)+2H+。回答下列问题:(1)在试管中加入少量(NH4)2Cr2O7固体,滴加足量浓KOH溶液,振荡、微热,观察到的主要现象是固体溶解、
(2)为探究(NH4)2Cr2O7 (摩尔质量252g/mol)的分解产物,按下图连接好装置,在A中加入5.040g样品进行实验。

①仪器B的名称是
②加热A至恒重,观察到D中溶液不变色,同时测得A、B中质量变化分别为2.00g、1.44g,写出重铬酸铵加热分解反应的化学方程式
③C的作用是
(3)实验室常用甲醛法测定含(NH4)2Cr2O7的样品中氮的质量分数,其反应原理为:2Ba2++Cr2O72-+H2O=2BaCrO4↓+2H+、 4NH4++6HCHO =3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1molH+相当],然后用NaOH标准溶液滴定反应生成的酸。
实验步骤:称取样品2.800g,配成250mL溶液,移取25.00mL样品溶液于250mL锥形瓶中,用氯化钡溶液使Cr2O72-完全沉淀后,加入10mL20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用0.200 mol·L-1 NaOH标准溶液滴定至终点。重复上述操作3次。
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则滴定时用去NaOH标准溶液的体积
②滴定结果如下表所示

该样品中氮的质量分数为
您最近一年使用:0次
2019-01-13更新
|
828次组卷
|
3卷引用:【省级联考】湖北省2019届高三上学期1月联考测试理科综合化学试题
名校
3 . 以黄铜矿(主要成分二硫化亚铁铜CuFeS2)为原料,用Fe2(SO4)3溶液作浸取剂提取铜,总反应的离子方程式是CuFeS2+4Fe3+ Cu2++5Fe2++2S。
Cu2++5Fe2++2S。
(1)该反应中,Fe3+体现________ 性。
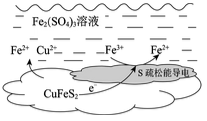
(2)上述总反应的原理如图所示。
负极的电极反应式是________ 。
(3)一定温度下,控制浸取剂pH=1,取三份相同质量黄铜矿粉末分别进行如下实验:
①对比实验I、II,通入空气,Cu2+浸出率提高的原因是________ 。
②由实验III推测,在浸取Cu2+过程中Ag+作催化剂,催化原理是:
ⅰ.CuFeS2+4Ag+=Fe2++Cu2++2Ag2S
ⅱ.Ag2S+2Fe3+=2Ag++2Fe2++S
为证明该催化原理,进行如下实验:
a.取少量黄铜矿粉末,加入少量0.0005mol·L-1Ag2SO4溶液,充分混合后静置。取上层清液,加入稀盐酸,观察到溶液中________ ,证明发生反应i。
b.取少量Ag2S粉末,加入________ 溶液,充分混合后静置。取上层清液,加入稀盐酸,有白色沉淀,证明发生反应ii。
(4)用实验II的浸取液电解提取铜的原理如图所示:
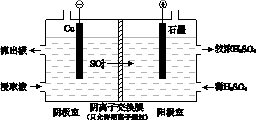
①电解初期,阴极没有铜析出。用电极反应式解释原因是_______________ 。
②将阴极室的流出液送入阳极室,可使浸取剂再生,再生的原理是_____________________ 。
 Cu2++5Fe2++2S。
Cu2++5Fe2++2S。(1)该反应中,Fe3+体现

(2)上述总反应的原理如图所示。
负极的电极反应式是
(3)一定温度下,控制浸取剂pH=1,取三份相同质量黄铜矿粉末分别进行如下实验:
| 实验 | 操作 | 2小时后Cu2+浸出率/% |
| I | 加入足量0.10mol·L-1Fe2(SO4)3溶液 | 78.2 |
| II | 加入足量0.10mol·L-1Fe2(SO4)3溶液,通入空气 | 90.8 |
| III | 加入足量0.10mol·L-1Fe2(SO4)3溶液,再加入少量0.0005mol·L-1Ag2SO4溶液 | 98.0 |
②由实验III推测,在浸取Cu2+过程中Ag+作催化剂,催化原理是:
ⅰ.CuFeS2+4Ag+=Fe2++Cu2++2Ag2S
ⅱ.Ag2S+2Fe3+=2Ag++2Fe2++S
为证明该催化原理,进行如下实验:
a.取少量黄铜矿粉末,加入少量0.0005mol·L-1Ag2SO4溶液,充分混合后静置。取上层清液,加入稀盐酸,观察到溶液中
b.取少量Ag2S粉末,加入
(4)用实验II的浸取液电解提取铜的原理如图所示:

①电解初期,阴极没有铜析出。用电极反应式解释原因是
②将阴极室的流出液送入阳极室,可使浸取剂再生,再生的原理是
您最近一年使用:0次
2017-05-20更新
|
348次组卷
|
5卷引用:湖北省宜昌市第一中学2018届高三年级适应性训练(二)理综化学试题
湖北省宜昌市第一中学2018届高三年级适应性训练(二)理综化学试题宁夏六盘山高级中学2017届高三第四次模拟考试理科综合化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题08-2020年北京新高考化学模拟试题北京理工大学附属中学2022-2023学年高三上学期12月月考化学试题安徽省定远县育才学校2019-2020学年高二下学期期末考试化学试题



