名校
解题方法
1 . 查阅资料知:FeCl3是一种共价化合物,熔点为306℃,沸点为315℃,无水FeCl3在空气中易潮解,加热易升华。
(1)实验室制备无水FeCl3的实验装置如图:
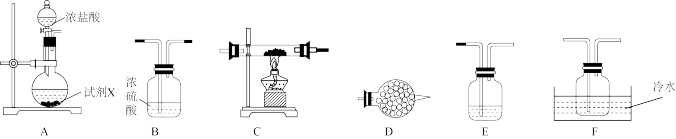
回答下列问题:
①上述仪器的连接顺序是A→_______ →B→_______ →_______ →D(填标号)
②试剂X是_______ (填名称)。
③装置D的作用是_______ 。
④C处右侧选用较粗玻璃管的原因是_______ 。
(2)工业上用NaClO3氧化酸性FeCl2废液制得。
①NaClO3氧化酸性FeCl2制备FeCl3的离子方程式为_______ 。
②为检验上述方法制备的FeCl3固体中是否含有FeCl2,应该进行的实验操作是_______ 。
③若酸性FeCl2废液中,c(Fe2+)=2.0×10-1mol•L-1,c(Fe3+)=1.0×10-2mol•L-1,c(Cl-)=5.3×10-1mol•L-1,则该溶液的 为
为 _______ 。(其他离子忽略不计)
(3)实验室中还常用 与FeCl3∙6H2O
与FeCl3∙6H2O共热 制备无水FeCl3,该反应的化学方程式为_______ 。
(1)实验室制备无水FeCl3的实验装置如图:

回答下列问题:
①上述仪器的连接顺序是A→
②试剂X是
③装置D的作用是
④C处右侧选用较粗玻璃管的原因是
(2)工业上用NaClO3氧化酸性FeCl2废液制得。
①NaClO3氧化酸性FeCl2制备FeCl3的离子方程式为
②为检验上述方法制备的FeCl3固体中是否含有FeCl2,应该进行的实验操作是
③若酸性FeCl2废液中,c(Fe2+)=2.0×10-1mol•L-1,c(Fe3+)=1.0×10-2mol•L-1,c(Cl-)=5.3×10-1mol•L-1,则该溶液的
 为
为 (3)实验室中还常用
 与FeCl3∙6H2O
与FeCl3∙6H2O
您最近一年使用:0次
名校
2 . (1)常温下,0.05 mol/L Ba(OH)2溶液中c(OH-)= _____ ,pH=______ 。
(2)某温度下,纯水中的c(H+)= 2×10-7mol/L,则此时溶液中的c(OH-)=____ ;若温度不变,滴入稀盐酸,使c(H+)= 5×10-4 mol/L,则溶液中c(OH-)=____ ,此时溶液中由水电离产生的c(H+)= _____ 。
(3)已知:lg2=0.3,lg3=0.5,lg5=0.7。常温时,将pH为5的HCl溶液与pH为2的H2SO4溶液等体积混合,混合后溶液的pH约为___________ 。
(4)常温下,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈______ (填“酸性”,“中性”或“碱性”)。
(5)25℃时,已知 HF 的电离常数为3.6×10-4,H3PO4的电离常数K1 =7.5×10-3,K2=6.2×10-8,K3 =4.4×10-13。则足量NaF溶液和H3PO4溶液反应的离子方程式为_______________________________ 。
(2)某温度下,纯水中的c(H+)= 2×10-7mol/L,则此时溶液中的c(OH-)=
(3)已知:lg2=0.3,lg3=0.5,lg5=0.7。常温时,将pH为5的HCl溶液与pH为2的H2SO4溶液等体积混合,混合后溶液的pH约为
(4)常温下,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈
(5)25℃时,已知 HF 的电离常数为3.6×10-4,H3PO4的电离常数K1 =7.5×10-3,K2=6.2×10-8,K3 =4.4×10-13。则足量NaF溶液和H3PO4溶液反应的离子方程式为
您最近一年使用:0次
名校
3 . 已知在酸性条件下,硫代硫酸钠会发生歧化反应:H2SO4+Na2S2O3=Na2SO4+SO2↑+S↓+H2O。设NA为阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,20gD2O中含有的氧原子的数目为NA |
| B.pH=2的H2SO4溶液中,含有的H+数目为0.02NA |
| C.常温下,向100mL18mol•L-1浓硫酸中加入足量的Cu,该过程转移电子的数目为1.8NA |
| D.32gSO2与足量的O2充分反应,生成的SO3分子总数为0.5NA |
您最近一年使用:0次
2023-04-20更新
|
385次组卷
|
4卷引用:选择题1-5
(已下线)选择题1-5辽宁省葫芦岛市协作校2022-2023学年高三下学期第一次考试化学试题(已下线)考点02 物质的量 气体摩尔体积(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)福建省永春第一中学2023届高三下学期适应性考试(五)化学试题



