1 . 下列说法正确的是
| A.水库中的钢闸门通常连接锌块,是采用了牺牲阳极的阴极保护法 |
| B.化学电源都是一次能源 |
| C.铁的表面镀铜的过程中,铜极连接电源负极 |
| D.合金的熔点都高于它的成分金属,合金的耐腐蚀性也都比其组成成分金属强 |
您最近一年使用:0次
2 . 下列说法正确的是
| A.铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
| B.铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| C.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al |
| D.电解食盐水一段时间后,可通入一定量的HCl气体来恢复原溶液 |
您最近一年使用:0次
11-12高二下·福建·期中
3 . 下列说法正确的是
| A.铅蓄电池放电时铅电极发生还原反应 |
| B.电解饱和食盐水时在阳极得到氯气,阴极得到金属钠 |
| C.给铁钉镀铜可采用CuSO4作电镀液 |
| D.生铁浸泡在食盐水中发生析氢腐蚀 |
您最近一年使用:0次
2016-04-28更新
|
117次组卷
|
4卷引用:2011-2012学年福建师大附中高二下学期期中考试化学试卷
(已下线)2011-2012学年福建师大附中高二下学期期中考试化学试卷2015-2016学年新疆兵团农二师华山中学高二下第一次月考化学试卷 河南省鹤壁市淇滨高级中学2017-2018学年高二上学期第三次月考化学试题陕西省延安市黄龙县中学2021-2022学年高二上学期第一次月考化学试题
12-13高二上·福建三明·期末
4 . Ⅰ.钢铁工业是国家工业的基础。请回答钢铁腐蚀、防护过程中的有关问题。
请写出钢铁在碱性、潮湿的环境下发生电化学腐蚀正极的电极反应式:_______________ ;
下列哪个装置示意图可防止铁棒被腐蚀___________________ 。

Ⅱ.某小组为研究电化学原理,设计如下图装置。请回答下列问题:

(1)a和b不连接时,铁片上发生反应的离子方程式为________________ ,
此时能量转化形式主要是化学能转化为__________ 能。
(2)a和b用导线连接时,外电路中的电子是从______ 电极流出(填“Fe”或“Cu”),______ (填Cu2+ 或SO42-)离子朝负极移动,Cu极所发生反应的电极反应式为______________ 。
(3)现在要在铁片上镀一层金属铜,则a极要和直流电源的________ (填“正极”或“负极”)连接;此时铜片上发生的电极反应式为________________________ 。
请写出钢铁在碱性、潮湿的环境下发生电化学腐蚀正极的电极反应式:
下列哪个装置示意图可防止铁棒被腐蚀

Ⅱ.某小组为研究电化学原理,设计如下图装置。请回答下列问题:

(1)a和b不连接时,铁片上发生反应的离子方程式为
此时能量转化形式主要是化学能转化为
(2)a和b用导线连接时,外电路中的电子是从
(3)现在要在铁片上镀一层金属铜,则a极要和直流电源的
您最近一年使用:0次
11-12高二上·福建厦门·期中
解题方法
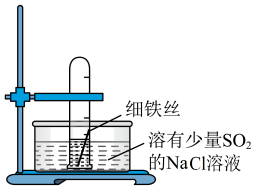
5 . 有一研究性学习小组在探究有关钢铁的腐蚀情况,他们进行了如下实验:在一个水槽中盛装1000 mL水,加入一定量的NaCl 固体溶解后通入SO2气体至溶液pH值约为4左右,另取一支试管(带刻度,规格50mL),一条约5cm的细钢丝,将钢丝放入试管中,加入约 10mL前面配好的溶液,迅速用拇指扣住试管口倒扣于水槽中,用铁架台将试管固定,如右下图。过一会儿:
(1)观察到试管中的液面逐渐下降,这说明
在该条件下,铁丝发生了______________ 腐蚀,
正极材料是______ 电极反应是__________________
(2)再过一段时间发现液面停止下降,并且开始逐渐
上升,露在液面上的铁丝表面由原来的银白色变棕褐色,这说明在该条件下,铁丝发生了
___________ 腐蚀,正极的电极反应为___________________________________
①总反应为:____________________________________ ;①反应的产物极易被进一步氧化,生成红褐色物质,②该反应的化学方程式为:____________________________ 若铁锈的组成为:Fe2O3·xH2O ,试写出由②反应的产物在通常条件下生成铁锈的反应方程式:
③__________________________________________________________________
(3)已知原来铁丝质量为2 g,发生(1)情况时,依液面下降的高度折为标准状况下的体积是5.6mL,则此时,铁丝的质量变为_________ g ,随后液面开始上升,即发生(2)的变化,依最终液面上升的高度折算为标准状况下的体积比最开始刚倒扣于水槽中试管中溶液的体积多了1.12mL,通过计算,(2)的过程共消耗氧气_______ mL,若x值为2,那么铁丝的质量应为___________ g(以上计算有效数字保留至小数点后三位)

(1)观察到试管中的液面逐渐下降,这说明
在该条件下,铁丝发生了
正极材料是
(2)再过一段时间发现液面停止下降,并且开始逐渐
上升,露在液面上的铁丝表面由原来的银白色变棕褐色,这说明在该条件下,铁丝发生了
①总反应为:
③
(3)已知原来铁丝质量为2 g,发生(1)情况时,依液面下降的高度折为标准状况下的体积是5.6mL,则此时,铁丝的质量变为
您最近一年使用:0次



