1 . 下列有关实验操作、现象(或数据)和结论均正确的是
| 选项 | 实验操作 | 实验现象或数据 | 结论 |
| A | 将变黑的银器放入装满食盐水的铝盆中,二者直接接触 | 银器恢复往日光泽 |  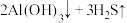 |
| B | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的 悬浊液 悬浊液 | 无砖红色沉淀 | 蔗糖未发生水解 |
| C | 向 溶液中滴加紫色石蕊试液 溶液中滴加紫色石蕊试液 | 溶液变蓝 | 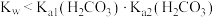 |
 | 石蜡油加强热,将产生的气体通入 的 的 溶液 溶液 | 溶液由红棕色变无色 | 气体中含有不饱和炔烃 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 双阴极微生物燃料电池处理含NH4废水的工作原理如图2所示,双阴极通过的电流相等,废水在电池中的运行模式如图1所示,下列说法错误的是

| A.I、Ⅲ为阴极室,Ⅱ为阳极室 |
| B.离子交换膜为阳离子交换膜 |
C.Ⅲ室会发生反应 |
| D.生成3.5gN2,理论上需要消耗10gO2 |
您最近一年使用:0次
3 . 微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 的溶液为例)。下列说法错误的是
的溶液为例)。下列说法错误的是
 的溶液为例)。下列说法错误的是
的溶液为例)。下列说法错误的是
| A.b极为正极、a极为负极 |
B.负极反应为 |
| C.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜 |
| D.当电路中转移1 mol电子时,模拟海水理论上除盐58.5 g |
您最近一年使用:0次
4 . 图1是一种双极膜(将 解离成
解离成 和
和 )电解合成
)电解合成 的反应器的简化装置(已知:法拉第常数
的反应器的简化装置(已知:法拉第常数 )。图2是一种低成本储能电池装置。下列说法正确的是
)。图2是一种低成本储能电池装置。下列说法正确的是
 解离成
解离成 和
和 )电解合成
)电解合成 的反应器的简化装置(已知:法拉第常数
的反应器的简化装置(已知:法拉第常数 )。图2是一种低成本储能电池装置。下列说法正确的是
)。图2是一种低成本储能电池装置。下列说法正确的是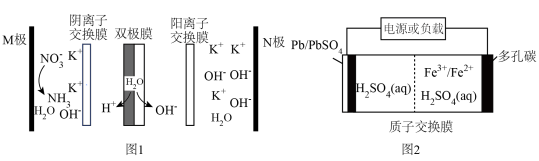
| A.用图2装置给图1供电,电极M接多孔碳极 |
B.图2装置放电总反应: |
C.电解合成过程中,图1中左侧 通过阴离子交换膜向右移动 通过阴离子交换膜向右移动 |
D.若N极产生 ,理论上外电路流过的电量为 ,理论上外电路流过的电量为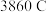 |
您最近一年使用:0次
2024-04-29更新
|
70次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
解题方法
5 . 某新型电池结构示意图如图所示,电解质为 溶液、
溶液、 溶液、 NaOH溶液,通过m和n两种离子交换膜将电解质溶液隔开,形成X、Y、Z三个电解质溶液区域。下列说法正确的是
溶液、 NaOH溶液,通过m和n两种离子交换膜将电解质溶液隔开,形成X、Y、Z三个电解质溶液区域。下列说法正确的是
 溶液、
溶液、 溶液、 NaOH溶液,通过m和n两种离子交换膜将电解质溶液隔开,形成X、Y、Z三个电解质溶液区域。下列说法正确的是
溶液、 NaOH溶液,通过m和n两种离子交换膜将电解质溶液隔开,形成X、Y、Z三个电解质溶液区域。下列说法正确的是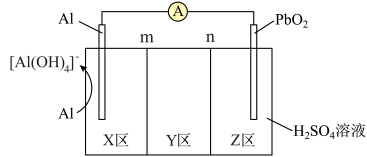
A.放电时,正极电极反应式为:A1+4OH--3e-=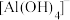 |
B.m为阴离子交换膜,放电时, 通过m膜向X区移动 通过m膜向X区移动 |
| C.放电时,消耗5.4g A1时Z区电解质溶液质量减少48.0 g |
D.放电时, 增重6.4g时Y区离子数目减少了0.3 NA个 增重6.4g时Y区离子数目减少了0.3 NA个 |
您最近一年使用:0次
名校
6 . 习近平总书记在浙江湖州市安吉县考察时提出了一个科学论断“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。请回答下列问题:
(1)硫酸工业排出的尾气(主要含 )可用软锰矿浆(
)可用软锰矿浆( )吸收,写出如图所示“反应”的化学方程式为
)吸收,写出如图所示“反应”的化学方程式为________ 。 和CO的方法之一是在汽车的排气管上装一个催化转化装置,使
和CO的方法之一是在汽车的排气管上装一个催化转化装置,使 和CO在催化剂作用下转化为无毒物质,发生反应
和CO在催化剂作用下转化为无毒物质,发生反应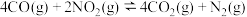 .一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和
.一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和 ,
, 的物质的量随时间的变化曲线如图所示。
的物质的量随时间的变化曲线如图所示。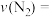
________ 。
②从11min起其他条件不变,压缩容器的容积变为1L,则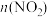 的变化曲线可能为图中的
的变化曲线可能为图中的________ (填字母)。
③恒温恒容条件下,不能说明该反应已经达到平衡状态的是________ (填标号)。
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.容器内混合气体密度保持不变
D.容器内混合气体平均相对分子质量保持不变
(3)利用反应 构成原电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题:
构成原电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题:________ (填“正极”或“负极”),发生________ (填“氧化反应”或“还原反应”),电极B上发生的电极反应为________ 。
(1)硫酸工业排出的尾气(主要含
 )可用软锰矿浆(
)可用软锰矿浆( )吸收,写出如图所示“反应”的化学方程式为
)吸收,写出如图所示“反应”的化学方程式为
 和CO的方法之一是在汽车的排气管上装一个催化转化装置,使
和CO的方法之一是在汽车的排气管上装一个催化转化装置,使 和CO在催化剂作用下转化为无毒物质,发生反应
和CO在催化剂作用下转化为无毒物质,发生反应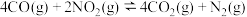 .一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和
.一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和 ,
, 的物质的量随时间的变化曲线如图所示。
的物质的量随时间的变化曲线如图所示。
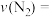
②从11min起其他条件不变,压缩容器的容积变为1L,则
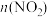 的变化曲线可能为图中的
的变化曲线可能为图中的③恒温恒容条件下,不能说明该反应已经达到平衡状态的是
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.容器内混合气体密度保持不变
D.容器内混合气体平均相对分子质量保持不变
(3)利用反应
 构成原电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题:
构成原电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能,回答下列问题: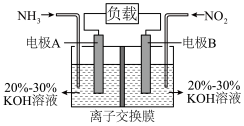
您最近一年使用:0次
名校
解题方法
7 . 钠基—海水电池因其具有环境友好、能量密度高和海水储量丰富且易得等优势,有望成为新一代储能器件,其工作原理如图所示。下列说法正确的是
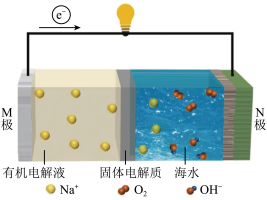
| A.M极为正极,发生还原反应 | B.放电时, 由左室移至海水中 由左室移至海水中 |
C.N极发生的电极反应为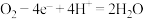 | D.可以将有机电解液换为低成本的钠盐水溶液 |
您最近一年使用:0次
名校
8 . 银饰用久了表面会有一层 而发黑,将银饰与
而发黑,将银饰与 片接触并加入
片接触并加入 溶液,可以除去银饰表面的
溶液,可以除去银饰表面的 ,下列说法正确的是
,下列说法正确的是
 而发黑,将银饰与
而发黑,将银饰与 片接触并加入
片接触并加入 溶液,可以除去银饰表面的
溶液,可以除去银饰表面的 ,下列说法正确的是
,下列说法正确的是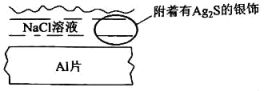
A. 是正极 是正极 | B.阳离子向银饰移动 |
C.电子由负极经 溶液流向正极 溶液流向正极 | D. 表面发生反应: 表面发生反应: |
您最近一年使用:0次
名校
解题方法
9 . 化学电源在生产生活中有着广泛的应用,同学们常常通过设计实验和查阅资料的方式学习化学电源的相关知识。
(1)甲同学为了解化学反应中的能量转化,设计了一组对比实验(实验装置如图Ⅰ和图Ⅱ)。预计产生气体的速率Ⅰ___________ Ⅱ(>、<或=),温度计的示数Ⅰ___________ Ⅱ(>、<或=);___________ (填序号)。
① ;②
;② ;③
;③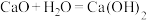
(3)用 和
和 组合形成的质子交换膜燃料电池的结构如下图:
组合形成的质子交换膜燃料电池的结构如下图:___________
②若线路中转移2mol电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(4)某原电池装置初始状态如图所示,交换膜两侧的溶液体积均为2L,该电池总反应为___________ ,当电路中转移1mol电子时,共有___________ mol离子通过交换膜,交换膜右侧溶液中
___________  (忽略溶液体积变化和
(忽略溶液体积变化和 溶于水)。
溶于水)。
(1)甲同学为了解化学反应中的能量转化,设计了一组对比实验(实验装置如图Ⅰ和图Ⅱ)。预计产生气体的速率Ⅰ

①
 ;②
;② ;③
;③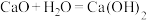
(3)用
 和
和 组合形成的质子交换膜燃料电池的结构如下图:
组合形成的质子交换膜燃料电池的结构如下图: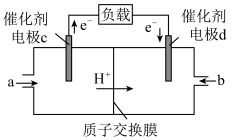
②若线路中转移2mol电子,则该燃料电池理论上消耗的
 在标准状况下的体积为
在标准状况下的体积为(4)某原电池装置初始状态如图所示,交换膜两侧的溶液体积均为2L,该电池总反应为

 (忽略溶液体积变化和
(忽略溶液体积变化和 溶于水)。
溶于水)。
您最近一年使用:0次
名校
解题方法
10 . 用热再生氨电池处理含Cu2+电镀废液的装置如图。该装置由电池部分和热再生部分组成:电池部分中,a极室为(NH4)2SO4-NH3混合液,b极室为(NH4)2SO4溶液;热再生部分加热a极室流出液,使[Cu(NH3)4]2+分解。下列说法不正确 的是

| A.装置中的离子交换膜为阳离子交换膜 |
| B.a极的电极反应为:Cu-2e-+4NH3=[Cu(NH3)4]2+ |
| C.电池部分的总反应为:Cu2++4NH3=[Cu(NH3)4]2+ |
| D.该方法可以富集Cu2+并产生电能,同时循环利用NH3 |
您最近一年使用:0次
2024-04-13更新
|
505次组卷
|
4卷引用:湖北省武汉市洪山高级中学2024届高三下学期第 2次模拟考试化学试卷
湖北省武汉市洪山高级中学2024届高三下学期第 2次模拟考试化学试卷 2023-2024学年海淀区第二学期期中考试高三化学试卷(已下线)北京市西城区2024届高三下学期第三次模拟测试化学试题北京市海淀区2023-2024学年高三下学期期中练习化学试题



