名校
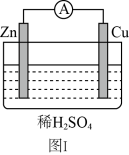
1 . 电能是现代社会应用最广泛的能源之一。______ 。
a.负极反应是 b.电子由Zn片通过导线流向Cu片
b.电子由Zn片通过导线流向Cu片
c.一段时间后,溶液的pH减小 d.溶液中的 向Cu片移动
向Cu片移动
(2)图Ⅰ所示原电池中,当Cu表面析出4.48 L氢气(标准状况)时,导线中通过的电子的物质的量为______ mol。
(3)图Ⅱ所示装置为电化学气敏传感器,通过电压表示数可测量环境中 的含量。电极b是
的含量。电极b是______ (填“正”或“负”)极;溶液中 向电极
向电极______ (填“a”或“b”)移动。
(4)图Ⅱ所示原电池中,a极的电极反应式为______ ,b极的电极反应式为______ 。

a.负极反应是
 b.电子由Zn片通过导线流向Cu片
b.电子由Zn片通过导线流向Cu片c.一段时间后,溶液的pH减小 d.溶液中的
 向Cu片移动
向Cu片移动(2)图Ⅰ所示原电池中,当Cu表面析出4.48 L氢气(标准状况)时,导线中通过的电子的物质的量为
(3)图Ⅱ所示装置为电化学气敏传感器,通过电压表示数可测量环境中
 的含量。电极b是
的含量。电极b是 向电极
向电极(4)图Ⅱ所示原电池中,a极的电极反应式为
您最近半年使用:0次
名校
2 . 水体中氨氮含量过高会造成水体富营养化。利用微生物燃料电池可以对废水中氨氮进行处理的装置如图,两极材料均为石墨棒,下列说法正确的是
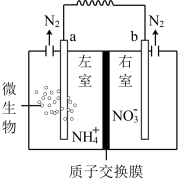

| A.a极表面发生还原反应 |
B.工作时 通过质子交换膜移向左室 通过质子交换膜移向左室 |
C.标准状况下,每转移 电子,负极生成 电子,负极生成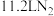 ,且左室 ,且左室 降低 降低 |
D.正极电极反应式为: |
您最近半年使用:0次
解题方法
3 . 电化学原理在污染治理方面有着重要的作用。
Ⅰ.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和 :
: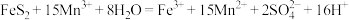
已知:两电极为完全相同的惰性电极。
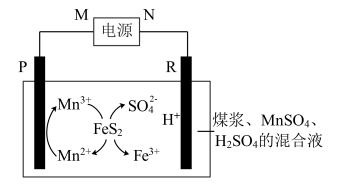
回答下列问题:
(1)N为电源的_______ (填“正极”或“负极”)。
(2)P上的电极反应为_______ 。
(3)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式_______ 。
(4)电解池工作时, 往
往_______ (填“P”或“R”)极移动,一段时间后,混合液中 的物质的量
的物质的量_______ (填“变大”、“变小”或“不变”)。
(5)电解过程中,混合溶液中的pH将_______ (填“变大”、“变小”或“不变”),理由是_______ 。
Ⅱ.微生物电池可用来处理废水中的对氯苯酚,原理如图所示。
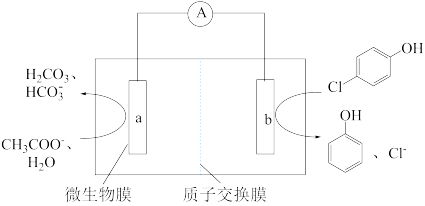
(6)该电池放电时,电子从_______ (填“b→a”或“a→b”)。
(7)a极上生成H2CO3的电极反应为_______ 。
(8)已知b极的电极反应为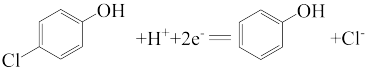 ,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为
,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为_______ mol(溶液体积变化忽略不计)。
Ⅰ.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和
 :
: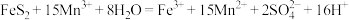
已知:两电极为完全相同的惰性电极。

回答下列问题:
(1)N为电源的
(2)P上的电极反应为
(3)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式
(4)电解池工作时,
 往
往 的物质的量
的物质的量(5)电解过程中,混合溶液中的pH将
Ⅱ.微生物电池可用来处理废水中的对氯苯酚,原理如图所示。

(6)该电池放电时,电子从
(7)a极上生成H2CO3的电极反应为
(8)已知b极的电极反应为
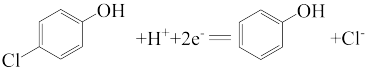 ,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为
,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为
您最近半年使用:0次
解题方法
4 . 化学能在一定条件下可转化为电能。
(1)某原电池装置如图所示。其中,Zn电极为原电池的_______ 极(填“正”或“负”),电极反应式是_______ 。能证明化学能转化为电能的实验现象是:_______ 、铜片上产生大量气泡。
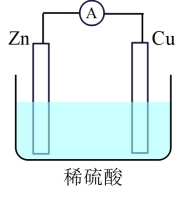
当铜表面析出22.4mL氢气(标准状况)时,导线中通过了_______ mol电子。
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如下图所示:

①NiO电极上发生的是_______ 反应(填“氧化”或“还原”)。
②外电路中,电子的流动方向是从_______ 电极流向_______ 电极(填“NiO”或“Pt”)。
③Pt电极上的电极反应式为_______ 。
(1)某原电池装置如图所示。其中,Zn电极为原电池的

当铜表面析出22.4mL氢气(标准状况)时,导线中通过了
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如下图所示:

①NiO电极上发生的是
②外电路中,电子的流动方向是从
③Pt电极上的电极反应式为
您最近半年使用:0次
名校
解题方法
5 . 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是
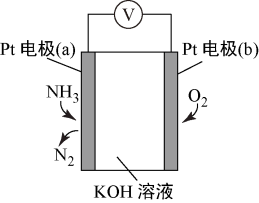
| A.O2在电极b上发生还原反应 |
| B.溶液中OH-向电极a移动 |
| C.反应消耗的NH3与O2的物质的量之比为4:5 |
| D.负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O |
您最近半年使用:0次
2021-08-06更新
|
1357次组卷
|
44卷引用:2015届北京市西城区高三二模理综化学试卷
2015届北京市西城区高三二模理综化学试卷2015-2016学年北京市东城区高二下学期期末化学试卷北京市北大附中实验学校2020-2021学年高二上学期10月月考化学试题北京市理工大学附属中学2020-2021学年高二上学期10月月考化学试题2016届广西柳铁一中高三上学期第一次月考理综化学试卷2017届四川省射洪中学高三上学期入学考试化学试卷2017届广东省华侨中学高三上学期摸底考试理综化学试卷2017届湖北省荆、荆、襄、宜四地七校高三上联考一化学卷2016-2017学年安徽省合肥一中等名校高二上期末化学卷2017届宁夏固原市第一中学高三下学期第一次月考理综化学试卷22016-2017学年湖北省鄂东南省级示范高中高二下学期期中联考化学试卷河北省衡水中学2016-2017学年高一下学期期中考试化学试题湖北省荆州中学2016-2017学年高一下学期5月阶段测化学试题安徽省无为县2018届高三上学期第一次月考化学试题辽宁省营口中学2017-2018学年高二上学期期末考试化学试题河南省三门峡市2018届高三上学期期末考试化学试题【全国百强校】河北省武邑中学2019届高三上学期第三次调研考试化学试题山西省祁县中学2017-2018学年高一下学期第一次月考化学试题【全国百强校】黑龙江省大庆实验中学2017-2018学年高二上学期期末考试化学试题【全国百强校】湖北省武汉市华中师范大学第一附属中学2018-2019学年高二上学期期末考试化学试题【市级联考】湖北省天门市、潜江市、应城市2018-2019学年高一下学期期中联考化学试题山西省应县第一中学校2018-2019学年高一月考八(6月月考)化学试题山东省滕州市第一中学2019-2020学年高一下学期第一次月考化学试题甘肃省静宁县第一中学2019-2020学年高一下学期期中考试(第二次月考)化学试题江苏省沭阳县修远中学、泗洪县淮北中学、洪翔中学2019-2020学年高二下学期联考化学试题天津市和平区2018-2019高二期末考试化学试题福建省连城县第一中学2020-2021学年高二上学期第一次月考化学试题鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第2节 化学能转化为电能——电池 课时2 化学电源广东省广州市执信中学2020-2021学年高二上学期9月月考化学试题青海省西宁市海湖中学2021届高三上学期第二阶段考试化学试题湖南省长沙市南雅中学2020-2021学年高二上学期第三次月考化学试题高中化学苏教2019版必修第二册-专题6 第三单元 第2课时 化学电源湖南师范大学附属中学2020-2021学年高一下学期第一次月考化学试题陕西省黄陵中学2020-2021学年高一下学期期中考试化学试题选择性必修1(SJ)专题1第二单元课时2 化学电源广东省惠州市惠城区2021--2022学年高三上学期8月开学摸底化学试题(已下线)课时30 新型原电池装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题19 原电池 化学电源(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练2017届宁夏固原市第一中学高三下学期第一次月考理综化学试卷1广西罗城仫佬族自治县高级中学2021-2022学年高二上学期开学检测化学试题内蒙古呼伦贝尔市满洲里市第一中学2021-2022学年高一下学期期末考试化学试题四川省内江市第六中学2022-2023学年高三上学期入学考试化学试题 1.2.2化学电源 课中广东省湛江市第二中学2023届高三上学期第一次月考化学试题
名校
6 . Li—CuO二次电池的比能量高、工作温度宽,性能优异,广泛应用于军事和空间领域。
(1)Li—CuO电池中,金属锂做_______ 极 。
(2)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣。比较Li、Na、Al分别作为电极时比能量的大小:____________ 。
(3)通过如下过程制备CuO。

①过程Ⅰ,H2O2的作用是__________________ 。
②过程Ⅱ产生Cu2(OH)2CO3的离子方程式是_____________________ 。
③过程Ⅱ,将CuSO4溶液加到Na2CO3溶液中,研究二者不同物质的量之比与产品纯度的关系(用测定铜元素的百分含量来表征产品的纯度),结果如下:
已知:Cu2(OH)2CO3中铜元素的百分含量为57.7%。
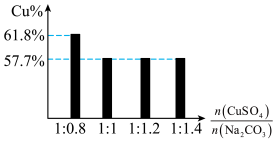
二者比值为1:0.8时,产品中可能含有的杂质是_____________ ,产生该杂质的原因是_________________________________ 。
④ 过程Ⅲ反应的化学方程式是_________________________ 。
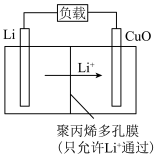
(4)Li—CuO二次电池以含Li+的有机溶液为电解质溶液,其工作原理示意如下。放电时,正极的电极反应式是______________________ 。
(1)Li—CuO电池中,金属锂做
(2)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣。比较Li、Na、Al分别作为电极时比能量的大小:
(3)通过如下过程制备CuO。

①过程Ⅰ,H2O2的作用是
②过程Ⅱ产生Cu2(OH)2CO3的离子方程式是
③过程Ⅱ,将CuSO4溶液加到Na2CO3溶液中,研究二者不同物质的量之比与产品纯度的关系(用测定铜元素的百分含量来表征产品的纯度),结果如下:
已知:Cu2(OH)2CO3中铜元素的百分含量为57.7%。

二者比值为1:0.8时,产品中可能含有的杂质是
④ 过程Ⅲ反应的化学方程式是
(4)Li—CuO二次电池以含Li+的有机溶液为电解质溶液,其工作原理示意如下。放电时,正极的电极反应式是

您最近半年使用:0次
2017-10-25更新
|
522次组卷
|
4卷引用:【市级联考】北京市2019届高三上学期一轮复习理科综合能力测试化学试题
【市级联考】北京市2019届高三上学期一轮复习理科综合能力测试化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题09-2020年北京新高考化学模拟试题山东省济南外国语学校2018届高三上学期阶段考试化学试题(已下线)寒假作业08 原电池-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)



