1 . 从NO 、SO
、SO 、H+、Cu2+、Ba2+、Ag+、Cl-等离子中选出适当的离子组成电解质,采用惰性电极对其溶液进行电解。
、H+、Cu2+、Ba2+、Ag+、Cl-等离子中选出适当的离子组成电解质,采用惰性电极对其溶液进行电解。
(1)两极分别放出H2和O2时,电解质的化学式可能是___________ (至少答一种,下同)。
(2)若阴极析出金属、阳极放出O2时,电解质的化学式可能是___________ 。
(3)两极分别放出气体,且体积比为1∶1,电解质的化学式可能是___________ 。
 、SO
、SO 、H+、Cu2+、Ba2+、Ag+、Cl-等离子中选出适当的离子组成电解质,采用惰性电极对其溶液进行电解。
、H+、Cu2+、Ba2+、Ag+、Cl-等离子中选出适当的离子组成电解质,采用惰性电极对其溶液进行电解。(1)两极分别放出H2和O2时,电解质的化学式可能是
(2)若阴极析出金属、阳极放出O2时,电解质的化学式可能是
(3)两极分别放出气体,且体积比为1∶1,电解质的化学式可能是
您最近一年使用:0次
2023-08-26更新
|
137次组卷
|
6卷引用:4.2.1 电解池原理-同步学习必备知识
(已下线)4.2.1 电解池原理-同步学习必备知识高二人教版选修4 第四章 第三节 电解池(已下线)1.2.3 电解池的工作原理及应用(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)第1课时 电解原理第1课时 电解的原理湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题15 电解池
22-23高二上·全国·课时练习
2 . 下列关于电化学知识说法正确的是
| A.电解AlCl3、FeCl3、CuCl2的混合溶液,在阴极上依次析出Cu、Fe、Al |
| B.电解CuSO4溶液一段时间后,加入适量Cu(OH)2可以使溶液恢复至原状态 |
C.铅蓄电池在充电时,连接电源正极发生的电极反应为:PbSO4+2e-=Pb+SO |
| D.将钢闸门与直流电流的负极相连,可防止钢闸门腐蚀 |
您最近一年使用:0次
22-23高二上·全国·课时练习
解题方法
3 . 火法炼铜得到的粗铜中含多种杂质(如锌、金和银等),其性能远不能达到电气工业的要求,工业上常用电解精炼法将粗铜提纯。在电解精炼时
| A.粗铜接电源负极 |
| B.纯铜做阴极 |
| C.杂质都将以单质形式沉积到池底 |
| D.纯铜片增重2.56g,电路中通过电子为0.04mol |
您最近一年使用:0次
22-23高二上·全国·课时练习
4 . 如图所示,通电5min后,第③极增重2.16g,此时CuSO4恰好电解完。设A池中原混合溶液的体积为200mL。
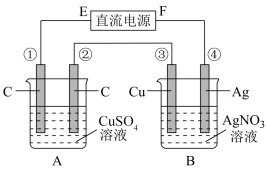
(1)电源F为______ 极;第②极为_____ 极;B池为_____ 池。
(2)A池中第②极上的电极反应式为_____ 。
(3)通电前A池中原混合溶液Cu2+的浓度为_____ 。

(1)电源F为
(2)A池中第②极上的电极反应式为
(3)通电前A池中原混合溶液Cu2+的浓度为
您最近一年使用:0次
22-23高二上·全国·课时练习
解题方法
5 . 在铁制品上镀上一定厚度的锌层,以下设计方案正确的是
| A.锌做阳极,镀件做阴极,溶液中含有Zn2+ |
| B.铂做阴极,镀件做阳极,溶液中含有Zn2+ |
| C.锌做阳极,镀件做阴极,溶液中含有Fe2+ |
| D.锌做阴极,镀件做阳极,溶液中含有Zn2+ |
您最近一年使用:0次
22-23高二上·全国·课后作业
解题方法
6 . 请按要求回答下列问题。
(1)根据图1回答①②:
A电极可观察到的现象是_______ ;B电极的电极反应式为_______ 。
②打开K1,合并K2。
A电极可观察到的现象是_______ ;B电极的电极反应式为_______ ;
(2)根据图2回答③④:_______ ,电解反应的离子方程式为_______ ;
④实验完成后,铜电极增重a g,石墨电极产生标准状况下的气体体积为_______ L。
(1)根据图1回答①②:

A电极可观察到的现象是
②打开K1,合并K2。
A电极可观察到的现象是
(2)根据图2回答③④:

④实验完成后,铜电极增重a g,石墨电极产生标准状况下的气体体积为
您最近一年使用:0次
7 . 如图所示X、Y分别是直流电源的两极,Z溶液可能为:①稀硫酸;②NaOH溶液;③Na2SO4溶液;④CuCl2溶液;⑤NaCl溶液;⑥稀盐酸;⑦CuSO4溶液。

(1)若通电后发现a、b两电极上均有气体产生,且V(a):V(b)=2:1,则电极a为_______ 极,发生的电极反应式为_______ ,电极b为_______ 极,发生的电极反应式为_______ ,Z溶液可能为_______ (写序号,下同)。
若产生的气体体积比1:1,则阳极的电极反应式为_______ ,Z溶液可能为_______ 。
(2)若通电后出现a电极的质量增加,b电极上有无色无味气体产生,则电极a为_______ 极,发生的电极反应式为_______ ,Z溶液可能为_______ 。
(3)若通电后出现a电极的质量减少,b电极质量增加,且质量变化值相等。则该装置可能为_______ 装置,Z溶液可能为_______ ,a电极反应式为_______ 。

(1)若通电后发现a、b两电极上均有气体产生,且V(a):V(b)=2:1,则电极a为
若产生的气体体积比1:1,则阳极的电极反应式为
(2)若通电后出现a电极的质量增加,b电极上有无色无味气体产生,则电极a为
(3)若通电后出现a电极的质量减少,b电极质量增加,且质量变化值相等。则该装置可能为
您最近一年使用:0次
22-23高二上·全国·课时练习
解题方法
8 . 三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调NiCl2溶液pH至7.5,加入适量硫酸钠后进行电解。电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。以下说法不正确的是
| A.可用铁作阳极材料 |
| B.电解过程中阴极附近溶液的pH升高 |
C.阳极反应方程式为: |
| D.1mol二价镍全部转化为三价镍时,外电路中通过了1mol电子 |
您最近一年使用:0次
22-23高二上·全国·课时练习
名校
9 . 某新型可充电电池,能长时间保持稳定的放电电压,该电池的总反应 。
。
(1)放电时负极反应为___________ ;
(2)充电时Fe(OH)3发生___________ 反应;
(3)放电时电子由___________ 极流向___________ 极;
(4)放电时1 mol K2FeO4发生反应,转移电子数是___________ 。
 。
。(1)放电时负极反应为
(2)充电时Fe(OH)3发生
(3)放电时电子由
(4)放电时1 mol K2FeO4发生反应,转移电子数是
您最近一年使用:0次
22-23高二上·全国·课时练习
10 . 锂离子电池的应用很广,其正极材料可再生利用。某锂离子电池正极材料有钴酸锂(LiCoO2),导电剂乙炔黑和铝箔等。充电时,该锂离子电池负极发生的反应为 ,充放电过程中,正极发生LiCoO2与Li1-xCoO2之间的转化。下列有关说法不正确的是
,充放电过程中,正极发生LiCoO2与Li1-xCoO2之间的转化。下列有关说法不正确的是
 ,充放电过程中,正极发生LiCoO2与Li1-xCoO2之间的转化。下列有关说法不正确的是
,充放电过程中,正极发生LiCoO2与Li1-xCoO2之间的转化。下列有关说法不正确的是A.放电时的负极反应式为: |
| B.钴酸锂(LiCoO2)中钴元素的化合价为+3 |
| C.放电时正极发生LiCoO2转化为Li1-xCoO2的反应 |
| D.放电时锂离子向正极移动 |
您最近一年使用:0次



