解题方法
1 . 某化学兴趣小组同学对电化学原理进行了一系列探究活动。
(1)如图,为某化学兴趣小组依据氧化还原反应:___________ (用离子方程式表示)设计的原电池装置,当导线中通过0.5mol电子的电量时,理论上石墨电极上产生气体体积为___________ L(标准状况下)。

(2)该实验小组的同学发现,用吸管吸出铁片附近溶液少许置于试管中,滴加几滴酚酞试剂,溶液变红,针对这一现象,某同学的假设是:铁电极材料不纯(材料中含有碳杂质),所以发生了___________ 腐蚀(填“吸氧”或“析氢”),试写出使酚酞溶液变红的电极反应式为___________ 。
(3)如图其他条件不变,若将盐桥换成n型铜丝,一段时间后,乙装置中石墨为___________ 极(填“正”、“负”、“阴”或“阳”),乙装置中总反应的离子方程式为___________ ,该反应为___________ (填“自发”或“非自发”)的氧化还原反应。___________ ,产物常用___________ 检验,一段时间后,乙装置中溶液pH___________ (填“变大”、“变小”或“不变”)。
(1)如图,为某化学兴趣小组依据氧化还原反应:

(2)该实验小组的同学发现,用吸管吸出铁片附近溶液少许置于试管中,滴加几滴酚酞试剂,溶液变红,针对这一现象,某同学的假设是:铁电极材料不纯(材料中含有碳杂质),所以发生了
(3)如图其他条件不变,若将盐桥换成n型铜丝,一段时间后,乙装置中石墨为
您最近半年使用:0次
解题方法
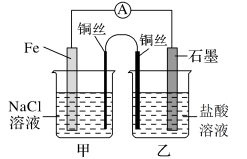
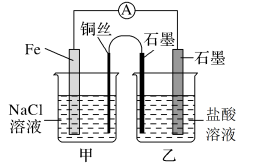
2 . 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题: 溶液,则反应一段时间后:
溶液,则反应一段时间后:
①乙池中阳极的电极反应式是_______ 。
②若要保护金属铁,可将甲池中的C棒换成 棒,则该防护方法称为
棒,则该防护方法称为_______ 。
(2)若两池中电解质溶液均为饱和 溶液:
溶液:
①写出乙池中总反应的离子方程式_______ 。
②甲池中碳极上电极反应式是_______ 。
③若乙池转移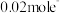 后停止实验,池中电解质溶液体积是
后停止实验,池中电解质溶液体积是 ,则室温下溶液混合均匀后的
,则室温下溶液混合均匀后的
_______ 。

 溶液,则反应一段时间后:
溶液,则反应一段时间后:①乙池中阳极的电极反应式是
②若要保护金属铁,可将甲池中的C棒换成
 棒,则该防护方法称为
棒,则该防护方法称为(2)若两池中电解质溶液均为饱和
 溶液:
溶液:①写出乙池中总反应的离子方程式
②甲池中碳极上电极反应式是
③若乙池转移
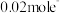 后停止实验,池中电解质溶液体积是
后停止实验,池中电解质溶液体积是 ,则室温下溶液混合均匀后的
,则室温下溶液混合均匀后的
您最近半年使用:0次
3 . 能源、环境与生产生活和社会发展密切相关。
(1)工业上利用CO和H2在催化剂作用下合成甲醇: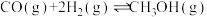 (甲醇结构式
(甲醇结构式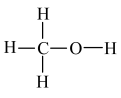 ),已知反应中有关物质的化学键键能数据如下表所示:
),已知反应中有关物质的化学键键能数据如下表所示:
则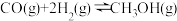
 =
=___________ kJ/mol
(2)以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池。下图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。___________ 极,B极的电极反应式为___________ 。
(3)如图,其中甲池的总反应式为: ,下列说法正确的是
,下列说法正确的是___________ 装置,乙池中石墨电极的名称是___________ 。
②甲池通入氧气的电极反应式为___________ 。
③电解一段时间后,乙池中溶液的pH将___________ (填“增大”“减小”或“不变”)
④丙池中阴极上发生的电极反应为___________ 。
(4)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有 ),实验室利用如图装置模拟该方法:
),实验室利用如图装置模拟该方法:___________ (填“正”或“负”)极,M电极的电极反应式为___________ 。
(1)工业上利用CO和H2在催化剂作用下合成甲醇:
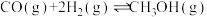 (甲醇结构式
(甲醇结构式 ),已知反应中有关物质的化学键键能数据如下表所示:
),已知反应中有关物质的化学键键能数据如下表所示:| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
则
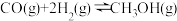
 =
=(2)以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池。下图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。

(3)如图,其中甲池的总反应式为:
 ,下列说法正确的是
,下列说法正确的是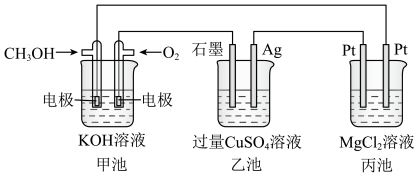
②甲池通入氧气的电极反应式为
③电解一段时间后,乙池中溶液的pH将
④丙池中阴极上发生的电极反应为
(4)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有
 ),实验室利用如图装置模拟该方法:
),实验室利用如图装置模拟该方法: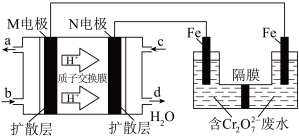
您最近半年使用:0次
名校
解题方法
4 . 某同学利用如图所示装置制作简单的燃料电池。
①电极a的电极反应式是_______________ 。
② 的迁移方向为
的迁移方向为_______________ (填“ ”或“
”或“ ”)。
”)。
③一段时间后,电极b附近的现象是_______________ 。
(2)一段时间后断开K1,闭合K2,电流表的指针偏转。
①电极b的电极反应式是______________ 。
②电极a附近的
___________ (选填“增大”、“减小”或“不变”)。
(3)下列说法中,不正确的是________ (填字母)。
a.通过调节K1、K2可以实现化学能和电能的相互转化
b.若将Na2SO4溶液替换为稀硫酸,闭合K2后,电极反应不变
c.闭合K1,电路中每转移4mol电子,电极a理论上产生的气体在标准状况下的体积为

①电极a的电极反应式是
②
 的迁移方向为
的迁移方向为 ”或“
”或“ ”)。
”)。③一段时间后,电极b附近的现象是
(2)一段时间后断开K1,闭合K2,电流表的指针偏转。
①电极b的电极反应式是
②电极a附近的

(3)下列说法中,不正确的是
a.通过调节K1、K2可以实现化学能和电能的相互转化
b.若将Na2SO4溶液替换为稀硫酸,闭合K2后,电极反应不变
c.闭合K1,电路中每转移4mol电子,电极a理论上产生的气体在标准状况下的体积为

您最近半年使用:0次
名校
5 . Ⅰ.下图装置的盐桥中盛有饱和 琼脂溶液,能够连接两份电解质溶液,形成闭合回路:
琼脂溶液,能够连接两份电解质溶液,形成闭合回路:___________ ,装置工作时,盐桥中的 移向
移向___________ 。(“ 溶液”或“
溶液”或“ 溶液”)
溶液”)
(2)若将盐桥换成n型铜丝,电路中也有电流通过,则左边装置是___________ ,(填“原电池”或“电解池”),则n型铜丝左端为___________ 极,该极电极反应式为:___________ 。
Ⅱ.配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(3) 可以形成多种配离子,如
可以形成多种配离子,如 、
、 、丁二酮肟镍分子(见图)等。
、丁二酮肟镍分子(见图)等。 中
中 键角比
键角比 分子中
分子中 键角
键角___________ (填“大”或“小”)。
②丁二酮肟镍分子内含有的作用力有___________ (填字母)。
a.配位键 b.离子键 c.氢键 d.金属键 e.共价键
(4)关于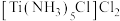 的说法中错误的是
的说法中错误的是___________ 。
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol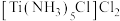 的水溶液中加入足量
的水溶液中加入足量 溶液,产生3mol白色沉淀
溶液,产生3mol白色沉淀
 琼脂溶液,能够连接两份电解质溶液,形成闭合回路:
琼脂溶液,能够连接两份电解质溶液,形成闭合回路: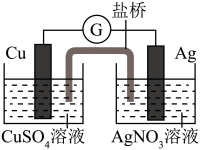
 移向
移向 溶液”或“
溶液”或“ 溶液”)
溶液”)(2)若将盐桥换成n型铜丝,电路中也有电流通过,则左边装置是
Ⅱ.配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(3)
 可以形成多种配离子,如
可以形成多种配离子,如 、
、 、丁二酮肟镍分子(见图)等。
、丁二酮肟镍分子(见图)等。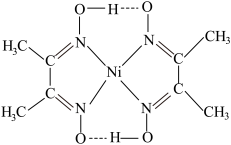
 中
中 键角比
键角比 分子中
分子中 键角
键角②丁二酮肟镍分子内含有的作用力有
a.配位键 b.离子键 c.氢键 d.金属键 e.共价键
(4)关于
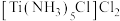 的说法中错误的是
的说法中错误的是A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol
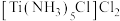 的水溶液中加入足量
的水溶液中加入足量 溶液,产生3mol白色沉淀
溶液,产生3mol白色沉淀
您最近半年使用:0次
解题方法
6 . 含镍废水对环境和人体健康均会造成巨大的影响。某化学小组在实验室设计了以下装置模拟工业含镍废水处理,图中电极均为惰性电极。错误 的是
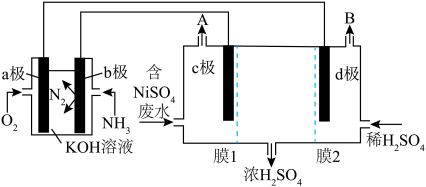
A.a极为正极, 极为阴极 极为阴极 |
B. 极的电极反应为2H2O-4e-=O2+4H+↑ 极的电极反应为2H2O-4e-=O2+4H+↑ |
| C.膜1为阴离子交换膜 |
D.b极消耗22.4LNH3,理论上 极上析出88.5gNi单质 极上析出88.5gNi单质 |
您最近半年使用:0次
解题方法
7 . 可利用电化学的原理回收利用工业废气中的CO2和SO2,实验原理示意图如下。
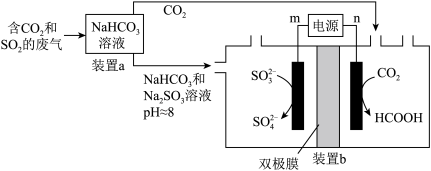
| A.装置b中左边的电极为阳极 |
| B.装置a中溶液的作用是吸收废气中的CO2和SO2 |
C.装置b中右边电极的电极反应式为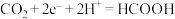 |
D.装置b若采用质子交换膜,每消耗1mol CO2则有2mol  转移 转移 |
您最近半年使用:0次
8 . 钛酸锂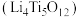 因其独特的尖晶石结构,在嵌入和嵌出锂离子时其结构上存在迁移通道,是一种非常有潜力的负极材料。以钛酸锂为负极材料的一种锂离子二次可充电电池如图所示。下列有关说法正确的是
因其独特的尖晶石结构,在嵌入和嵌出锂离子时其结构上存在迁移通道,是一种非常有潜力的负极材料。以钛酸锂为负极材料的一种锂离子二次可充电电池如图所示。下列有关说法正确的是
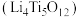 因其独特的尖晶石结构,在嵌入和嵌出锂离子时其结构上存在迁移通道,是一种非常有潜力的负极材料。以钛酸锂为负极材料的一种锂离子二次可充电电池如图所示。下列有关说法正确的是
因其独特的尖晶石结构,在嵌入和嵌出锂离子时其结构上存在迁移通道,是一种非常有潜力的负极材料。以钛酸锂为负极材料的一种锂离子二次可充电电池如图所示。下列有关说法正确的是
A.放电时, 向 向 极移动 极移动 |
B.放电时, 的化合价降低 的化合价降低 |
C. 均位于元素周期表的d区 均位于元素周期表的d区 |
D.充电时, 极的电极反应式: 极的电极反应式: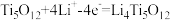 |
您最近半年使用:0次
名校
解题方法
9 . 完成下列问题
(1)如图所示,甲池的总反应式为 ,
,___________ (填“原电池”或“电解池”),写出通入 一极发生电极反应式
一极发生电极反应式___________ 。
②乙池中电解反应的化学方程式为___________ 。
③当甲池中消耗 时,乙池中
时,乙池中 电极上析出固体的质量是
电极上析出固体的质量是___________ 。
(2)高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂,可以用如图所示电解装置制取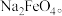 电解一段时间后,
电解一段时间后, 降低的区域在
降低的区域在___________ (填“阴极室”或“阳极室”);阳极电极反应式为:___________ 。 电极上的电极反应式为
电极上的电极反应式为___________ ;
②该装置中使用的是___________ (填“阴”或“阳”)离子交换膜。
(1)如图所示,甲池的总反应式为
 ,
,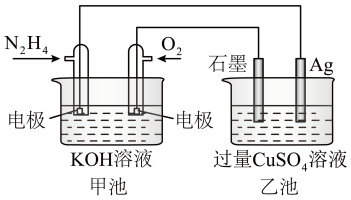
 一极发生电极反应式
一极发生电极反应式②乙池中电解反应的化学方程式为
③当甲池中消耗
 时,乙池中
时,乙池中 电极上析出固体的质量是
电极上析出固体的质量是(2)高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂,可以用如图所示电解装置制取
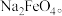 电解一段时间后,
电解一段时间后, 降低的区域在
降低的区域在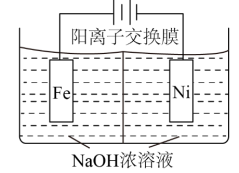
 电极上的电极反应式为
电极上的电极反应式为②该装置中使用的是
您最近半年使用:0次
解题方法
10 . 一种Zn-催化电极(表面锂掺杂了锡纳米粒子)催化制甲酸盐的电化学装置如图所示。下列说法正确的是

| A.放电时,正极电极反应式为:CO2+2e-+H2O=HCOO-+OH- |
| B.充电时,催化电极周围pH升高 |
| C.放电时,锡纳米粒子能提高CO2的平衡转化率 |
| D.充电时,催化电极应与电源的负极相连 |
您最近半年使用:0次



