名校
解题方法
1 . 电化学在生活中有着广泛的应用
I.乙醛酸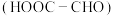 是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
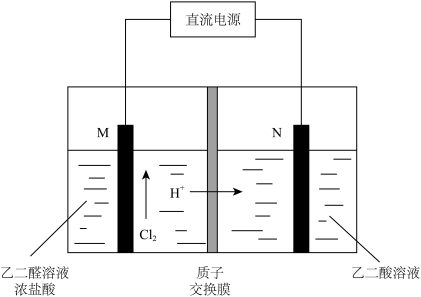
(1)N电极上的电极反应式为__________ 。
(2)若有 通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为
通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为______  。
。
II.某课外活动小组用如图所示装置进行实验,试回答下列问题:
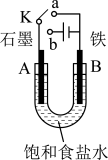
(3)若开始时开关K与a连接,则B极的电极反应式为__________ 。
(4)若开始时开关K与b极连接,则B极的电极反应式为__________ ,总反应的离子方程式为__________ 。
(5)若开始时开关K与b连接,下列说法正确的是______。(填字母)
(6)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
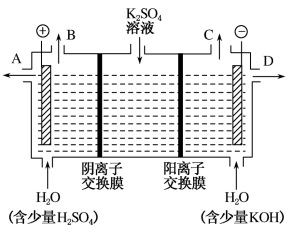
①该电解槽的阳极反应式为__________ 。
②制得的氢氧化钾溶液从出口______ 导出(填“A”“B”“C”或“D”)。
I.乙醛酸
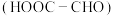 是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
(1)N电极上的电极反应式为
(2)若有
 通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为
通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为 。
。II.某课外活动小组用如图所示装置进行实验,试回答下列问题:

(3)若开始时开关K与a连接,则B极的电极反应式为
(4)若开始时开关K与b极连接,则B极的电极反应式为
(5)若开始时开关K与b连接,下列说法正确的是______。(填字母)
A.溶液中 向A极移动 向A极移动 |
B.从A极处逸出的气体能使湿润的 淀粉试纸变蓝 淀粉试纸变蓝 |
| C.反应一段时间后加适量盐酸可恢复到电解前电解质溶液的浓度 |
D.若标准状况下B极产生 气体,则溶液中转移 气体,则溶液中转移 电子 电子 |

①该电解槽的阳极反应式为
②制得的氢氧化钾溶液从出口
您最近一年使用:0次
名校
解题方法
2 . 根据下图判断,下列说法正确的是
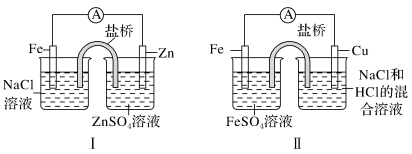

| A.装置Ⅰ和装置Ⅱ中负极反应均是Fe-2e-=Fe2+ |
| B.放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的pH均增大 |
| C.装置Ⅰ和装置Ⅱ中正极反应均是O2+2H2O+4e- =4OH- |
| D.装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动 |
您最近一年使用:0次
2023-01-26更新
|
400次组卷
|
2卷引用:黑龙江省齐齐哈尔三立高中2022-2023学年高一下学期期初考试化学试题
名校
解题方法
3 . 能源、材料、环境和健康等领域与化学息息相关。
(1)如图为利用甲烷燃料电池电解AlCl3溶液的装置,电极材料均为石墨。秋林同学用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。

①x为图2电池的_______ (填“正”“负”“阴”“阳”)极;图1电池工作时,OH-向_______ (填“a”或“b”)极移动。
②a极电极反应式为_______ 。
③每消耗3molCH4,理论上生成_______ g白色沉淀。
(2)A、B、C、D四种物质之间有如图所示的转化关系。已知:A是空气中的主要成分之一,B、C、D均为化合物,且C为一种红棕色气体。
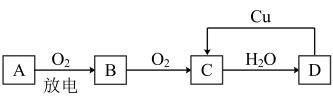
写出D→C的化学方程式:_______ ;其中D表现出_______ 性。
(3)一种在恒温、恒定气流流速下,催化氧化HCl生产Cl2工艺的主要反应机理如图所示。
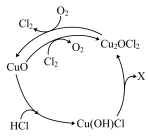
①X为_______ 。
②总反应化学方程式式为_______ 。
(1)如图为利用甲烷燃料电池电解AlCl3溶液的装置,电极材料均为石墨。秋林同学用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。

①x为图2电池的
②a极电极反应式为
③每消耗3molCH4,理论上生成
(2)A、B、C、D四种物质之间有如图所示的转化关系。已知:A是空气中的主要成分之一,B、C、D均为化合物,且C为一种红棕色气体。

写出D→C的化学方程式:
(3)一种在恒温、恒定气流流速下,催化氧化HCl生产Cl2工艺的主要反应机理如图所示。

①X为
②总反应化学方程式式为
您最近一年使用:0次
名校
4 . 有机电化学合成是目前公认的一种绿色可持续性合成策略,电化学合成1,2-二氯乙烷的装置如图。
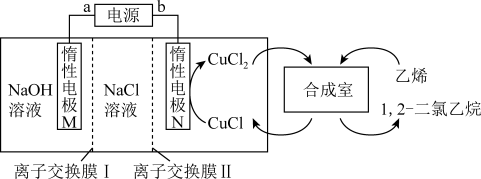
下列说法错误的是

下列说法错误的是
| A.a为负极,离子交换膜1为阳离子交换膜 |
B.M极发生反应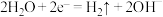 |
C.电路中每通过1mol 理论上消耗14g乙烯 理论上消耗14g乙烯 |
D.随电解进行 与 与 需及时补充 需及时补充 |
您最近一年使用:0次
2023-01-13更新
|
268次组卷
|
2卷引用:福建省永春第一中学2023届高三下学期期初考试化学试题
名校
解题方法
5 . 某课题组以纳米Fe2O3作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图)。下列说法正确的是


| A.放电时,金属锂和石墨的复合材料作电池的负极,纳米Fe2O3作电池的正极 |
| B.放电时,正极的电极反应为Fe2O3+6Li++6e-=2Fe+3Li2O |
| C.该电池可以用水溶液作电解质溶液 |
| D.充电完成后,电池被磁铁吸引 |
您最近一年使用:0次
2023-01-10更新
|
112次组卷
|
2卷引用:江西省丰城中学2022-2023学年高二下学期入学考试化学试题
名校
解题方法
6 . 高铁酸盐在能源、环保等领域有着广泛的应用。某研究小组用电解法制取 ,装置示意图如下。
,装置示意图如下。
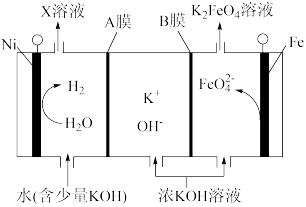
下列说法不正确 的是
 ,装置示意图如下。
,装置示意图如下。
下列说法
| A.Ni电极与外接直流电源的负极相连 |
| B.KOH溶液可以循环使用 |
C.Fe电极上的电极反应为 |
D.A膜是阴离子交换膜,外电路中转移1 mol  ,有1 mol ,有1 mol  通过A膜 通过A膜 |
您最近一年使用:0次
2023-01-04更新
|
267次组卷
|
2卷引用:北京市第九中学2023-2024学年高二下学期2月开学考化学试题
名校
解题方法
7 . LiOH是生产航空航天润滑剂的原料。清华大学首创三室膜电解法制备氢氧化锂,其模拟装置如图所示。下列有关说法正确的是


| A.X极的电极反应式为2H2O-4e=4H+O2↑ |
| B.a极为电源的负极,Y极上发生氧化反应 |
| C.膜1为阳离子交换膜,膜2为阴离子交换膜 |
| D.每转移2mol电子,理论上生成52gLiOH |
您最近一年使用:0次
2023-01-02更新
|
515次组卷
|
2卷引用:福建省漳州市华安县第一中学2023-2024学年高三上学期开学考试化学试题
解题方法
8 . 已知铅蓄电池的工作原理为Pb+PbO2+2H2SO4 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4mol电子时铁电极的质量减少11.2g。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4mol电子时铁电极的质量减少11.2g。请回答下列问题。
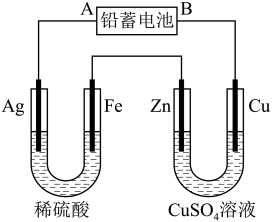
(1)A是铅蓄电池的_______ 极,铅蓄电池正极反应式为_______ ,放电过程中电解液的密度_______ (填“减小”、“增大”或“不变”)。
(2)Ag电极的电极反应式是_______ ,该电极的电极产物共_______ g。
(3)Cu电极的电极反应式是_______ ,CuSO4溶液的浓度_______ (填“减小”、“增大”或“不变”)
(4)如图表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示_______ 。
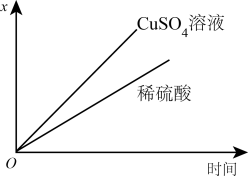
a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4mol电子时铁电极的质量减少11.2g。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4mol电子时铁电极的质量减少11.2g。请回答下列问题。
(1)A是铅蓄电池的
(2)Ag电极的电极反应式是
(3)Cu电极的电极反应式是
(4)如图表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示

a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
您最近一年使用:0次
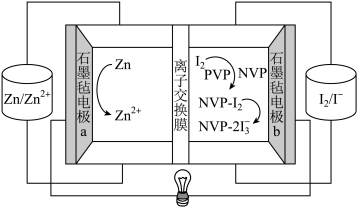
9 . 2022年7月,中科院在锌碘液流可充电电池领域研究中取得重要进展。该研究引入了聚乙烯吡咯烷酮(PVP),其单体为NVP,NVP可结合I2,经一系列变化生成可溶性聚碘配合物NVP-2I ,有效提高锌碘液流电池碘正极容量,避免了电池改进前I2+I-=I
,有效提高锌碘液流电池碘正极容量,避免了电池改进前I2+I-=I 导致I-利用率降低,其工作原理如图所示。下列说法不正确的是
导致I-利用率降低,其工作原理如图所示。下列说法不正确的是
 ,有效提高锌碘液流电池碘正极容量,避免了电池改进前I2+I-=I
,有效提高锌碘液流电池碘正极容量,避免了电池改进前I2+I-=I 导致I-利用率降低,其工作原理如图所示。下列说法不正确的是
导致I-利用率降低,其工作原理如图所示。下列说法不正确的是
| A.充电时,a极为阴极 |
| B.将该电池用于铁制品的腐蚀防护,应将电极b与铁制品相连 |
C.电池改进前,放电时1molI ,转化为I-,转移2mol电子 ,转化为I-,转移2mol电子 |
D.放电时,b极反应:2I2+NVP-I2+2e-=NVP-2I |
您最近一年使用:0次
2022-12-03更新
|
439次组卷
|
4卷引用:重庆市南开中学校2022-2023学年高二下学期开学考试化学试题
重庆市南开中学校2022-2023学年高二下学期开学考试化学试题湖湘名校教育联合体五市十校教研教改共同体2022-2023学年高三第二次大联考化学试题(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(11-16)(已下线)专题卷16 离子隔膜在电化学中的应用-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)
名校
解题方法
10 . 填空。
(1)某课外活动小组同学用如图装置(M、N为外电源的两个电极)进行实验,试回答下列问题:
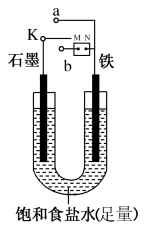
①若开始时开关K与a连接,则铁发生电化学腐蚀中的_____ 腐蚀。请写出正极反应式:____ 。
②若开始时开关K与b连接时,两极均有气体产生,则铁电极为______ 极(填“阴”或“阳”),该电极上发生的电极反应式为_______ ,总反应的离子方程式为_______ 。
③当电路中转移0.2mol电子时,100ml溶液中,NaOH溶液的浓度是_______ mol/L
(2)该小组同学设想,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠。
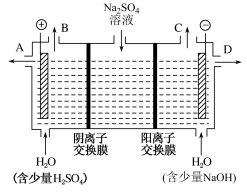
B出口导出的气体是_______ ,制得的氢氧化钠溶液从出口_______ (填“A”、“B”、“C”或“D”)导出。通过阴离子交换膜的离子数_______ (填“>”、“<”或“=”)通过阳离子交换膜的离子数。
(1)某课外活动小组同学用如图装置(M、N为外电源的两个电极)进行实验,试回答下列问题:

①若开始时开关K与a连接,则铁发生电化学腐蚀中的
②若开始时开关K与b连接时,两极均有气体产生,则铁电极为
③当电路中转移0.2mol电子时,100ml溶液中,NaOH溶液的浓度是
(2)该小组同学设想,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠。

B出口导出的气体是
您最近一年使用:0次



