电化学在生活中有着广泛的应用
I.乙醛酸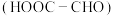 是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
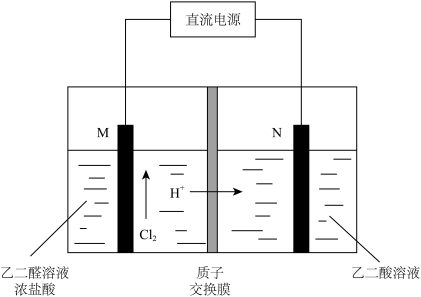
(1)N电极上的电极反应式为__________ 。
(2)若有 通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为
通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为______  。
。
II.某课外活动小组用如图所示装置进行实验,试回答下列问题:
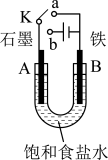
(3)若开始时开关K与a连接,则B极的电极反应式为__________ 。
(4)若开始时开关K与b极连接,则B极的电极反应式为__________ ,总反应的离子方程式为__________ 。
(5)若开始时开关K与b连接,下列说法正确的是______。(填字母)
(6)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
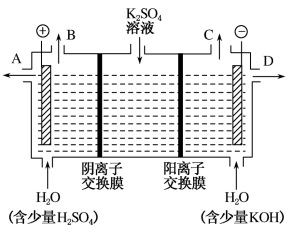
①该电解槽的阳极反应式为__________ 。
②制得的氢氧化钾溶液从出口______ 导出(填“A”“B”“C”或“D”)。
I.乙醛酸
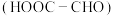 是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
(1)N电极上的电极反应式为
(2)若有
 通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为
通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为 。
。II.某课外活动小组用如图所示装置进行实验,试回答下列问题:

(3)若开始时开关K与a连接,则B极的电极反应式为
(4)若开始时开关K与b极连接,则B极的电极反应式为
(5)若开始时开关K与b连接,下列说法正确的是______。(填字母)
A.溶液中 向A极移动 向A极移动 |
B.从A极处逸出的气体能使湿润的 淀粉试纸变蓝 淀粉试纸变蓝 |
| C.反应一段时间后加适量盐酸可恢复到电解前电解质溶液的浓度 |
D.若标准状况下B极产生 气体,则溶液中转移 气体,则溶液中转移 电子 电子 |

①该电解槽的阳极反应式为
②制得的氢氧化钾溶液从出口
更新时间:2023-03-22 21:35:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】如图是一个化学过程的示意图,回答下列问题:
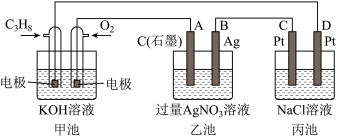
(1)甲池是_______ 装置,电极B的名称是_______ 。
(2)甲装置中通入 的电极反应
的电极反应_______ ,丙装置中D极的产物是_______ (写化学式)。
(3)一段时间,当乙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的
_______ 。(已知:NaCl溶液足量,电解后溶液体积为200mL)。乙池的PH值将_______ (填“变大”、“变小”或“不变”)
(4)若要使乙池恢复电解前的状态,应向乙池中加入_______ (写物质化学式)。

(1)甲池是
(2)甲装置中通入
 的电极反应
的电极反应(3)一段时间,当乙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的

(4)若要使乙池恢复电解前的状态,应向乙池中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电解原理在化学工业中有着广泛的应用。
(1)如图,其中a是电解液,X、Y是两块电极板。若X、Y是惰性电极,a是CuSO4溶液,则电解时的化学方程式为___________ 。
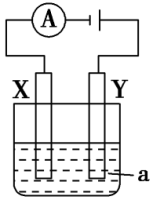
通电一段时间后,向烧杯中的电解质溶液中加入0.2 mol CuO粉末,电解质溶液恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为___________ ;当X、Y分别是铁和铜,a仍是CuSO4溶液,则Y极的电极反应式为___________ 。
(2)已知+2价的铁的化合物通常具有较强的还原性,易被氧化。实验室用亚铁盐溶液与烧碱反应很难制得白色纯净的Fe(OH)2沉淀,但是若用电解的方法却可以较易制得纯净的Fe(OH)2沉淀。制备装置如图所示,其中a、b两电极材料分别为铁和石墨。

①a电极上的反应式为___________ 。
②电解液d最好选___________ (填字母,下同)。
A.纯水 B.NaOH溶液 C.AgNO3溶液 D.H2SO4溶液
③液体c为___________ 。
A.苯 B.醋酸 C.四氯化碳 D.酒精
(1)如图,其中a是电解液,X、Y是两块电极板。若X、Y是惰性电极,a是CuSO4溶液,则电解时的化学方程式为

通电一段时间后,向烧杯中的电解质溶液中加入0.2 mol CuO粉末,电解质溶液恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为
(2)已知+2价的铁的化合物通常具有较强的还原性,易被氧化。实验室用亚铁盐溶液与烧碱反应很难制得白色纯净的Fe(OH)2沉淀,但是若用电解的方法却可以较易制得纯净的Fe(OH)2沉淀。制备装置如图所示,其中a、b两电极材料分别为铁和石墨。

①a电极上的反应式为
②电解液d最好选
A.纯水 B.NaOH溶液 C.AgNO3溶液 D.H2SO4溶液
③液体c为
A.苯 B.醋酸 C.四氯化碳 D.酒精
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)如图所示,某同学设计了一个燃料电池探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 为阳离子交换膜。(甲醚
为阳离子交换膜。(甲醚 )
)
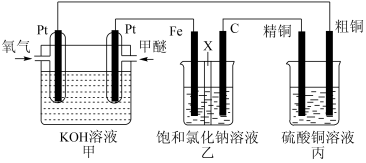
①写出甲装置中通入甲醚一极的电极反应式:___________ 。
②写出乙装置中的总反应的化学方程式:___________ 。
③电解一段时间后,丙装置中精铜质量增加9.6g,则消耗甲醚(标准状况下)体积为___________ mL。
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。(提示:放电顺序SO >OH-)
>OH-)

①图中b极要连接电源的___________ (填“正”或“负”)极。
②SO 放电的电极反应式为
放电的电极反应式为___________ 。
(1)如图所示,某同学设计了一个燃料电池探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
 为阳离子交换膜。(甲醚
为阳离子交换膜。(甲醚 )
)
①写出甲装置中通入甲醚一极的电极反应式:
②写出乙装置中的总反应的化学方程式:
③电解一段时间后,丙装置中精铜质量增加9.6g,则消耗甲醚(标准状况下)体积为
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。(提示:放电顺序SO
 >OH-)
>OH-)
①图中b极要连接电源的
②SO
 放电的电极反应式为
放电的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)依据反应:2Ag+(aq)+Cu(s) =Cu2+(aq)+2Ag(s)设计的原电池如下图所示。

①电极X的材料是___________ ;Y溶液可以是___________ ;
②银电极上发生的电极反应式是___________ 。
③在电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向CuSO4溶液一端扩散的离子是___________ (填离子符号)。
(2)金属腐蚀一般可分为化学腐蚀和电化学腐蚀,可以采用电化学手段进行防腐。
①洗过的铁锅,未及时擦干容易生锈。写出铁锅生锈过程的正极反应式___________ 。
②为了减缓某水库钢闸门被腐蚀的速率,可以采用下图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用___________ (填写字母序号)。
A.铜 B.钠 C.锌 D.石墨
③图乙所示方案也可以减缓钢闸门的腐蚀速率,则钢闸门应连接直流电源的___________ 极,钢闸门上发生的电极反应式为___________ 。


①电极X的材料是
②银电极上发生的电极反应式是
③在电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向CuSO4溶液一端扩散的离子是
(2)金属腐蚀一般可分为化学腐蚀和电化学腐蚀,可以采用电化学手段进行防腐。
①洗过的铁锅,未及时擦干容易生锈。写出铁锅生锈过程的正极反应式
②为了减缓某水库钢闸门被腐蚀的速率,可以采用下图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
③图乙所示方案也可以减缓钢闸门的腐蚀速率,则钢闸门应连接直流电源的

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
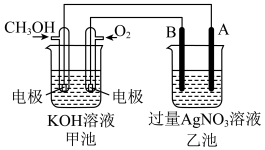
【推荐2】某电化学原理的示意图如图。填写下列空白: 的电极为
的电极为___________ 极,通入 的电极上发生的电极反应为
的电极上发生的电极反应为___________ ;工作过程中,甲池溶液的碱性会___________ (填“增强”、“减弱”或“不变”,下同)。若将甲池中的 溶液换成稀硫酸,工作过程中,甲池溶液的酸性会
溶液换成稀硫酸,工作过程中,甲池溶液的酸性会___________ 。
(2)若乙池中A为石墨电极,则A作___________ 极,该电极的电极反应式为___________ ;若乙池中A为铁电极,当铁电极的质量增加 时,理论上甲池中消耗的氧气在标准状况下的体积为
时,理论上甲池中消耗的氧气在标准状况下的体积为___________ L。
(3)若将乙池设计为电解精炼铜的装置,则___________ (填“A”或“B”,下同)极为粗铜;若将乙池改为电镀装置,则___________ 极为待镀金属制品。
(4)若将乙池中的硝酸银溶液换为硫酸铜溶液,通电一段时间后,向所得溶液中加入 碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为
碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为___________  。
。
 的电极为
的电极为 的电极上发生的电极反应为
的电极上发生的电极反应为 溶液换成稀硫酸,工作过程中,甲池溶液的酸性会
溶液换成稀硫酸,工作过程中,甲池溶液的酸性会(2)若乙池中A为石墨电极,则A作
 时,理论上甲池中消耗的氧气在标准状况下的体积为
时,理论上甲池中消耗的氧气在标准状况下的体积为(3)若将乙池设计为电解精炼铜的装置,则
(4)若将乙池中的硝酸银溶液换为硫酸铜溶液,通电一段时间后,向所得溶液中加入
 碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为
碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2021年我国自主研发的神舟十三号载人飞船成功进入太空,其轨道舱和推进舱使用太阳能电池阵——镍镉蓄电池组系统,返回舱使用的是银锌蓄电池组。
(1)飞船在光照区运行时,太阳能电池帆板将____ 能转化为____ 能。除供给飞船使用放电,多余部分用镍镉蓄电池储存起来,其工作原理为Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2。下列有关镍镉电池的说法正确的是
Cd(OH)2+2Ni(OH)2。下列有关镍镉电池的说法正确的是___ 。
A.放电时负极反应式为Cd+2OH--2e-=Cd(OH)2
B.放电时电子由镍电极经导线流向镉电极
C.充电时阳极反应式为Ni(OH)2+OH--2e-=NiOOH+H2O
D.充电时电解质溶液中的OH-移向镉电极
(2)返回舱使用的是银锌蓄电池组,其工作原理为:Zn+Ag2O+H2O 2Ag+Zn(OH)2。
2Ag+Zn(OH)2。
①其负极的电极材料为____ ,负极反应类型为____ 。
②在电池使用的过程中,电解质溶液中KOH的物质的量浓度____ (填“增大”、“减小”或“不变”)。
③当电池工作时通过电路对外提供了1mol电子,则正极质量减轻____ g。
(1)飞船在光照区运行时,太阳能电池帆板将
 Cd(OH)2+2Ni(OH)2。下列有关镍镉电池的说法正确的是
Cd(OH)2+2Ni(OH)2。下列有关镍镉电池的说法正确的是A.放电时负极反应式为Cd+2OH--2e-=Cd(OH)2
B.放电时电子由镍电极经导线流向镉电极
C.充电时阳极反应式为Ni(OH)2+OH--2e-=NiOOH+H2O
D.充电时电解质溶液中的OH-移向镉电极
(2)返回舱使用的是银锌蓄电池组,其工作原理为:Zn+Ag2O+H2O
 2Ag+Zn(OH)2。
2Ag+Zn(OH)2。①其负极的电极材料为
②在电池使用的过程中,电解质溶液中KOH的物质的量浓度
③当电池工作时通过电路对外提供了1mol电子,则正极质量减轻
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】将0.3molNaCl固体与0.1molCuSO4•5H2O固体混合溶于水,配成1000mL混合液.然后取出200mL溶液,用石墨作电极,通电一段时间.电解过程分为三个阶段试回答:
(1)其中第一阶段发生的电解反应的离子方程式为____ 。
(2)电解的最后一个阶段,阴极上发生的电极反应式变为_____ 。
(3)若Cl-正好全部变为氯气逸出时,阴极上产生气体的体积____ L(标准状况下)。
(1)其中第一阶段发生的电解反应的离子方程式为
(2)电解的最后一个阶段,阴极上发生的电极反应式变为
(3)若Cl-正好全部变为氯气逸出时,阴极上产生气体的体积
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】甲、乙两池电极材料都是铁棒与碳棒(如图),乙池箭头方向为电子移动方向。请回答:
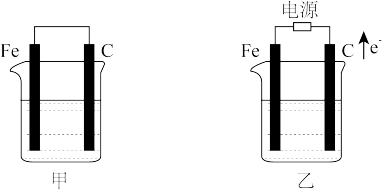
(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的_________ 棒;乙池中的________ 棒。
②在乙池中阳极的电极反应是__________ 。
(2)若两池中均盛放滴加少量酚酞的饱和NaCl溶液。
①甲池中的铁容易发生腐蚀,该腐蚀属于电化学腐蚀中的_________ 腐蚀。
②测得乙池中有0.2mol电子发生转移,则标准状况下理论共有_________ L气体生成。

(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的
②在乙池中阳极的电极反应是
(2)若两池中均盛放滴加少量酚酞的饱和NaCl溶液。
①甲池中的铁容易发生腐蚀,该腐蚀属于电化学腐蚀中的
②测得乙池中有0.2mol电子发生转移,则标准状况下理论共有
您最近一年使用:0次




