名校
1 . 氧化和还原是认识物质性质、分析化学变化的重要视角之一,对生产、生活乃至生命活动中有着十分重要的作用。
(1)下列物质间的转化,需要加入氧化剂才能实现的是_____。
(2)下列溶液中的离子因发生氧化还原反应而不能大量共存的是_____。
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2
①配平下列化学方程式并标出电子转移方向和个数。_____
_____NaIO3+_____NaHSO3—_____I2+_____Na2SO4+_____H2SO4+_____H2O
②在该反应中NaHSO3体现_____ (填“氧化性”或“还原性”),I2为_____ (填“氧化产物”或“还原产物”)。
③已知: 、I2、I-、
、I2、I-、 和一些未知物组成的一个氧化还原反应,其中
和一些未知物组成的一个氧化还原反应,其中 是氧化产物,该反应中还原性
是氧化产物,该反应中还原性
_____ I-(填“>”或“<”),写出该反应的化学方程式_____ 。
化学能与电能之间的转化,是能量转化的重要形式之一,对于生产与生活有很多。

(4)汽车的启动电源常用铅酸蓄电池。其结构如图所示,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4+2H2O。根据此反应判断下列叙述中正确的是_____。
(5)港珠澳大桥设计寿命120年,对桥体钢构件采用了多种防腐方法。下列分析错误的是_____。
(6)用如图装置可以模拟铁的电化学防护,下列说法不正确的是_____。

(7)如图是乙醇燃料电池工作时的示意图,乙池中M、N两个电极的材料是石墨和铁中的一种,工作时M、N两个电极的质量都不减少
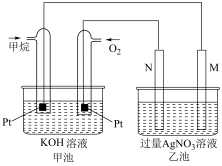
①甲池中通入乙醇的铂电极名称是_____ (选填“正极”、“负极”、“阴极”、“阳极”),通入O2的铂电极反应式为_____ 。
②乙池属于_____ (填“原电池”或“电解池”),工作时,乙池中电子流出的电极是_____ (选填“M”或N”);
③若乙池中某电极析出金属银4.32g时,甲池中理论上消耗氧气为_____ L(标况下);
④若用电解方法精炼粗铜,乙池电解液选用CuSO4溶液,则N电极的材料是_____ (选填“粗铜”或“精铜”),反应一段时间以后,电解液溶液的浓度_____ 。(选填“增大”、“减小”“不变”)
(1)下列物质间的转化,需要加入氧化剂才能实现的是_____。
| A.NH3→NO | B.Fe2O3→Fe |
| C.KClO3→Cl2 | D.H2SO4→SO2 |
(2)下列溶液中的离子因发生氧化还原反应而不能大量共存的是_____。
A.Fe2+、H+、 、 、 |
B.Cu2+、Al3+、 、Cl- 、Cl- |
C.K+、Al3+、OH-、 |
D.Ba2+、Na+、 、ClO- 、ClO- |
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2
①配平下列化学方程式并标出电子转移方向和个数。
_____NaIO3+_____NaHSO3—_____I2+_____Na2SO4+_____H2SO4+_____H2O
②在该反应中NaHSO3体现
③已知:
 、I2、I-、
、I2、I-、 和一些未知物组成的一个氧化还原反应,其中
和一些未知物组成的一个氧化还原反应,其中 是氧化产物,该反应中还原性
是氧化产物,该反应中还原性
化学能与电能之间的转化,是能量转化的重要形式之一,对于生产与生活有很多。

(4)汽车的启动电源常用铅酸蓄电池。其结构如图所示,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4+2H2O。根据此反应判断下列叙述中正确的是_____。
| A.PbO2是电池的负极 |
| B.Pb是负极 |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
(5)港珠澳大桥设计寿命120年,对桥体钢构件采用了多种防腐方法。下列分析错误的是_____。
| A.防腐原理主要是避免发生反应:2Fe+O2+2H2O=2Fe(OH)2 |
| B.钢构件表面喷涂环氧树脂涂层,是为了隔绝空气、水等防止形成原电池 |
| C.采用外加电流的阴极保护时需外接镁、锌等作辅助阳极 |
| D.钢构件可采用不锈钢材料以减缓电化学腐蚀 |
(6)用如图装置可以模拟铁的电化学防护,下列说法不正确的是_____。

| A.若X为碳棒,开关K置于A处时,铁电极反应2H2O+2e-=H2+2OH- |
| B.若X为碳棒,开关K置于A处可以减缓铁的腐蚀 |
| C.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀 |
| D.若X为锌棒,开关K置于B处时,铁电极反应为2H++2e-=H2 |
(7)如图是乙醇燃料电池工作时的示意图,乙池中M、N两个电极的材料是石墨和铁中的一种,工作时M、N两个电极的质量都不减少

①甲池中通入乙醇的铂电极名称是
②乙池属于
③若乙池中某电极析出金属银4.32g时,甲池中理论上消耗氧气为
④若用电解方法精炼粗铜,乙池电解液选用CuSO4溶液,则N电极的材料是
您最近一年使用:0次
2 . 电化学原理有着重要的应用。
(1)探究电化学反应的规律
某研究小组将两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验装置如图所示。
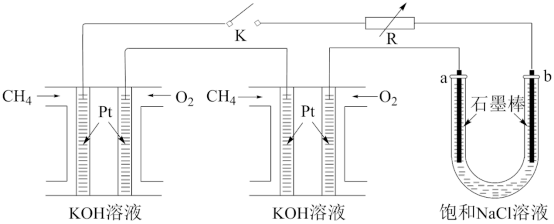
①甲烷燃料电池工作时,负极上通入的气体为____ (填化学式);闭合开关K后a、b电极上均有气体产生,其中a电极上得到的气体为____ (填化学式)。
②若每个电池甲烷通入量均为1L(标准状况),且反应完全,则理论上最多能产生氯气的体积为____ L(标准状况)。
(2)探究氧化还原反应的规律
为探究NaHSO3溶液与CuSO4溶液反应时,Cl-对反应的影响,设计如图实验。
①实验乙中右边烧杯电极的反应式为____ 。
②已知E为电池电动势【又称理论电压,为两个电极电位之差,即E=E(+)-E(-)】,根据实验可知,甲电池与乙电池相比较,E甲____ E乙(填“>”、“<”或“=”)。
③从氧化还原反应的角度分析,Cl-对反应的影响为____ (填选项字母)。
A.增强了Cu2+的氧化性 B.减弱了Cu2+氧化性
C.增强了HSO 的还原性 D.减弱了HSO
的还原性 D.减弱了HSO 的还原性
的还原性
(1)探究电化学反应的规律
某研究小组将两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验装置如图所示。

①甲烷燃料电池工作时,负极上通入的气体为
②若每个电池甲烷通入量均为1L(标准状况),且反应完全,则理论上最多能产生氯气的体积为
(2)探究氧化还原反应的规律
为探究NaHSO3溶液与CuSO4溶液反应时,Cl-对反应的影响,设计如图实验。
| 编号 | 甲 | 乙 |
| 实验 |  | 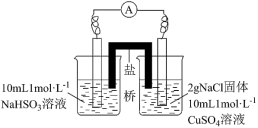 |
| 现象 | 电流计发生较小偏转,3min时无明显现象 | 电流计发生明显偏转,30s时,左边烧杯石墨电极上产生气体;右边烧杯石墨电极上产生白色沉淀(经检验为CuCl) |
①实验乙中右边烧杯电极的反应式为
②已知E为电池电动势【又称理论电压,为两个电极电位之差,即E=E(+)-E(-)】,根据实验可知,甲电池与乙电池相比较,E甲
③从氧化还原反应的角度分析,Cl-对反应的影响为
A.增强了Cu2+的氧化性 B.减弱了Cu2+氧化性
C.增强了HSO
 的还原性 D.减弱了HSO
的还原性 D.减弱了HSO 的还原性
的还原性
您最近一年使用:0次
3 . 高锰酸钾是一种常用的消毒剂和氧化剂。回答下列问题:
实验(一):电解法制备 。
。
以石墨、铜为电极,电解 溶液制备
溶液制备 溶液,装置如图所示。
溶液,装置如图所示。

(1)电解过程中,Cu极附近电解质溶液的pH___________ (填“升高”“降低”或“不变”)。阳极的电极反应式为___________ 。
(2)铜极、石墨极能否互换并简述理由:___________ 。
实验(二):探究 和
和 氧化性强弱。装置如图所示。
氧化性强弱。装置如图所示。
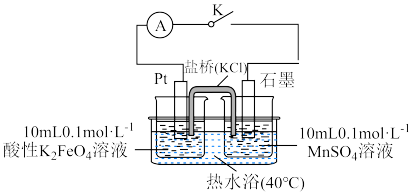
关闭开关K,观察到左烧杯中紫红色溶液变为浅黄色,右烧杯中无色溶液变为紫红色。
(3)关闭K,盐桥中___________ 向左烧杯迁移。盐桥的主要作用是___________ 。
(4)正极反应式为___________ ,实验结论是氧化性:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
实验(三):探究影响草酸和酸性 溶液反应的因素(
溶液反应的因素( ,
,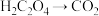 )。
)。
为了探究外界条件改变对反应速率的影响,设计如下实验方案:
(5)通过实验①、②可探究___________ 的改变对反应速率的影响。
(6)在一定 溶液中加入适量硫酸,再加入一定量草酸溶液,产生
溶液中加入适量硫酸,再加入一定量草酸溶液,产生 体积(同温同压)与反应时间的关系如图所示(水浴温度保持35℃)。
体积(同温同压)与反应时间的关系如图所示(水浴温度保持35℃)。
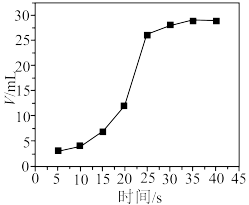
 时间段反应速率突增,其原因可能是
时间段反应速率突增,其原因可能是___________ 。
实验(一):电解法制备
 。
。以石墨、铜为电极,电解
 溶液制备
溶液制备 溶液,装置如图所示。
溶液,装置如图所示。
(1)电解过程中,Cu极附近电解质溶液的pH
(2)铜极、石墨极能否互换并简述理由:
实验(二):探究
 和
和 氧化性强弱。装置如图所示。
氧化性强弱。装置如图所示。
关闭开关K,观察到左烧杯中紫红色溶液变为浅黄色,右烧杯中无色溶液变为紫红色。
(3)关闭K,盐桥中
(4)正极反应式为

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。实验(三):探究影响草酸和酸性
 溶液反应的因素(
溶液反应的因素( ,
,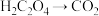 )。
)。为了探究外界条件改变对反应速率的影响,设计如下实验方案:
| 实验 序号 | 实验温度/℃ |  溶液(含硫酸) 溶液(含硫酸) |  溶液 溶液 |  | 溶液颜色褪至无色时所需时间/s | ||
 |  |  |  |  | |||
| ① | 20 | 2 | 0.02 | 5 | 0.1 | 5 |  |
| ② | 20 | 2 | 0.02 | 4 | 0.1 | 6 | 10 |
| ③ | 40 | 2 | 0.02 | 4 | 0.1 | 6 |  |
(5)通过实验①、②可探究
(6)在一定
 溶液中加入适量硫酸,再加入一定量草酸溶液,产生
溶液中加入适量硫酸,再加入一定量草酸溶液,产生 体积(同温同压)与反应时间的关系如图所示(水浴温度保持35℃)。
体积(同温同压)与反应时间的关系如图所示(水浴温度保持35℃)。
 时间段反应速率突增,其原因可能是
时间段反应速率突增,其原因可能是
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
I.某小组研究Na2S溶液与KMnO4溶液反应,探究过程如下。
资料:单质硫可溶于过量硫化钠溶液,Na2S2溶液呈淡黄色。
(1)根据实验可知,Na2S具有_______ 性。
(2)甲同学预测实验I中S2- 被氧化成SO 。
。
①根据实验现象,乙同学认为甲的预测不合理,理由是_______ 。
②乙同学取实验I中少量溶液进行实验,检测到有SO ,得出S2- 被氧化成SO
,得出S2- 被氧化成SO 的结论,丙同学否定了该结论,理由是
的结论,丙同学否定了该结论,理由是_______ 。
③同学们经讨论后,设计了如下实验,证实该条件下MnO 的确可以将S2- 氧化成SO
的确可以将S2- 氧化成SO 。
。
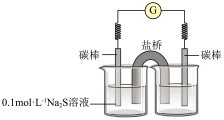
右侧烧杯中的溶液是____ ;连通后电流计指针偏转,一段时间后,____ (填操作和现象)。
II.甲烷和甲醇的燃料电池具有广阔的开发和应用前景。
(3)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC的工作原理如图所示:
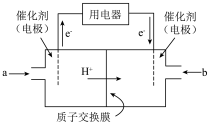
通入a物质的电极是原电池的_______ (填“正”或“负”)极,其电极反应式为_______ 。
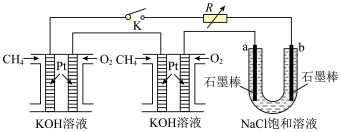
(4)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示U形管中氯化钠溶液的体积为800mL。闭合K后,若每个电池中甲烷通入量为0.224L(标准状况),且反应完全,则理论上通过电解池的电量为_______ (法拉第常数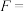
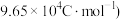 ,若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
,若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为_______ (假设反应后溶液体积不变)。
I.某小组研究Na2S溶液与KMnO4溶液反应,探究过程如下。
| 实验序号 | I | Ⅱ |
| 实验过程 | 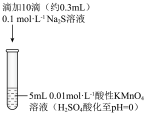 |  |
| 实验现象 | 紫色变浅(pH>1),生成棕褐色沉 淀(MnO2) | 溶液呈淡黄色(pH≈8),生成浅粉色沉淀(MnS) |
资料:单质硫可溶于过量硫化钠溶液,Na2S2溶液呈淡黄色。
(1)根据实验可知,Na2S具有
(2)甲同学预测实验I中S2- 被氧化成SO
 。
。①根据实验现象,乙同学认为甲的预测不合理,理由是
②乙同学取实验I中少量溶液进行实验,检测到有SO
 ,得出S2- 被氧化成SO
,得出S2- 被氧化成SO 的结论,丙同学否定了该结论,理由是
的结论,丙同学否定了该结论,理由是③同学们经讨论后,设计了如下实验,证实该条件下MnO
 的确可以将S2- 氧化成SO
的确可以将S2- 氧化成SO 。
。
右侧烧杯中的溶液是
II.甲烷和甲醇的燃料电池具有广阔的开发和应用前景。
(3)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC的工作原理如图所示:

通入a物质的电极是原电池的
(4)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示U形管中氯化钠溶液的体积为800mL。闭合K后,若每个电池中甲烷通入量为0.224L(标准状况),且反应完全,则理论上通过电解池的电量为
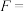
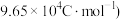 ,若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
,若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
您最近一年使用:0次
名校
解题方法
5 . 结合所学知识,按要求回答问题。
(1)按要求写出电极反应式
①碱性锌锰电池的总反应为Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,写出正极反应式___________ 。
②将2FeCl3+2KI=I2+2FeCl2+2KCl设计成双液电池:正极烧杯中盛放的溶液为___________ ,电池负极的电极反应式为___________ 。
(2)如图是以石墨为电极,电解MgCl2溶液的装置:
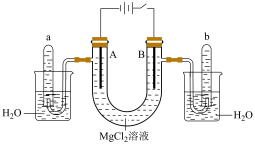
①电解时,A电极发生的电极反应为___________ 。
②检验b管中气体的方法是___________ 。
(3)某同学设计了如下图所示装置,用氢氧燃料电池作为电源探究粗铜精炼原理,根据要求回答问题:
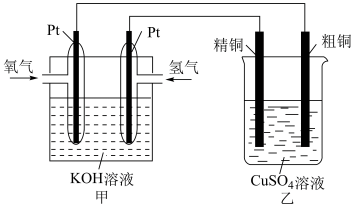
①甲装置中通入氧气的电极为___________ (填“正极”或“负极”),氧气发生的电极反应式___________ 。
②如果粗铜中含有铁、银等杂质,粗铜电极发生的电极反应式有___________ 。乙装置中反应一段时间后,CuSO4溶液的浓度___________ (填“增大”、“减小”或“不变”)。
③已知NA为阿伏加德罗常数的值。若在标准状况下,甲装置有2.24L氧气参加反应,则乙装置中阴极析出铜的质量理论上为___________ g。
(1)按要求写出电极反应式
①碱性锌锰电池的总反应为Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,写出正极反应式
②将2FeCl3+2KI=I2+2FeCl2+2KCl设计成双液电池:正极烧杯中盛放的溶液为
(2)如图是以石墨为电极,电解MgCl2溶液的装置:

①电解时,A电极发生的电极反应为
②检验b管中气体的方法是
(3)某同学设计了如下图所示装置,用氢氧燃料电池作为电源探究粗铜精炼原理,根据要求回答问题:

①甲装置中通入氧气的电极为
②如果粗铜中含有铁、银等杂质,粗铜电极发生的电极反应式有
③已知NA为阿伏加德罗常数的值。若在标准状况下,甲装置有2.24L氧气参加反应,则乙装置中阴极析出铜的质量理论上为
您最近一年使用:0次
解题方法
6 . 结合所学知识,回答下列问题。
(1)按要求写出电极反应式
①碱性锌锰电池的总反应为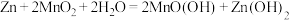 ,写出负极电极反应式
,写出负极电极反应式_____ 。
②将 设计成双液电池:正极烧杯中盛放的溶液为
设计成双液电池:正极烧杯中盛放的溶液为_____ ,电池正极的电极反应式为_____ 。
(2)下图是以石墨为电极,电解饱和食盐水的装置:
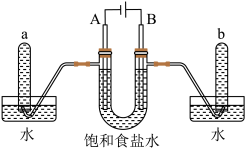
①电解时,A电极发生的电极下应式为_____ 。
②检验b试管中气体的操作是_____ 。
(3)某同学设计了如下图所示装置,用氢氧燃料电池作为电源探究粗铜精炼原理,根据要求回答下列问题:
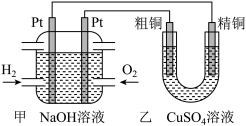
①甲装置中通入氧气的电极为_____ (填“正极”或“负极”),该极发生的电极反应式为_____ 。
②如果粗铜中含有铁、银等杂质,粗铜电极发生的电极反应式有_____ 。乙装置中反应一段时间后, 溶液的
溶液的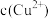
_____ (填“增大”、“减小”或“不变”)。
③在标准状况下,甲装置有 氧气参加反应,则乙装置中阴极析出铜的质量理论上为
氧气参加反应,则乙装置中阴极析出铜的质量理论上为_____ g。
(1)按要求写出电极反应式
①碱性锌锰电池的总反应为
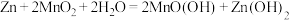 ,写出负极电极反应式
,写出负极电极反应式②将
 设计成双液电池:正极烧杯中盛放的溶液为
设计成双液电池:正极烧杯中盛放的溶液为(2)下图是以石墨为电极,电解饱和食盐水的装置:

①电解时,A电极发生的电极下应式为
②检验b试管中气体的操作是
(3)某同学设计了如下图所示装置,用氢氧燃料电池作为电源探究粗铜精炼原理,根据要求回答下列问题:

①甲装置中通入氧气的电极为
②如果粗铜中含有铁、银等杂质,粗铜电极发生的电极反应式有
 溶液的
溶液的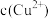
③在标准状况下,甲装置有
 氧气参加反应,则乙装置中阴极析出铜的质量理论上为
氧气参加反应,则乙装置中阴极析出铜的质量理论上为
您最近一年使用:0次
7 . 电解工作原理的实际应用非常广泛。
(1)电解精炼银时,阴极反应为_____ 。
(2)工业上为了处理含有 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有 和
和 沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法
沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误 的是_____(填字母)。
(3)某同学设计了如图装置进行以下电化学实验。
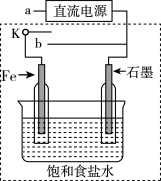
①当开关K与a连接时,两极均有气泡产生。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为_____ 。请写出此时Fe电极上的电极反应_____ 。
(4)1L某溶液中含有的离子如下表:
用惰性电极电解该溶液,当电路中有3mol 通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),则a=
通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),则a=_____ ,阳极生成_____ mol 。
。
(1)电解精炼银时,阴极反应为
(2)工业上为了处理含有
 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有 和
和 沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法
沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法A.阳极反应: |
B.阴极反应: |
| C.在电解过程中工业废水由酸性变为碱性 |
| D.可以将铁电极改为石墨电极 |
(3)某同学设计了如图装置进行以下电化学实验。

①当开关K与a连接时,两极均有气泡产生。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为
(4)1L某溶液中含有的离子如下表:
| 离子 |  |  |  |  |
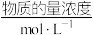 | 1 | 1 |  | 1 |
 通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),则a=
通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),则a= 。
。
您最近一年使用:0次
解题方法
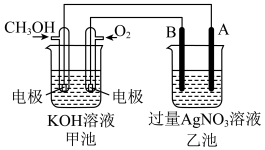
8 . 某电化学原理的示意图如图。填写下列空白: 的电极为
的电极为___________ 极,通入 的电极上发生的电极反应为
的电极上发生的电极反应为___________ ;工作过程中,甲池溶液的碱性会___________ (填“增强”、“减弱”或“不变”,下同)。若将甲池中的 溶液换成稀硫酸,工作过程中,甲池溶液的酸性会
溶液换成稀硫酸,工作过程中,甲池溶液的酸性会___________ 。
(2)若乙池中A为石墨电极,则A作___________ 极,该电极的电极反应式为___________ ;若乙池中A为铁电极,当铁电极的质量增加 时,理论上甲池中消耗的氧气在标准状况下的体积为
时,理论上甲池中消耗的氧气在标准状况下的体积为___________ L。
(3)若将乙池设计为电解精炼铜的装置,则___________ (填“A”或“B”,下同)极为粗铜;若将乙池改为电镀装置,则___________ 极为待镀金属制品。
(4)若将乙池中的硝酸银溶液换为硫酸铜溶液,通电一段时间后,向所得溶液中加入 碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为
碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为___________  。
。
 的电极为
的电极为 的电极上发生的电极反应为
的电极上发生的电极反应为 溶液换成稀硫酸,工作过程中,甲池溶液的酸性会
溶液换成稀硫酸,工作过程中,甲池溶液的酸性会(2)若乙池中A为石墨电极,则A作
 时,理论上甲池中消耗的氧气在标准状况下的体积为
时,理论上甲池中消耗的氧气在标准状况下的体积为(3)若将乙池设计为电解精炼铜的装置,则
(4)若将乙池中的硝酸银溶液换为硫酸铜溶液,通电一段时间后,向所得溶液中加入
 碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为
碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为 。
。
您最近一年使用:0次
2023-11-13更新
|
469次组卷
|
2卷引用:福建省泉州市2023-2024学年高二上学期期中考试化学试题
解题方法
9 . 燃料电池是一种连续的将燃料和氧化剂的化学能直接转化为电能的化学装置,氢气,氨、甲醇等气体或液体均可做燃料电池的燃料,具有广阔的发展前景。
(1)一种将燃料电池与电解池相组合的新工艺,可将高耗能的氯碱工业节能超过 。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极均为惰性电极。所用的离子交换膜都只允许阳离子通过。
。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极均为惰性电极。所用的离子交换膜都只允许阳离子通过。
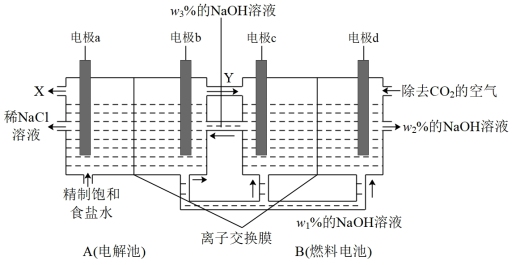
①X是___________ 。
②电池工作时电极a连接___________ (填“电极b”、“电极c”或“电极d”);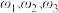 由大到小的顺序为
由大到小的顺序为___________ 。
③电极c的电极方程式为___________ 。
(2)甲烷碱性燃料电池提供电能,用电解法处理酸性含铬废水(主要含有 )时,铁板作阴、阳极,处理过程中发生反应:
)时,铁板作阴、阳极,处理过程中发生反应: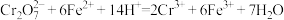 ,最后
,最后 以
以 形式除去。阳极电极反应式为
形式除去。阳极电极反应式为______ ,电解过程中废水的
_______ (填“变大”、“不变”或“变小”),当消耗甲烷 (标准状况)时最多有
(标准状况)时最多有______ g的 被还原。
被还原。
(1)一种将燃料电池与电解池相组合的新工艺,可将高耗能的氯碱工业节能超过
 。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极均为惰性电极。所用的离子交换膜都只允许阳离子通过。
。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极均为惰性电极。所用的离子交换膜都只允许阳离子通过。
①X是
②电池工作时电极a连接
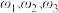 由大到小的顺序为
由大到小的顺序为③电极c的电极方程式为
(2)甲烷碱性燃料电池提供电能,用电解法处理酸性含铬废水(主要含有
 )时,铁板作阴、阳极,处理过程中发生反应:
)时,铁板作阴、阳极,处理过程中发生反应: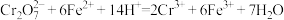 ,最后
,最后 以
以 形式除去。阳极电极反应式为
形式除去。阳极电极反应式为
 (标准状况)时最多有
(标准状况)时最多有 被还原。
被还原。
您最近一年使用:0次
10 . 电化学的发展是化学对人类的一项重大贡献。探究原电池和电解池原理,对生产生活具有重要的意义。
(1)利用新型镁-锂双离子二次电池的(图甲)做电源同时电解乙池和丙池。

①放电时,Li+的向_______ (镇“m极”或“n极”)移动;甲池中正极的电极反应式为:_______ 。
②给镁-锂双离子二次电池充电时,m与电源的_______ 极相连,当导线中每通过0.2mole-,甲池的左室中溶液的质量减少_______ g。
③电解一段时间后,乙池中溶液的pH将_______ (填“增大”“减小”或“不变”)。
④丙池发生电解反应的总方程式为_______ 。
(2)用电化学装置探究c(H+)对 与Cl-反应生成Cl2的影响。
与Cl-反应生成Cl2的影响。

①在酸性条件下,该反应的离子方程式为_______ 。
②上图装置验证增大c(H+),可提高 的氧化性,请补全操作和现象:闭合K,至指针读数稳定后,
的氧化性,请补全操作和现象:闭合K,至指针读数稳定后,_______ 。
(1)利用新型镁-锂双离子二次电池的(图甲)做电源同时电解乙池和丙池。

①放电时,Li+的向
②给镁-锂双离子二次电池充电时,m与电源的
③电解一段时间后,乙池中溶液的pH将
④丙池发生电解反应的总方程式为
(2)用电化学装置探究c(H+)对
 与Cl-反应生成Cl2的影响。
与Cl-反应生成Cl2的影响。
①在酸性条件下,该反应的离子方程式为
②上图装置验证增大c(H+),可提高
 的氧化性,请补全操作和现象:闭合K,至指针读数稳定后,
的氧化性,请补全操作和现象:闭合K,至指针读数稳定后,
您最近一年使用:0次



