解题方法
1 . 在如图所示装置中,试管A、B中的电极为多孔的惰性电极;C、D为两个铂夹,夹在被 溶液浸湿的滤纸条上,滤纸条的中部滴有
溶液浸湿的滤纸条上,滤纸条的中部滴有 液滴;电源有a、b两极。若在A、B中充满
液滴;电源有a、b两极。若在A、B中充满 溶液后倒立于盛有
溶液后倒立于盛有 溶液的水槽中,断开
溶液的水槽中,断开 ,闭合
,闭合 、
、 ,通直流电,实验现象如图所示,则:
,通直流电,实验现象如图所示,则:

(1)标出电源的正、负极:a为_______ 极,b为_______ 极。
(2)在湿的 滤纸条中部的
滤纸条中部的 液滴处有什么现象发生
液滴处有什么现象发生________ ?
(3)写出电极反应式:A中_______ ,B中_______ 。
(4)电解一段时间后,A、B中均有气体包围电极。此时切断 、
、 ,闭合
,闭合 ,检流计的指针是否移动?
,检流计的指针是否移动?_______ (填“是”或“否”),原因是_______ 。
 溶液浸湿的滤纸条上,滤纸条的中部滴有
溶液浸湿的滤纸条上,滤纸条的中部滴有 液滴;电源有a、b两极。若在A、B中充满
液滴;电源有a、b两极。若在A、B中充满 溶液后倒立于盛有
溶液后倒立于盛有 溶液的水槽中,断开
溶液的水槽中,断开 ,闭合
,闭合 、
、 ,通直流电,实验现象如图所示,则:
,通直流电,实验现象如图所示,则:
(1)标出电源的正、负极:a为
(2)在湿的
 滤纸条中部的
滤纸条中部的 液滴处有什么现象发生
液滴处有什么现象发生(3)写出电极反应式:A中
(4)电解一段时间后,A、B中均有气体包围电极。此时切断
 、
、 ,闭合
,闭合 ,检流计的指针是否移动?
,检流计的指针是否移动?
您最近一年使用:0次
解题方法
2 . 请分别以氢氧燃料电池和电解水装置为例,分析原电池与电解池的区别与联系_______ 。
您最近一年使用:0次
解题方法
3 . 甲烷燃料电池采用铂作为电极材料,两个电极上分别通入 和
和 ,电解质溶液为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验,如下图所示。回答下列问题。
,电解质溶液为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验,如下图所示。回答下列问题。

(1)甲烷燃料电池工作时,其电极反应分别为:正极___________ ;负极___________ 。
(2)闭合开关K后,a、b电极上均有气体产生,其中b电极上得到的是___________ ,电解NaCl溶液的总反应式为___________ 。
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上最多能产生氯气的体积为___________ L(标准状况)。
 和
和 ,电解质溶液为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验,如下图所示。回答下列问题。
,电解质溶液为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验,如下图所示。回答下列问题。
(1)甲烷燃料电池工作时,其电极反应分别为:正极
(2)闭合开关K后,a、b电极上均有气体产生,其中b电极上得到的是
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上最多能产生氯气的体积为
您最近一年使用:0次
4 . 如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:

(1)若两装置中均为 溶液,反应一段时间后:
溶液,反应一段时间后:
①有红色物质析出的是甲装置中的___________ 棒,乙装置中的___________ 棒;
②乙装置的电化学防护法称为___________ ,其中碳极的电极反应式是:___________ 。
③取少量甲装置中负极附近溶液加入2滴 溶液,现象为
溶液,现象为___________ ,生成沉淀的化学式为___________ 。
(2)若两装置中均为饱和 溶液:
溶液:
①写出乙装置中总反应的离子方程式:___________ 。
②将湿润的淀粉 试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因
试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因___________
(3)用铂作电极电解饱和的下列物质的水溶液,一会儿后,向剩余电解液中加适量水,能使溶液和电解前相同的是___________。

(1)若两装置中均为
 溶液,反应一段时间后:
溶液,反应一段时间后:①有红色物质析出的是甲装置中的
②乙装置的电化学防护法称为
③取少量甲装置中负极附近溶液加入2滴
 溶液,现象为
溶液,现象为(2)若两装置中均为饱和
 溶液:
溶液:①写出乙装置中总反应的离子方程式:
②将湿润的淀粉
 试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因
试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因(3)用铂作电极电解饱和的下列物质的水溶液,一会儿后,向剩余电解液中加适量水,能使溶液和电解前相同的是___________。
A. | B. | C. | D. |
您最近一年使用:0次
2021-11-20更新
|
491次组卷
|
5卷引用:4.4 金属的腐蚀与防护-2021-2022学年高二化学课后培优练(人教版选修4)
(已下线)4.4 金属的腐蚀与防护-2021-2022学年高二化学课后培优练(人教版选修4)河北省张家口市宣化第一中学2021-2022学年高二上学期期中考试化学试题(已下线)第28讲 金属的腐蚀与防护(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)河北省石家庄市第一中学东校区2023-2024学年高二上学期第一次月考化学试题河北省石家庄第一中学2023-2024学年高二上学期10月月考化学试题
5 . 电解原理在化学工业中有广泛应用。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
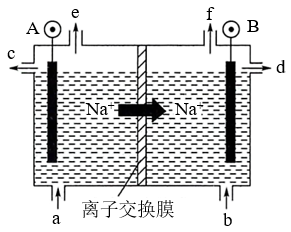
①电解饱和食盐水的总反应的离子方程式是___________ 。
②精制饱和食盐水在b口加入的物质为___________ (写化学式)
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
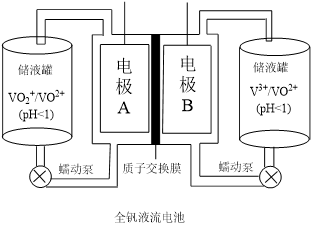
①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是___________ 。
②当完成储能时,阴极溶液的颜色是___________
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。
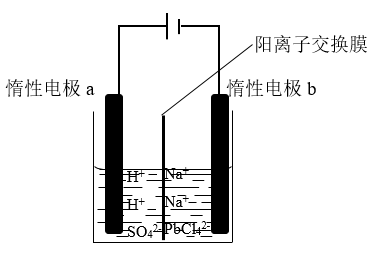
①写出电解时阴极的电极反应式___________
②电解过程中通过阳离子交换膜的离子主要为___________
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向___________ 极室(填“阴”或者“阳”)加入___________ (填化学式)。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:

①电解饱和食盐水的总反应的离子方程式是
②精制饱和食盐水在b口加入的物质为
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
| 离子种类 | VO | VO2+ | V3+ | V2+ |
| 颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |

①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是
②当完成储能时,阴极溶液的颜色是
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。

①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向
您最近一年使用:0次
2021-11-10更新
|
1568次组卷
|
8卷引用:4.3.1 电解原理-2021-2022学年高二化学课后培优练(人教版选修4)
(已下线)4.3.1 电解原理-2021-2022学年高二化学课后培优练(人教版选修4)山东省实验中学2021-2022学年高二上学期期中化学试题第四章化学反应与电能山东省枣庄滕州市第一中学2022-2023学年高二上学期10月月考化学试题福建省厦门集美中学2022-2023学年高二上学期第一次月考(10月)化学试题山东省新泰市第一中学2022-2023学年高二上学期期中考试化学试题山东省嘉祥县第一中学2022-2023学年高二上学期期末考试化学试题(已下线)专题突破卷07 化学反应与能量?-2024年高考化学一轮复习考点通关卷(新教材新高考)
名校
解题方法
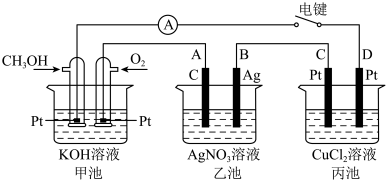
6 . 某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时。观察到电流表的指针发生了偏转。
(1)甲池为___________ (填“原电池”、“电解池”或“电镀池”),通入 电极的电极反应式为
电极的电极反应式为___________ 。
(2)乙池中A(石墨)电极的名称为___________ (填“正极”、“负极”、“阴极”或“阳极”)。总反应的离子方程式为___________ 。
(3)当乙池中B极质量增加21.6g时,甲池中理论上消耗 的体积为
的体积为___________ mL(标准状况下),丙池中___________ 极析出___________ g铜。
(4)若丙池中电极不变,将其溶液换成 溶液,电键闭合一段时向后。甲中溶液的pH将
溶液,电键闭合一段时向后。甲中溶液的pH将___________ (填“增大”“减小”或“不变”);丙中溶液的pH将___________ (填“增大”、“减小”或“不变”)。
(1)甲池为
 电极的电极反应式为
电极的电极反应式为(2)乙池中A(石墨)电极的名称为
(3)当乙池中B极质量增加21.6g时,甲池中理论上消耗
 的体积为
的体积为(4)若丙池中电极不变,将其溶液换成
 溶液,电键闭合一段时向后。甲中溶液的pH将
溶液,电键闭合一段时向后。甲中溶液的pH将
您最近一年使用:0次
2021-11-08更新
|
692次组卷
|
4卷引用:4.3.1 电解原理-2021-2022学年高二化学课后培优练(人教版选修4)
(已下线)4.3.1 电解原理-2021-2022学年高二化学课后培优练(人教版选修4)河北省唐山市第一中学2021-2022学年高二上学期期中考试化学试题(已下线)第26讲 电解池的原理(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)陕西省西安市2023-2024学年高二下学期4月期中联考化学试题
名校
7 . 铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

在相同条件下,三组装置中铁电极腐蚀最快的是_______ (填装置序号),该装置中正极反应式为_______ ;为防止金属 被腐蚀,可以采用上述
被腐蚀,可以采用上述_______ (填装置序号)装置原理进行防护;装置③中的石墨电极为_______ 极, 电极的电极反应式为
电极的电极反应式为_______ 。
(2)新型固体 隔膜电池广泛应用于电动汽车。电池反应为
隔膜电池广泛应用于电动汽车。电池反应为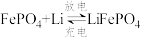 ,电解质为含
,电解质为含 的导电固体,且充、放电时电池内两极间的隔膜只允许
的导电固体,且充、放电时电池内两极间的隔膜只允许 自由通过而导电。该电池放电时
自由通过而导电。该电池放电时 向
向_______ 极移动(填“正”或“负”),负极反应为 ,则正极反应式为
,则正极反应式为_______ 。
(3)钢铁生锈现象随处可见,钢铁的电化学腐蚀原理如图所示:

①写出该腐蚀过程中的电池反应方程式:_______ 。
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图中虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向_______ 。该防护方法名称为_______ 。
③写出修改后石墨电极的电极反应式:_______ 。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

在相同条件下,三组装置中铁电极腐蚀最快的是
 被腐蚀,可以采用上述
被腐蚀,可以采用上述 电极的电极反应式为
电极的电极反应式为(2)新型固体
 隔膜电池广泛应用于电动汽车。电池反应为
隔膜电池广泛应用于电动汽车。电池反应为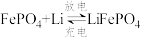 ,电解质为含
,电解质为含 的导电固体,且充、放电时电池内两极间的隔膜只允许
的导电固体,且充、放电时电池内两极间的隔膜只允许 自由通过而导电。该电池放电时
自由通过而导电。该电池放电时 向
向 ,则正极反应式为
,则正极反应式为(3)钢铁生锈现象随处可见,钢铁的电化学腐蚀原理如图所示:

①写出该腐蚀过程中的电池反应方程式:
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图中虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向
③写出修改后石墨电极的电极反应式:
您最近一年使用:0次
名校
8 . 氯碱工业是高能耗产业,一种将电解池与燃料电池相组合的新工艺节能超过30%。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子交换膜都只允许阳离子通过。
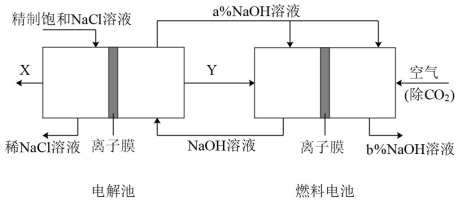
(1)图中X、Y分别是___ 、___ (填化学式),比较图示中a%与b%的大小___ 。
(2)写出燃料电池B中的电极反应:正极:___ 。负极:___ 。
(3)这种设计的主要节能之处在于(写出两处)___ ;___ 。

(1)图中X、Y分别是
(2)写出燃料电池B中的电极反应:正极:
(3)这种设计的主要节能之处在于(写出两处)
您最近一年使用:0次
2021-06-20更新
|
733次组卷
|
2卷引用:人教2019版选择性必修一第四章 化学反应与电能 复习与提高
9 . 如图所示的装置进行电解。通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色。
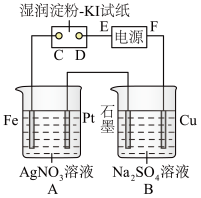
(1)E为电源的___ 极,F为电源的___ 极。
(2)A中发生反应的化学方程式为___ 。
(3)在B中观察到的现象是___ 。
(4)D端的电极反应式为___ 。

(1)E为电源的
(2)A中发生反应的化学方程式为
(3)在B中观察到的现象是
(4)D端的电极反应式为
您最近一年使用:0次
2020-12-13更新
|
598次组卷
|
7卷引用:4.2.1 电解原理(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
(已下线)4.2.1 电解原理(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)高二人教版选修4 第四章 第三节 电解池(已下线)4.2.1 电解原理(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)(已下线)4.2.2 电解原理的应用(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)2018-2019学年人教版高中化学选修四电化学基础章末综合测评题(四)(已下线)第4章 电化学基础(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)贵州省黔西南顶效开发区顶兴学校2021-2022学年高二下学期入学考试化学试题
解题方法
10 . 某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:
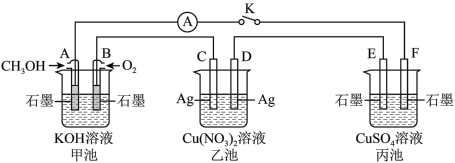
(1)甲池为__________ (填“原电池”或“电解池”),A电极的电极反应式为__________ 。
(2)丙池中E电极为_________ (填“正极”、“负极”、“阴极”或“阳极”),丙池总反应的离子方程式为__________ 。
(3)当乙池中C极质量减轻5.4 g时,甲池中B电极理论上消耗O2的体积为_____ mL(标准状况)
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是___ (填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
(5)爱迪生蓄电池的反应式为:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂.用如图装置可以制取少量高铁酸钠。
Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂.用如图装置可以制取少量高铁酸钠。
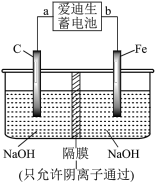
①此装置中爱迪生蓄电池的正极是________ (填“a”或“b”),该电池工作一段时间后必须充电,充电时阴极的电极反应式为____________________ 。
②写出在用电解法制取高铁酸钠时,阳极的电极反应式为____________________ 。

(1)甲池为
(2)丙池中E电极为
(3)当乙池中C极质量减轻5.4 g时,甲池中B电极理论上消耗O2的体积为
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
(5)爱迪生蓄电池的反应式为:Fe+NiO2+2H2O
 Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂.用如图装置可以制取少量高铁酸钠。
Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂.用如图装置可以制取少量高铁酸钠。
①此装置中爱迪生蓄电池的正极是
②写出在用电解法制取高铁酸钠时,阳极的电极反应式为
您最近一年使用:0次



