名校
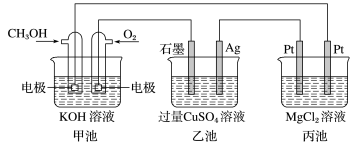
1 . 如图所示,甲池的总反应式为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是
| A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化为电能的装置 |
B.甲池中消耗560mL(标准状况下) ,此时乙池中银极增重3.2g ,此时乙池中银极增重3.2g |
C.甲池通入 的电极反应为 的电极反应为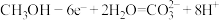 |
D.反应一段时间后,向丙池中加入一定量盐酸,一定能使 溶液恢复到原浓度 溶液恢复到原浓度 |
您最近一年使用:0次
2021-10-28更新
|
245次组卷
|
4卷引用:江西省遂川中学2021-2022学年高二上学期第三次月考化学(A卷)试题
名校
解题方法
2 . 一种充电电池放电时的电极反应为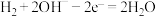 ;
; ,当为电池充电时,与外电源正极连接的电极上发生的反应是
,当为电池充电时,与外电源正极连接的电极上发生的反应是
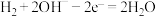 ;
; ,当为电池充电时,与外电源正极连接的电极上发生的反应是
,当为电池充电时,与外电源正极连接的电极上发生的反应是A. 的还原 的还原 |
B.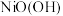 的还原 的还原 |
C.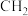 的氧化 的氧化 |
D. 的氧化 的氧化 |
您最近一年使用:0次
2021-09-19更新
|
356次组卷
|
5卷引用:江西省宁冈中学2021-2022学年高二上学期11月份第二次段考化学试题
名校
解题方法
3 . Mg-Li1-xFePO4是一种新型二次电池,其装置的示意图如下(Li+透过膜只允许Li+通过)。下列说法正确的是
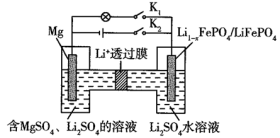

| A.断开K1、闭合K2,右室的电极为阳极,Li+发生还原反应 |
| B.断开K2、闭合K1,右室的电极反应式:Li1-xFePO4+xLi++xe-=LiFePO4 |
| C.断开K2、闭合K1,外电路中通过a mol电子时,左室溶液质量增加12a g |
D.该二次电池的总反应为xMg+xLi2SO4+2Li1-xFePO4 xMgSO4+2LiFePO4 xMgSO4+2LiFePO4 |
您最近一年使用:0次
2021-09-11更新
|
865次组卷
|
5卷引用:江西省景德镇市2022届高三第一次模拟化学试题
江西省景德镇市2022届高三第一次模拟化学试题河南省大联考2022届高三上学期阶段性测试(一)化学试题辽宁省沈阳市第十中学 2021-2022学年高三上学期第三阶段考试化学试题(已下线)专题11 电化学-2022年高考化学二轮复习重点专题常考点突破练陕西省西安交通大学附属中学2023-2024年高二上学期第一次月考化学试题
名校
4 . 按如图所示装置进行下列不同的操作,其中不正确的是
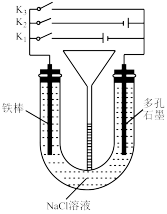

| A.先只接通K1,一段时间后,漏斗液面上升,然后再只接通K2,漏斗液面下降 |
| B.只接通K1,一段时间后,U形管中出现白色沉淀 |
| C.只接通K2,U形管左、右两端液面均下降 |
| D.铁腐蚀的速率由大到小的顺序是:只接通K1>只闭合K3>都断开>只闭合K2 |
您最近一年使用:0次
2021-08-26更新
|
713次组卷
|
6卷引用:江西省抚州市临川一中、临川一中实验学校2022届高三第一次月考化学试题
名校
5 . 利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法不正确的是
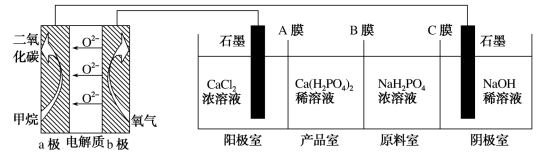

| A.a极反应:CH4-8e-+4O2-=CO2+2H2O |
| B.A、C膜均为阳离子交换膜,B膜为阴离子交换膜 |
| C.可用铁电极替换阴极的石墨电极 |
| D.a极上通入2.24L甲烷,阳极室Ca2+减少0.4mol |
您最近一年使用:0次
解题方法
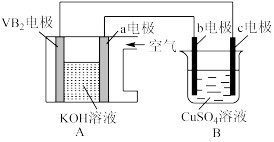
6 . 碱性硼化钒(VB2)一空气电池工作时反应为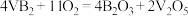 。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过
。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过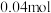 电子时,B装置内共收集到
电子时,B装置内共收集到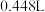 气体(标准状况下),则下列说法不正确的是
气体(标准状况下),则下列说法不正确的是
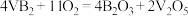 。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过
。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过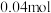 电子时,B装置内共收集到
电子时,B装置内共收集到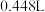 气体(标准状况下),则下列说法不正确的是
气体(标准状况下),则下列说法不正确的是
A.VB2电极发生的电极反应为 |
| B.外电路中电流由c电极流向VB2电极 |
| C.电解过程中,b电极表面有气泡产生 |
D.若B装置内的液体体积为 ,则 ,则 溶液的物质的量浓度为 溶液的物质的量浓度为 |
您最近一年使用:0次
解题方法
7 . 高铁电池作为新型可充电电池,具有放电曲线平坦,高能高容量,原料丰富,绿色无污染等优点。如图为简易的高铁电池的工作装置。已知:放电后,两极都产生红褐色悬浮物。下列说法正确的是
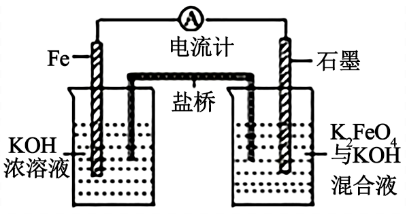

A.该电池放电时的总反应为Fe + FeO + 2H+ + 2H2O =2Fe(OH)3 + 2H+ + 2H2O =2Fe(OH)3 |
| B.放电时,此盐桥中阴离子的运动方向是从右向左 |
C.该电池充电时阳极反应的电极反应方程式为 FeO + 3e- + 4H2O = 2Fe(OH)3 + 5OH- + 3e- + 4H2O = 2Fe(OH)3 + 5OH- |
| D.每消耗56 g Fe,转移电子6 mol |
您最近一年使用:0次
8 . 某研究机构使用Li—SO2Cl2电池作为电源电解制备Ni(H2PO2)2,其工作原理如图所示。已知电池反应为2Li+SO2Cl2=2LiCl+SO2↑,下列说法正确的是


| A.电池的f极连接电解池的h极 |
| B.膜a、c是阴离子交换膜,膜b是阳离子交换膜 |
| C.电池中C电极的电极反应式为SO2Cl2+2e-=2Cl-+SO2↑ |
| D.电解池中不锈钢电极溶解,需要及时更换补充 |
您最近一年使用:0次
9 . 如图所示实验装置中,若将K闭合,则下列有关说法中正确的是
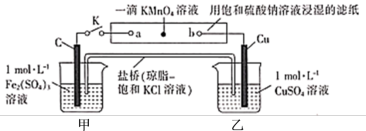

| A.电子沿Cu→b→a→C路径流动 |
| B.C电极的电极反应式为2H++2e-=H2↑ |
| C.滤纸上的红点向b移动 |
| D.一段时间后乙池中c(Cu2+)增大 |
您最近一年使用:0次
名校
10 . 二甲醚(CH3OCH3)被称为 21 世纪的新型燃料,它清洁、高效、具有优良的环保性能,二甲醚是种无色气体,具有轻微的醚香味,二甲醚可作燃料电池的燃料。
(1)以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。请写出该电池中负极上的电极反应式是:___________ 。
(2)用(1)中的燃料电池为电源,以石墨为电极电解500mLNaCl溶液,装置如图甲所示。

①请写出电解过程中总反应的离子方程式___________ 。
②当燃料电池消耗 2.8 LO2 (标准状况下)时,计算此时:NaCl 溶液中c(OH-)=___________ mol/L (假设溶液的体积不变,气体全部从溶液中逸出)。
③短暂电解之后,要使溶液恢复原状,应该向溶液中加入物质___________ (填名称)。
(3)用(1)中的燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图乙所示。
①上述装置中 D电极应连接二甲醚燃料电池的___________ (填“正极”或“负极”),该电解池中离子交换膜为___________ 离子交换膜(填“阴”或“阳”)。
②该电解池的阳极反应式为___________ 。
(1)以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。请写出该电池中负极上的电极反应式是:
(2)用(1)中的燃料电池为电源,以石墨为电极电解500mLNaCl溶液,装置如图甲所示。

①请写出电解过程中总反应的离子方程式
②当燃料电池消耗 2.8 LO2 (标准状况下)时,计算此时:NaCl 溶液中c(OH-)=
③短暂电解之后,要使溶液恢复原状,应该向溶液中加入物质
(3)用(1)中的燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图乙所示。
①上述装置中 D电极应连接二甲醚燃料电池的
②该电解池的阳极反应式为
您最近一年使用:0次
2021-02-05更新
|
357次组卷
|
3卷引用:江西师范大学附属中学2020-2021学年高二上学期期末考试化学试题



