1 . 能源、环境与生产生活和社会发展密切相关。
(1)工业上利用CO和H2在催化剂作用下合成甲醇: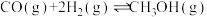 (甲醇结构式
(甲醇结构式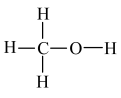 ),已知反应中有关物质的化学键键能数据如下表所示:
),已知反应中有关物质的化学键键能数据如下表所示:
则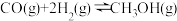
 =
=___________ kJ/mol
(2)以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池。下图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。___________ 极,B极的电极反应式为___________ 。
(3)如图,其中甲池的总反应式为: ,下列说法正确的是
,下列说法正确的是___________ 装置,乙池中石墨电极的名称是___________ 。
②甲池通入氧气的电极反应式为___________ 。
③电解一段时间后,乙池中溶液的pH将___________ (填“增大”“减小”或“不变”)
④丙池中阴极上发生的电极反应为___________ 。
(4)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有 ),实验室利用如图装置模拟该方法:
),实验室利用如图装置模拟该方法:___________ (填“正”或“负”)极,M电极的电极反应式为___________ 。
(1)工业上利用CO和H2在催化剂作用下合成甲醇:
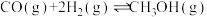 (甲醇结构式
(甲醇结构式 ),已知反应中有关物质的化学键键能数据如下表所示:
),已知反应中有关物质的化学键键能数据如下表所示:| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
则
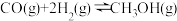
 =
=(2)以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池。下图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。

(3)如图,其中甲池的总反应式为:
 ,下列说法正确的是
,下列说法正确的是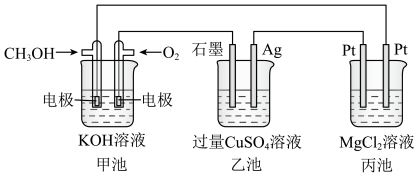
②甲池通入氧气的电极反应式为
③电解一段时间后,乙池中溶液的pH将
④丙池中阴极上发生的电极反应为
(4)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有
 ),实验室利用如图装置模拟该方法:
),实验室利用如图装置模拟该方法: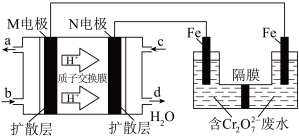
您最近半年使用:0次
名校
解题方法
2 . 应用电化学原理,回答下列问题。
(1)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是_______ 。
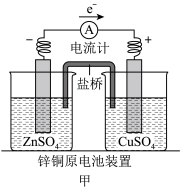
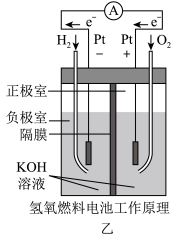
(2)乙中正极反应式为___________ ;若将H2换成CH4,则负极反应式为___________ 。
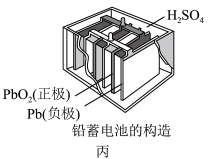
(3)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池___________ 极相连接。充电时该电极反应式___________ 。
(4)若用铅蓄电池作为电源电解硝酸银溶液500mL,电路中转移0.2mol电子,则溶液中氢离子浓度为___________ (忽略溶液体积变化)。
(5)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可利用电解原理,将氨转化为高纯氢气,其装置如图所示。

①电解过程中OH-的移动方向为___________ (填“从左往右”或“从右往左”);
②阳极的电极反应式为___________ 。
(1)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是

(2)乙中正极反应式为

(3)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池

(4)若用铅蓄电池作为电源电解硝酸银溶液500mL,电路中转移0.2mol电子,则溶液中氢离子浓度为
(5)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可利用电解原理,将氨转化为高纯氢气,其装置如图所示。

①电解过程中OH-的移动方向为
②阳极的电极反应式为
您最近半年使用:0次
名校
解题方法
3 . 双盐 电池由
电池由 替代了
替代了 在正极材料中的嵌入,解决了
在正极材料中的嵌入,解决了 扩散缓慢、锂离子电池锂枝晶生长等问题,其充、放电过程如图所示。下列说法正确的是
扩散缓慢、锂离子电池锂枝晶生长等问题,其充、放电过程如图所示。下列说法正确的是
 电池由
电池由 替代了
替代了 在正极材料中的嵌入,解决了
在正极材料中的嵌入,解决了 扩散缓慢、锂离子电池锂枝晶生长等问题,其充、放电过程如图所示。下列说法正确的是
扩散缓慢、锂离子电池锂枝晶生长等问题,其充、放电过程如图所示。下列说法正确的是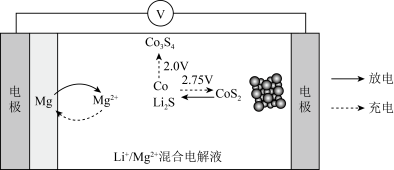
A.放电时, 电极的电势高于 电极的电势高于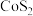 电极 电极 |
| B.充电时,若充电电压为2.0V,可能造成电池性能衰减 |
C.放电时,每转移2  ,正极质量减少14g ,正极质量减少14g |
D.充电时,充电电压为2.75V时,负极区的反应为: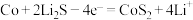 |
您最近半年使用:0次
2024-02-17更新
|
709次组卷
|
4卷引用:湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
名校
解题方法
4 . 镍镉电池是应用广泛的二次电池,其总反应为:Cd+2NiOOH+2H2O 2Ni(OH)2+ Cd(OH)2,制造密封式镍镉电池的部分工艺如下:
2Ni(OH)2+ Cd(OH)2,制造密封式镍镉电池的部分工艺如下:
I.Ni(OH)2的制备
以硫酸镍(NiSO4)为原料制备Ni(OH)2的主要过程如下图所示。制备过程中,通过降低镍离子的浓度可以降低Ni(OH)2沉淀速率,从而避免沉淀团聚,提升电池性能。

已知:Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O
(1)操作a是___________ 。
(2)制备过程中,需先加氨水,再加过量NaOH,请分析:
①先加氨水的目的是___________ 。
②用化学平衡移动原理分析加入NaOH需过量的原因是___________ 。
(3)用无水乙醇代替水洗涤滤渣的优点是___________ (答出1条即可)。
II.镍镉电池的组装
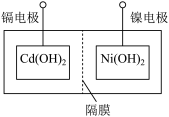
主要步骤:①将Ni(OH)2和Cd(OH)2固定,中间以隔膜隔开(如下图所示);
②将多组上述结构串联;③向电池中注入KOH溶液;④密封。
(4)下列对镍镉电池组装和使用的分析正确的是___________ (填字母序号)。
a.密封镍镉电池可以避免KOH变质
b.镍电极为电池的负极,镉电极为电池的正极
c.电池组装后,应先充电,再使用
(5)该电池充电时,阳极反应式为___________ ,阴极反应式为___________ 。充电时,若Cd(OH)2耗尽后继续充电,会造成安全隐患,镉电极上生成的气体是___________ 。
(6)已知:①隔膜可以透过阴离子和分子;②O2可以与Cd发生反应生成Cd(OH)2制造电池时,在镉电极加入过量的Cd(OH)2,则Cd(OH)2不会被消耗完,对电池进行过度充电保护,此时:OH-从______ 电极区(填“镍”或“镉”)到______ 电极区(填“镍”或“镉”,下同)。O2从______ 电极区到_____ 电极区。
 2Ni(OH)2+ Cd(OH)2,制造密封式镍镉电池的部分工艺如下:
2Ni(OH)2+ Cd(OH)2,制造密封式镍镉电池的部分工艺如下:I.Ni(OH)2的制备
以硫酸镍(NiSO4)为原料制备Ni(OH)2的主要过程如下图所示。制备过程中,通过降低镍离子的浓度可以降低Ni(OH)2沉淀速率,从而避免沉淀团聚,提升电池性能。

已知:Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O
(1)操作a是
(2)制备过程中,需先加氨水,再加过量NaOH,请分析:
①先加氨水的目的是
②用化学平衡移动原理分析加入NaOH需过量的原因是
(3)用无水乙醇代替水洗涤滤渣的优点是
II.镍镉电池的组装
主要步骤:①将Ni(OH)2和Cd(OH)2固定,中间以隔膜隔开(如下图所示);
②将多组上述结构串联;③向电池中注入KOH溶液;④密封。

(4)下列对镍镉电池组装和使用的分析正确的是
a.密封镍镉电池可以避免KOH变质
b.镍电极为电池的负极,镉电极为电池的正极
c.电池组装后,应先充电,再使用
(5)该电池充电时,阳极反应式为
(6)已知:①隔膜可以透过阴离子和分子;②O2可以与Cd发生反应生成Cd(OH)2制造电池时,在镉电极加入过量的Cd(OH)2,则Cd(OH)2不会被消耗完,对电池进行过度充电保护,此时:OH-从
您最近半年使用:0次
名校
解题方法
5 . 某小组进行电化学研究, 甲同学设计如图的原电池装置,乙同学利用甲设计的装置及提供的药品与材料,不能完成的实验是
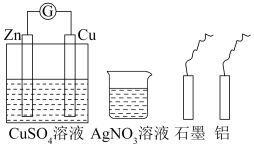

| A.在石墨电极上镀锌 | B.设计一个新的原电池 |
| C.使甲同学的正极变为负极 | D.使锌电极受到保护 |
您最近半年使用:0次
名校
解题方法
6 . 液体锌电池是一种电压较高的二次电池,具有成本低、安全性强、可循环使用等特点,其放电过程示意图如图。下列说法不正确 的是
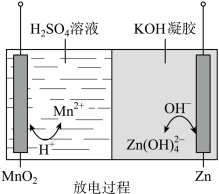
已知:① ;②KOH凝胶中允许离子存在、生成或迁移。
;②KOH凝胶中允许离子存在、生成或迁移。

已知:①
 ;②KOH凝胶中允许离子存在、生成或迁移。
;②KOH凝胶中允许离子存在、生成或迁移。A.充电过程中,阴极的电极反应: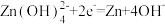 |
B.放电过程中,正极的电极反应: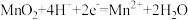 |
C.放电过程中, 由正极向负极迁移 由正极向负极迁移 |
D.在充、放电过程中,凝胶中的 可再生 可再生 |
您最近半年使用:0次
2024-01-04更新
|
503次组卷
|
7卷引用:湖南省长沙市明德中学 2021-2022学年高二上学期12月月考化学试题
名校
解题方法
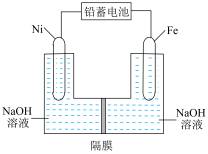
7 . 铅蓄电池在日常生活中应用广泛。回答下列问题:
(1)现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移 电子时铁电极的质量减少
电子时铁电极的质量减少 ,则:
,则:
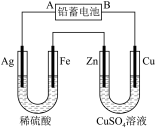
①A是铅蓄电池的___________ 极。
②Cu电极的电极反应式是___________ , 溶液的浓度
溶液的浓度___________ (填“减小”“增大”或“不变”)。
(2)铅蓄电池的 可以用石墨为电极,
可以用石墨为电极, 和
和 的混合溶液为电解液制取。阳极发生的电极反应式为
的混合溶液为电解液制取。阳极发生的电极反应式为___________ 。
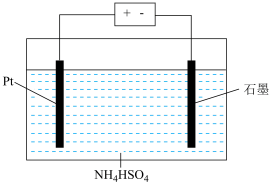
(3)将 溶液加入如图所示的电解池的阳极区,用铅蓄电池进行电解,电解过程中阳极区发生如下反应:
溶液加入如图所示的电解池的阳极区,用铅蓄电池进行电解,电解过程中阳极区发生如下反应: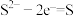 ,
, 。
。
电解时阴极的电极反应式:___________ ,电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成___________ 。
(4) 是一种既能杀菌、消毒,又能䋈凝净水的水处理剂,其电解制法如图所示,请根据图示写出
是一种既能杀菌、消毒,又能䋈凝净水的水处理剂,其电解制法如图所示,请根据图示写出 电极发生的电极反应为:
电极发生的电极反应为:___________ 。
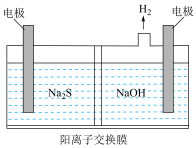
(5)工业上常采用催化还原法和碱吸收法处理 气体。当吸收液失去吸收能力后通入
气体。当吸收液失去吸收能力后通入 可得到
可得到 溶液,用如图所示装置电解所得
溶液,用如图所示装置电解所得 溶液可制得强氧化剂
溶液可制得强氧化剂 。
。
请写出电解 溶液的化学方程式
溶液的化学方程式___________ 。
(1)现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移
 电子时铁电极的质量减少
电子时铁电极的质量减少 ,则:
,则:
①A是铅蓄电池的
②Cu电极的电极反应式是
 溶液的浓度
溶液的浓度(2)铅蓄电池的
 可以用石墨为电极,
可以用石墨为电极, 和
和 的混合溶液为电解液制取。阳极发生的电极反应式为
的混合溶液为电解液制取。阳极发生的电极反应式为(3)将
 溶液加入如图所示的电解池的阳极区,用铅蓄电池进行电解,电解过程中阳极区发生如下反应:
溶液加入如图所示的电解池的阳极区,用铅蓄电池进行电解,电解过程中阳极区发生如下反应: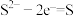 ,
, 。
。
电解时阴极的电极反应式:
(4)
 是一种既能杀菌、消毒,又能䋈凝净水的水处理剂,其电解制法如图所示,请根据图示写出
是一种既能杀菌、消毒,又能䋈凝净水的水处理剂,其电解制法如图所示,请根据图示写出 电极发生的电极反应为:
电极发生的电极反应为:
(5)工业上常采用催化还原法和碱吸收法处理
 气体。当吸收液失去吸收能力后通入
气体。当吸收液失去吸收能力后通入 可得到
可得到 溶液,用如图所示装置电解所得
溶液,用如图所示装置电解所得 溶液可制得强氧化剂
溶液可制得强氧化剂 。
。
请写出电解
 溶液的化学方程式
溶液的化学方程式
您最近半年使用:0次
名校
8 . 回答下列问题
(1)某兴趣小组的同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
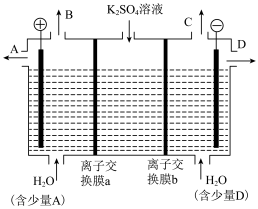
①该电解槽的阴极反应式为___________ 。
②通电开始后,阳极附近溶液pH会___________ (填“变大”、“变小”或“不变”)
③出口A获得___________ 产品,离子交换膜b是___________ 离子交换膜(填“阳”或“阴”)。
(2)电化学在化学工业中有着广泛应用。根据图示电化学装置,回答下列问题:
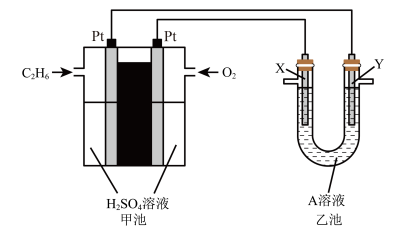
①甲池通入乙烷(C2H6)一极的电极反应式为___________ 。
②乙池中,若X、Y都是石墨,A是饱和食盐水,乙池中的离子反应方程式为___________ 。
③若使用铜棒、铁质钥匙等材料用该装置实现在铁质钥匙表面镀一层金属铜,CuSO4溶液作电解液,则乙池中:铁质钥匙应放在___________ 极(填X或Y),电镀一段时间后,CuSO4溶液浓度___________ (“减小”“不变”“增大”)。
④乙池中,若X、Y都是石墨,A是足量AgNO3溶液,体积为2L,电解一段时间后,甲池消耗1.12LO2 (标准状况下),则乙池溶液的pH为___________ (忽略溶液体积的变化)。
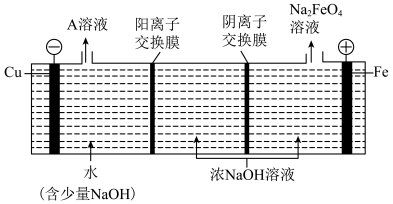
(3)工业上通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图所示,则阳极的电极反应式为___________ ,当制备0.5mol Na2FeO4时,阴极产生气体体积为___________ (标准状况下)。
(1)某兴趣小组的同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阴极反应式为
②通电开始后,阳极附近溶液pH会
③出口A获得
(2)电化学在化学工业中有着广泛应用。根据图示电化学装置,回答下列问题:

①甲池通入乙烷(C2H6)一极的电极反应式为
②乙池中,若X、Y都是石墨,A是饱和食盐水,乙池中的离子反应方程式为
③若使用铜棒、铁质钥匙等材料用该装置实现在铁质钥匙表面镀一层金属铜,CuSO4溶液作电解液,则乙池中:铁质钥匙应放在
④乙池中,若X、Y都是石墨,A是足量AgNO3溶液,体积为2L,电解一段时间后,甲池消耗1.12LO2 (标准状况下),则乙池溶液的pH为
(3)工业上通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图所示,则阳极的电极反应式为

您最近半年使用:0次
名校
解题方法
9 . 降低能耗是氯碱工业发展的重要方向。
(1)我国利用氯碱厂生产的 作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
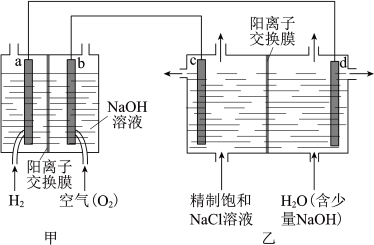
① 极为
极为_____ (填“正”或“负”)极。
②乙装置中电解饱和 溶液的化学方程式为
溶液的化学方程式为_____ 。
③下列说法正确的是_____ 。
A.甲装置可以实现化学能向电能转化
B.甲装置中 透过阳离子交换膜向
透过阳离子交换膜向 极移动
极移动
C.乙装置中 极一侧流出的是淡盐水
极一侧流出的是淡盐水
④结合化学用语解释 极区产生
极区产生 的原因:
的原因:_____ 。
⑤实际生产中,阳离子交换膜的损伤会造成 迁移至阳极区,从而在电解池阳极能检测到
迁移至阳极区,从而在电解池阳极能检测到 ,产生
,产生 的电极反应式为
的电极反应式为_____ 。下列生产措施有利于提高 产量、降低阳极
产量、降低阳极 含量的是
含量的是_____ 。
A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用 浓度高的精制饱和食盐水为原料
浓度高的精制饱和食盐水为原料
(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入 ,避免水电离的
,避免水电离的 直接得电子生成
直接得电子生成 ,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为_____ 。
(1)我国利用氯碱厂生产的
 作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
作燃料,将氢燃料电站应用于氯碱工业,其示意图如下。
①
 极为
极为②乙装置中电解饱和
 溶液的化学方程式为
溶液的化学方程式为③下列说法正确的是
A.甲装置可以实现化学能向电能转化
B.甲装置中
 透过阳离子交换膜向
透过阳离子交换膜向 极移动
极移动C.乙装置中
 极一侧流出的是淡盐水
极一侧流出的是淡盐水④结合化学用语解释
 极区产生
极区产生 的原因:
的原因:⑤实际生产中,阳离子交换膜的损伤会造成
 迁移至阳极区,从而在电解池阳极能检测到
迁移至阳极区,从而在电解池阳极能检测到 ,产生
,产生 的电极反应式为
的电极反应式为 产量、降低阳极
产量、降低阳极 含量的是
含量的是A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用
 浓度高的精制饱和食盐水为原料
浓度高的精制饱和食盐水为原料(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入
 ,避免水电离的
,避免水电离的 直接得电子生成
直接得电子生成 ,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
您最近半年使用:0次
2023-10-01更新
|
48次组卷
|
3卷引用:北京市大兴区第一中学1+3学部2021-2022学年高二上学期期中考试化学试卷
名校
解题方法
10 . 某课外活动小组用如图所示装置进行实验(电解液足量)。下列说法正确的是
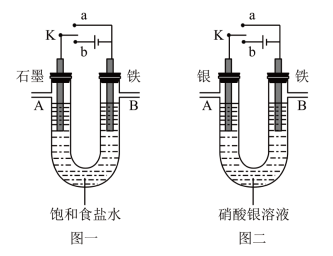

| A.图二中若开始实验时开关K与a连接,电解液的浓度保持不变 |
| B.图一中若开始实验时开关K与b连接,一段时间后向电解液中加适量稀盐酸可使电解液恢复到电解前的浓度 |
C.图一中若开始实验时开关K与a连接,B极的电极反应式为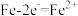 |
| D.图二中若开始实验时开关K与b连接,A极减少的质量不等于B极增加的质量 |
您最近半年使用:0次



