解题方法
1 . 按下图装置进行实验,并回答下列问题
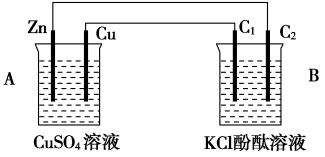
(1)判断装置的名称:A池为_______ , B池为_______ 。
(2)铜极为_______ 极,电极反应式为_______ ,石墨棒C1为_______ 极,电极反应式为_______ 。
(3)石墨棒C2附近发生的实验现象为_______ 。

(1)判断装置的名称:A池为
(2)铜极为
(3)石墨棒C2附近发生的实验现象为
您最近半年使用:0次
解题方法
2 . 镍镉(NiCd)可充电电池在现代生活中有广泛应用。有一种镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行: 。
。
(1)此蓄电池放电时,该电池某一电极发生还原反应的物质是_______ 。
A.NiO(OH) B.Cd C.Cd(OH)2 D.Ni(OH)2
放电时负极反应式是_______
(2)有关该蓄电池的说法中,正确的是_______。
(3)假如用此蓄电池做电源,电解M(NO3)x溶液(惰性电极),当该蓄电池消耗0.36 g水时,电解M(NO3)x溶液的某一极析出了a g金属M,则金属M的相对原子质量的计算式为_______ (用含a、x的式子表示)。
 。
。(1)此蓄电池放电时,该电池某一电极发生还原反应的物质是
A.NiO(OH) B.Cd C.Cd(OH)2 D.Ni(OH)2
放电时负极反应式是
(2)有关该蓄电池的说法中,正确的是_______。
| A.充电时阳极反应:Ni(OH)2+OH--e-=NiO(OH)+H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的c(OH-)减小 |
| D.放电时电解质溶液中的OH-向正极移动 |
您最近半年使用:0次
名校
解题方法
3 . 粗铜中一般含有锌、铁、银、金等杂质。在如图所示的装置中,甲池的总反应方程式为2CH3OH+3O2+4KOH=2K2CO3+6H2O。接通电路一段时间后,精Cu电极质量增加了3.2 g。在此过程中,下列说法正确的是
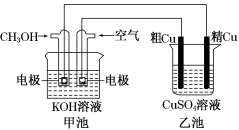
| A.乙池中CuSO4溶液的浓度减小 |
| B.甲池中理论上消耗标准状况下空气的体积是2.8 L(空气中O2体积分数以20%计算) |
| C.甲池是电能转化为化学能的装置,乙池是化学能转化为电能的装置 |
D.甲池通入CH3OH一极的电极反应为CH3OH-6e-+2H2O=CO +8H+ +8H+ |
您最近半年使用:0次
2022-12-11更新
|
233次组卷
|
3卷引用:山东省济南市莱芜第四中学2021-2022学年高二上学期第二次质量检测化学试题
解题方法
4 . 填空。
(1)氯碱工业是高耗能产业,一种将电解池与燃料电池相结合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
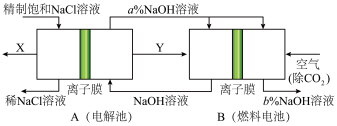
①图中X是_______ (填化学式),写出另外一极产生Y气体的电极反应式为_______ ,比较图示中氢氧化钠质量分数a%与b%的大小:a%_______ b%(填大于、小于、等于)。
②写出燃料电池B中正极发生的电极反应:_______ 。
(2)利用LiOH和钴氧化物可制备锂离子电池正极材料,LiOH可由电解法制备。利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。

B极区电解液为_______ 溶液,阳极电极反应式为_______ ,电解过程中Li+ 向_______ (填“A”或“B”)电极迁移。
(1)氯碱工业是高耗能产业,一种将电解池与燃料电池相结合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。

①图中X是
②写出燃料电池B中正极发生的电极反应:
(2)利用LiOH和钴氧化物可制备锂离子电池正极材料,LiOH可由电解法制备。利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。

B极区电解液为
您最近半年使用:0次
解题方法
5 . 某化学兴趣小组的同学用如图所示装置研究电化学问题。当闭合该装置的电键时,观察到电流计的指针发生偏转。下列有关说法中不正确的是
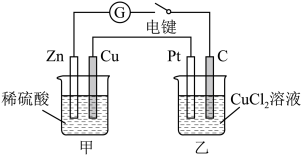

| A.甲装置是原电池,乙装置是电解池 |
| B.当甲中产生0.1 mol气体时,乙中析出固体的质量为6.4 g |
| C.实验一段时间后,甲烧杯中溶液的pH增大 |
| D.将乙中的C电极换成铜电极,则乙装置可变成电镀装置 |
您最近半年使用:0次
解题方法
6 . 如图装置所示,是用氢氧燃料电池B进行的某电解实验:

(1)若电池B使用了亚氨基锂(Li2NH)固体作为储氢材料,其储氢原理是:Li2NH+H2=LiNH2+LiH,则下列说法中正确的是_____ 。
(2)在电池B工作时:
①若用固体Ca(HSO4)2为电解质传递H+,则电子由_____ 极流出,H+向_____ 极移动。(填“a”或“b”)
②b极上的电极反应式为:____ 。
③外电路中,每转移0.1mol电子,在a极消耗____ L的H2(标准状况下)。
(3)若A中X、Y都是惰性电极,电解液W是滴有酚酞的饱和NaCl溶液,则B工作时:
①电解池中X极上的电极反应式是____ ,在X极这边观察到的现象是_____ 。
②检验Y电极上反应产物的方法是____ 。
③若A中其它均不改变,只将电极Y换成铁棒,可实现的实验目的是_____ 。

(1)若电池B使用了亚氨基锂(Li2NH)固体作为储氢材料,其储氢原理是:Li2NH+H2=LiNH2+LiH,则下列说法中正确的是
| A.Li2NH中N的化合价是-1 |
| B.该反应中H2既是氧化剂又是还原剂 |
| C.Li+和H+的离子半径相等 |
| D.此法储氢和钢瓶储氢的原理相同 |
①若用固体Ca(HSO4)2为电解质传递H+,则电子由
②b极上的电极反应式为:
③外电路中,每转移0.1mol电子,在a极消耗
(3)若A中X、Y都是惰性电极,电解液W是滴有酚酞的饱和NaCl溶液,则B工作时:
①电解池中X极上的电极反应式是
②检验Y电极上反应产物的方法是
③若A中其它均不改变,只将电极Y换成铁棒,可实现的实验目的是
您最近半年使用:0次
解题方法
7 . 科研人员用惰性电极设计出甲烷燃料电池并用于电解食盐水的装置如下图所示,电池的电解质是掺杂了Y2O3与ZrO2的固体,可在高温下传导O2-。下列说法正确的是


| A.若燃料电池消耗0.5mol的CH4,则D电极产生44.8L气体 |
| B.电池工作时,Cl-通过离子交换膜移向C电极 |
| C.D电极附近溶液pH减小 |
| D.A电极上发生的电极反应式CH4-8e-+4O2-=CO2+2H2O |
您最近半年使用:0次
2022-12-09更新
|
139次组卷
|
2卷引用:吉林省洮南市第一中学2021-2022学年高三上学期第四次月考化学试题
名校
解题方法
8 . 某同学利用下图所示装置探究金属的腐蚀与防护条件。下列不合理的是
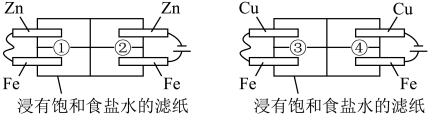

A.①区 电极的电极反应式为 电极的电极反应式为 , , 电极附近滴加 电极附近滴加 溶液未出现蓝色, 溶液未出现蓝色, 被保护 被保护 |
B.②区 电极的电极反应式为 电极的电极反应式为 , , 电极附近滴加 电极附近滴加 溶液出现蓝色, 溶液出现蓝色, 被腐蚀 被腐蚀 |
C.③区 电极上产生气泡, 电极上产生气泡, 电极附近滴加 电极附近滴加 溶液后出现蓝色, 溶液后出现蓝色, 被腐蚀 被腐蚀 |
D.④区 电极附近滴加酚酞后变成红色, 电极附近滴加酚酞后变成红色, 电极附近滴加 电极附近滴加 溶液出现蓝色, 溶液出现蓝色, 被腐蚀 被腐蚀 |
您最近半年使用:0次
2022-12-09更新
|
503次组卷
|
2卷引用:山东省青岛第二中学2020-2021学年高二上学期期末化学试题
解题方法
9 . 装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:

(1)B极是电源的________ 极,C极的电极反应式为_____________ ,
(2)一段时间后丁中X极附近的颜色逐渐____________ (填“变深”或“变浅”)。
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为_____________ 。
(4)现用丙装置给铜件镀银,则H应该是______ (填“铜”或“银”),电镀液是__________ 溶液。常温下,当乙中溶液的c(OH-)=0.1mol·L-1时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为____________ g。
(5)若甲烧杯是在铁件表面镀铜,已知电镀前两电极质量相同,电镀完成后将它们取出,洗净、烘干、称量,发现二者质量相差7.68g,则电镀时电路中通过的电子为____ mol。

(1)B极是电源的
(2)一段时间后丁中X极附近的颜色逐渐
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为
(4)现用丙装置给铜件镀银,则H应该是
(5)若甲烧杯是在铁件表面镀铜,已知电镀前两电极质量相同,电镀完成后将它们取出,洗净、烘干、称量,发现二者质量相差7.68g,则电镀时电路中通过的电子为
您最近半年使用:0次
解题方法
10 . 某同学设计了如图所示装置,可探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
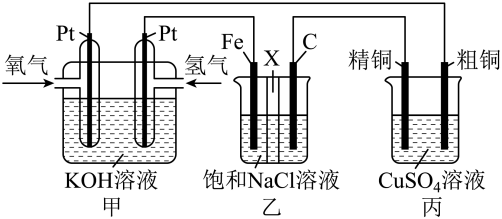
根据要求回答相关问题:
(1)甲装置中通入氧气的电极为_______ (填“正极”或“负极”),负极的电极反应式_______ 。
(2)乙装置中Fe电极为_______ (填“阳极”或“阴极”);C电极上发生_______ (填“氧化”或“还原”)反应,电极反应式为_______ 。
(3)反应一段时间后,乙装置中氢氧化钠主要在_______ (填“Fe电极”或“C电极”)区生成。
(4)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间后,CuSO4溶液的浓度_______ (填“增大”“减小”或“不变”)。
(5)已知NA为阿伏加德罗常数的值。若在标准状况下,有2.24L氧气参加反应,则丙装置中阴极析出铜的质量为_______ 。

根据要求回答相关问题:
(1)甲装置中通入氧气的电极为
(2)乙装置中Fe电极为
(3)反应一段时间后,乙装置中氢氧化钠主要在
(4)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间后,CuSO4溶液的浓度
(5)已知NA为阿伏加德罗常数的值。若在标准状况下,有2.24L氧气参加反应,则丙装置中阴极析出铜的质量为
您最近半年使用:0次



