名校
1 . 人们应用原电池原理制作多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(1)如图利用氧化还原反应设计而成的原电池:
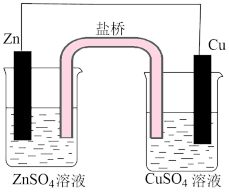
①左边烧杯内发生___________ (填“氧化”或“还原”)反应。
②右边烧杯内的电极反应式是___________ 。
③外电路中电子的流向是___________ 。
④电池总反应离子方程式是_______ 。盐桥M中装有 溶液和琼脂,其作用是
溶液和琼脂,其作用是_______ 。
(2)HCOOH燃料电池。研究HCOOH燃料电池性能的装置如图-2所示,两电极区间用允许K+、H+通过的半透膜隔开。
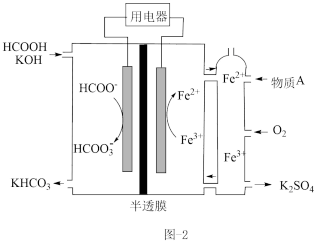
①电池负极电极反应式为_______ ;放电过程中需补充的物质A为______ (填化学式)。
②图-2所示的HCOOH燃料电池放电的本质是通过HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为_____ 。
(3)CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠(NASICON),其中O2-可以在固体介质NASICON中自由移动。传感器中通过的电流越大,充入气体中CO的含量越高,请回答:

①a极电极反应式为_______ 。
②工作时,O2-由电极_______ (填“a”或“b”,下同)向电极_______ 移动。
(4)利用电化学原理,将CO、O2和熔融K2CO3制成燃料电池,模拟工业电解法处理含 的废水,如图。电解过程中溶液中发生如下反应:
的废水,如图。电解过程中溶液中发生如下反应: +6Fe2++14H+=2Cr3++6Fe3++7H2O。
+6Fe2++14H+=2Cr3++6Fe3++7H2O。

①如图,CO在石墨Ⅰ电极放电生成Y,Y可循环使用。甲池工作时,石墨II附近发生的电极反应式为_______ 。
②甲中消耗0.12molCO,最多可以处理含
_______ mol的废水。
(1)如图利用氧化还原反应设计而成的原电池:

①左边烧杯内发生
②右边烧杯内的电极反应式是
③外电路中电子的流向是
④电池总反应离子方程式是
 溶液和琼脂,其作用是
溶液和琼脂,其作用是(2)HCOOH燃料电池。研究HCOOH燃料电池性能的装置如图-2所示,两电极区间用允许K+、H+通过的半透膜隔开。

①电池负极电极反应式为
②图-2所示的HCOOH燃料电池放电的本质是通过HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为
(3)CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠(NASICON),其中O2-可以在固体介质NASICON中自由移动。传感器中通过的电流越大,充入气体中CO的含量越高,请回答:

①a极电极反应式为
②工作时,O2-由电极
(4)利用电化学原理,将CO、O2和熔融K2CO3制成燃料电池,模拟工业电解法处理含
 的废水,如图。电解过程中溶液中发生如下反应:
的废水,如图。电解过程中溶液中发生如下反应: +6Fe2++14H+=2Cr3++6Fe3++7H2O。
+6Fe2++14H+=2Cr3++6Fe3++7H2O。
①如图,CO在石墨Ⅰ电极放电生成Y,Y可循环使用。甲池工作时,石墨II附近发生的电极反应式为
②甲中消耗0.12molCO,最多可以处理含

您最近一年使用:0次
名校
解题方法
2 . 催化剂 (II)的应用,使
(II)的应用,使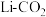 电池的研究取得了新的进展。
电池的研究取得了新的进展。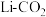 电池结构和该催化剂作用下正极反应可能的历程如下图所示。
电池结构和该催化剂作用下正极反应可能的历程如下图所示。
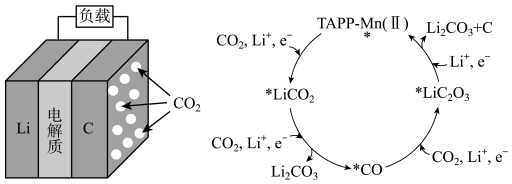
下列说法正确 的是
 (II)的应用,使
(II)的应用,使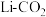 电池的研究取得了新的进展。
电池的研究取得了新的进展。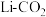 电池结构和该催化剂作用下正极反应可能的历程如下图所示。
电池结构和该催化剂作用下正极反应可能的历程如下图所示。
下列说法
| A.Li-CO2电池可使用水溶液 |
| B.放电时,Li+由正极向负极迁移 |
| C.充电时,正极反应为3CO2+4Li++4e-=2Li2CO3+C |
D.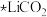 、 、 、 、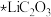 都是正极反应的中间产物 都是正极反应的中间产物 |
您最近一年使用:0次
名校
3 . 甲烷燃料电池采用铂为电极,作为化学电源进行电解实验
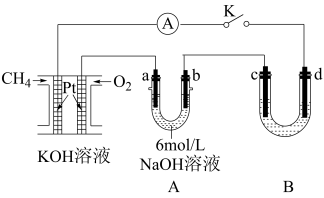
(1)写出燃料电池的正、负极反应式
负极:_______ ,
正极:_______ 。
(2)已知 A 中两个电极的材料分别为石墨和铁,用该装置可以制备高铁酸钾K2FeO4。资料显示: FeO 在溶液中呈紫红色。闭合 K,一段时间后,发现某电极附近溶液变成紫红色,该电极是
在溶液中呈紫红色。闭合 K,一段时间后,发现某电极附近溶液变成紫红色,该电极是_______ (填 a 或 b),该电极的电极反应式 为:_______ 。
(3)若 B 中的溶液为饱和 NaCl 溶液,用该装置模拟氯碱工业。
① 检验 c 电极产物的方法是:_______ 。
② 写出 d 电极的电极反应式:_______ 。
(4)若用 B 装置模拟工业粗铜精炼,则 c 极为_______ ,电解质溶液为_______ 。电解一段时间后, 电解液浓度_______ (填“变大” 、“不变”或“变小”);当燃料电池消耗标准状况下 O2的体积为 0.112L 时,理论上可以得到纯铜_______ g。

(1)写出燃料电池的正、负极反应式
负极:
正极:
(2)已知 A 中两个电极的材料分别为石墨和铁,用该装置可以制备高铁酸钾K2FeO4。资料显示: FeO
 在溶液中呈紫红色。闭合 K,一段时间后,发现某电极附近溶液变成紫红色,该电极是
在溶液中呈紫红色。闭合 K,一段时间后,发现某电极附近溶液变成紫红色,该电极是(3)若 B 中的溶液为饱和 NaCl 溶液,用该装置模拟氯碱工业。
① 检验 c 电极产物的方法是:
② 写出 d 电极的电极反应式:
(4)若用 B 装置模拟工业粗铜精炼,则 c 极为
您最近一年使用:0次
名校
解题方法
4 . 某科研小组在研究硅氧材料的电化学性能时,将硅氧材料作为正极,金属锂作为负极,非水体系的LiPF6作为电解液,起到在正、负极间传递Li+的作用,且充、放电时电解液所含的物质种类不发生变化。电池放电时的总反应为5SiO2+(4+x)Li=2Li2Si2O5+LixSi。下列说法中错误的是
| A.硅氧材料导电性差,可与石墨形成复合物以增强电极的导电性 |
| B.电池充电时,电解液中的Li+向锂电极移动 |
| C.放电时的正极反应为5SiO2+(4+x)Li++(4+x)e-=2Li2Si2O5+LixSi |
D.电池充电时,外电路转移lmol电子,则硅氧材料的质量增重 g g |
您最近一年使用:0次
2022-03-07更新
|
424次组卷
|
4卷引用:陕西省西安市西工大附中2021-2022学年高三上学期第四次适应性训练理综化学试题
名校
5 .  具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备
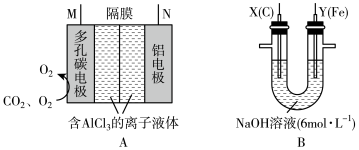
具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备 ,采用的装置如图B所示,以
,采用的装置如图B所示,以 辅助的
辅助的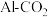 电池(如图A)为电源进行电解。
电池(如图A)为电源进行电解。
(1) 的电子式为
的电子式为___________ 。
(2)图A中正极反应式为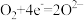 、
、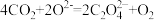 ,则该电池的总反应方程式为
,则该电池的总反应方程式为___________ 。
(3)图A中N极名称是___________ (填“正极”或“负极”),M极与图B___________ (填“X”或“Y”)极相连。
(4)电解过程中,图BX极区溶液的pH___________ (填“增大”“减小”或“不变”)。
(5)图B中两极均有气体产生,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况下的气体体积),则Y电极质量减小___________ g。
 具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备
具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备 ,采用的装置如图B所示,以
,采用的装置如图B所示,以 辅助的
辅助的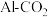 电池(如图A)为电源进行电解。
电池(如图A)为电源进行电解。
(1)
 的电子式为
的电子式为(2)图A中正极反应式为
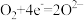 、
、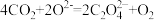 ,则该电池的总反应方程式为
,则该电池的总反应方程式为(3)图A中N极名称是
(4)电解过程中,图BX极区溶液的pH
(5)图B中两极均有气体产生,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况下的气体体积),则Y电极质量减小
您最近一年使用:0次
名校
6 . 乙醇是一种比较理想的可用于燃料电池的有机物。乙醇来源丰富,可以通过含糖有机物的发酵进行大规模的生产。下图是以乙醇燃料电池为电源,电解含NO的废气制备HNO3示意图(c、d均为石墨电极)。
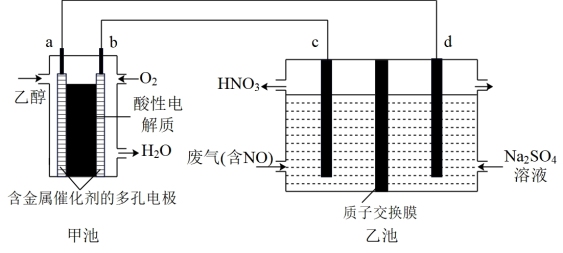
(1)请写出甲池中a极上的电极反应式:___________ 。
(2)导线中电子转移的方向为___________→___________、___________ →___________ (用a、b、c、d表示)。___________
(3)请写出乙池中c极上的电极反应式:___________ 。
(4)假设电解前,乙池两侧溶液体积均为100ml,左侧溶液中c (HNO3)为0.1 mol/L。电解结束后,左侧溶液中c (HNO3)变为0.3 mol/L,则处理NO的体积为___________ (标准状况);若忽略溶液体积变化,乙池右侧溶液的pH与电解前相比___________ (填“增大”、“减小”或“不变”)。

(1)请写出甲池中a极上的电极反应式:
(2)导线中电子转移的方向为___________→___________、___________ →___________ (用a、b、c、d表示)。
(3)请写出乙池中c极上的电极反应式:
(4)假设电解前,乙池两侧溶液体积均为100ml,左侧溶液中c (HNO3)为0.1 mol/L。电解结束后,左侧溶液中c (HNO3)变为0.3 mol/L,则处理NO的体积为
您最近一年使用:0次
2022-03-01更新
|
111次组卷
|
2卷引用:河北省保定市徐水综合高级中学2021-2022学年高二上学期第二次月考化学试题
7 . 氟离子电池因能量密度高环境友好而成为一种前景广阔的新型电池,结构如下图所示,充电时 从电极乙流向电极甲。下列说法正确的是
从电极乙流向电极甲。下列说法正确的是

 从电极乙流向电极甲。下列说法正确的是
从电极乙流向电极甲。下列说法正确的是
| A.充电时,电极甲与外加电源的正极相连 |
B.充电时,导线上每通过2mol  ,乙电极质量减少19g ,乙电极质量减少19g |
| C.放电时,电极乙为正极,发生还原反应 |
D.放电时,电极甲发生反应: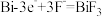 |
您最近一年使用:0次
8 . 完成下列问题
(1)绿色电源“直接二甲醚( )燃料电池”的工作原理如图所示:
)燃料电池”的工作原理如图所示:
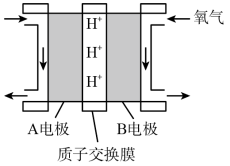
 的移动方向为由
的移动方向为由___________ (填“A”或“B”,下同)电极到___________ 电极。写出A电极的电极反应式: ___________ 。
(2) 和
和 是主要大气污染物,利用下图装置可同时吸收
是主要大气污染物,利用下图装置可同时吸收 和NO。
和NO。
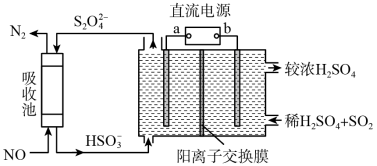
①a是直流电源的___________ 极。
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为___________ 。
③用离子方程式表示吸收NO的原理___________ 。
(1)绿色电源“直接二甲醚(
 )燃料电池”的工作原理如图所示:
)燃料电池”的工作原理如图所示:
 的移动方向为由
的移动方向为由(2)
 和
和 是主要大气污染物,利用下图装置可同时吸收
是主要大气污染物,利用下图装置可同时吸收 和NO。
和NO。
①a是直流电源的
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为
③用离子方程式表示吸收NO的原理
您最近一年使用:0次
名校
9 . I.观察下列装置,回答下列问题:
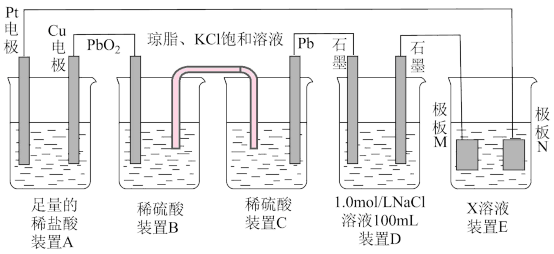
(1)装置B中PbO2上发生的电极反应式为___________ 。
(2)装置A总反应的离子方程式为___________ 。
(3)若装置E中的目的是在Cu材料上镀银,则溶液X为___________ ,极板N的材料为___________ ,极板M处的电极反应式为___________ 。
(4)当装置A中Cu电极质量改变6.4g时,装置D中产生气体体积为___________ L(标况下,不考虑气体的溶解)。
II.电解Na2CO3溶液,原理如图所示。
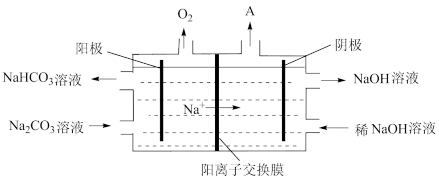
(5)阳极的电极反应式为___________ ,阴极产生的物质A的化学式为___________ 。

(1)装置B中PbO2上发生的电极反应式为
(2)装置A总反应的离子方程式为
(3)若装置E中的目的是在Cu材料上镀银,则溶液X为
(4)当装置A中Cu电极质量改变6.4g时,装置D中产生气体体积为
II.电解Na2CO3溶液,原理如图所示。

(5)阳极的电极反应式为
您最近一年使用:0次
10 . 利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g)
CH3OH(g) 
②CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 
③CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g) 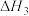
回答下列问题:
(1)反应①的化学平衡常数K的表达式为___________ 。
(2)已知反应①中相关的化学键键能数据如下:
由此计算 =
=___________ kJ·mol-1,已知 =-58kJ·mol-1,则
=-58kJ·mol-1,则 =
=___________ kJ·mol-1。
(3)科学家提出制备合成气反应历程分两步:
反应①:CH4(g)=C(ads)+2H2(g)(慢反应)
反应②:C(ads)+CO2(g)=2CO(g)(快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图所示:
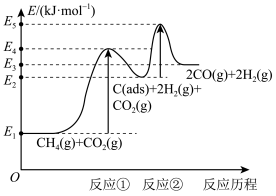
CH4与CO2制备合成气的热化学方程式为___________ 。
(4)利用铜基配合物1,10—phenanthroline—Cu催化剂电催化CO2还原制备碳基燃料(包括CO、烷烃和酸等)是减少CO2在大气中累积和实现可再生能源有效利用的关键手段之一,其装置原理如图所示。
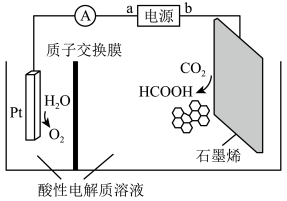
①该装置工作过程中,图中Pt电极附近溶液的pH___________ (填“变大”或“变小”),每转移2mol电子,阴极室溶液质量增加___________ g。
②阴极的电极反应式为___________ 。
③若该电源为铅蓄电池,当向外电路每提供2mol电子,理论上消耗硫酸的质量为___________ g。
④该装置工作过程中阳极的电极反应式为___________ 。
①CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g) 
②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 
③CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g) 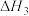
回答下列问题:
(1)反应①的化学平衡常数K的表达式为
(2)已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算
 =
= =-58kJ·mol-1,则
=-58kJ·mol-1,则 =
=(3)科学家提出制备合成气反应历程分两步:
反应①:CH4(g)=C(ads)+2H2(g)(慢反应)
反应②:C(ads)+CO2(g)=2CO(g)(快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图所示:

CH4与CO2制备合成气的热化学方程式为
(4)利用铜基配合物1,10—phenanthroline—Cu催化剂电催化CO2还原制备碳基燃料(包括CO、烷烃和酸等)是减少CO2在大气中累积和实现可再生能源有效利用的关键手段之一,其装置原理如图所示。

①该装置工作过程中,图中Pt电极附近溶液的pH
②阴极的电极反应式为
③若该电源为铅蓄电池,当向外电路每提供2mol电子,理论上消耗硫酸的质量为
④该装置工作过程中阳极的电极反应式为
您最近一年使用:0次



