1 . 电化学原理在现实生活中有着十分广泛的应用。请回答下列问题:
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述_______ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为_______ 。
(2)电镀在工业上有着广泛的应用,可以镀锌、镀铜、镀金等。利用如图所示装置可以将铜牌变为银牌,即在铜牌表面电镀一层银,该电解池的阴极反应可表示为_______ 。

(3)钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含 的水溶液制备金属钴,其装置如图甲、乙。
的水溶液制备金属钴,其装置如图甲、乙。

①图乙中Co电极应连接乙醇燃料电池的_______ 极(填“a”或“b”。
②图甲中a极上发生的电极反应是_______ 。
③生成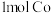 ,Ⅰ室溶液质量理论上减少
,Ⅰ室溶液质量理论上减少_______ g。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)电镀在工业上有着广泛的应用,可以镀锌、镀铜、镀金等。利用如图所示装置可以将铜牌变为银牌,即在铜牌表面电镀一层银,该电解池的阴极反应可表示为

(3)钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含
 的水溶液制备金属钴,其装置如图甲、乙。
的水溶液制备金属钴,其装置如图甲、乙。
①图乙中Co电极应连接乙醇燃料电池的
②图甲中a极上发生的电极反应是
③生成
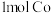 ,Ⅰ室溶液质量理论上减少
,Ⅰ室溶液质量理论上减少
您最近一年使用:0次
2022-01-16更新
|
228次组卷
|
2卷引用:福建省宁德市2021-2022学年高二上学期期末质量检测化学试题1
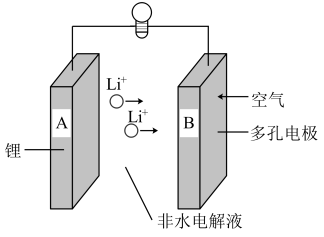
2 . 锂空气充电电池有望成为电池行业的“明日之星”,其放电时的工作原理如图所示。已知电池反应: 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是
| A.电池工作时,正极的电极反应式:O2+2e-+2Li+=Li2O2 |
| B.放电时,B极消耗22.4L的O2,外电路中通过2mol电子 |
| C.充电时,B电极上的电势比A电极上的高 |
| D.充电时,A极接电源的负极 |
您最近一年使用:0次
2022-01-16更新
|
140次组卷
|
2卷引用:福建省宁德市2021-2022学年高二上学期期末质量检测化学试题1
3 . 如图所示,某化学兴趣小组设计了一个燃料电池,并探究氯碱工业原理和粗铜精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:
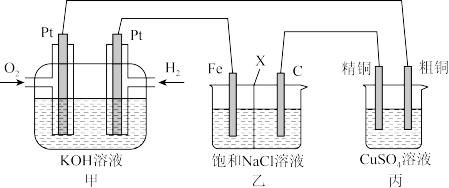
(1)甲装置中通氢气一极的电极反应式为______ 。
(2)乙装置中铁电极为______ 极,该装置中的电解反应方程式为______ 。
(3)若有1.12L(标准状况下)氧气参与反应,丙装置中阴极增重的质量为______ g。
(4)某粗铜中含有铁、金、银等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如图工艺流程:.
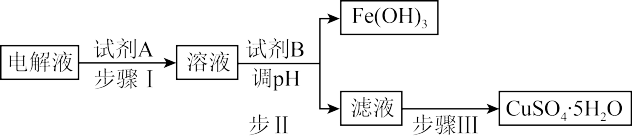
已知:几种金属阳离子开始沉淀和沉淀完全的pH:
①步骤I中加入的试剂A应选择______ (填序号)。
a.氯气 b.过氧化氢 c.酸性高锰酸钾溶液
②步骤II中调节pH的范围是______ 。
③步骤III的操作是加热浓缩、______ 、______ 。

(1)甲装置中通氢气一极的电极反应式为
(2)乙装置中铁电极为
(3)若有1.12L(标准状况下)氧气参与反应,丙装置中阴极增重的质量为
(4)某粗铜中含有铁、金、银等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如图工艺流程:.

已知:几种金属阳离子开始沉淀和沉淀完全的pH:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
a.氯气 b.过氧化氢 c.酸性高锰酸钾溶液
②步骤II中调节pH的范围是
③步骤III的操作是加热浓缩、
您最近一年使用:0次
4 . 中国科学院研发了一种新型钾电池,有望成为锂电池的替代品。该电池的电解质为CF3SO3K溶液,其简要组成如图所示。电池放电时的总反为:2KC14H10+xMnFe(CN)6=2K1-xC14H10+xK2MnFe(CN)6。电池工作中下列说法中正确的是
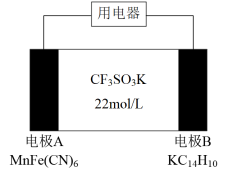
| A.正极反应为 :2K+ + 2e- + MnFe(CN)6 =K2MnFe(CN)6 |
| B.电极B质量增加,电极A质量减少 |
| C.CF3SO3K溶液的浓度变大 |
| D.电子从电极A经过CF3SO3K溶液流向电极B |
您最近一年使用:0次
2022-01-11更新
|
730次组卷
|
2卷引用:湖北省部分省级示范高中2020-2021学年高一下学期期末测试化学试题
名校
5 . 以二甲醚(CH3OCH3)一空气燃料电池为电源进行如下实验,装置如图所示。用装置D精炼粗银,e电极为粗银(含有铁、铜杂质)。其他电极均为石墨。B、C、D装置中溶液体积均为100mL,忽略反应前后溶液体积变化(装置中电解质溶液都过量)。
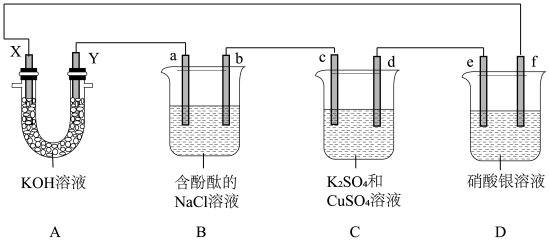
请回答下列问题:
(1)f极材料是___________ ;d极名称是___________ ;a极发生___________ (填“氧化”或“还原”)反应。
(2)写出X极的电极反应式:___________ 。
(3)b极附近可能的现象是___________ 。
(4)已知f极净增质量为21.6g时,C装置两极收集的气体体积(同温同压下)相同,则原溶液中c(CuSO4)=___________ 。

请回答下列问题:
(1)f极材料是
(2)写出X极的电极反应式:
(3)b极附近可能的现象是
(4)已知f极净增质量为21.6g时,C装置两极收集的气体体积(同温同压下)相同,则原溶液中c(CuSO4)=
您最近一年使用:0次
名校
6 . 电化学原理在生产生活中具有广泛的应用。
I.某研究性小组进行以下相关探究。
实验Ⅰ:用图1装置电解CuCl2溶液产生的氯气通入NaOH溶液来制取少量漂白液:

(1)导气管W端应与出气口__ 连接(填“X”或“Y”),写出制取漂白液的化学方程式___ 。
(2)实验后发现阴极碳棒上除了附着有红色物质,还附着有少量白色物质。查阅资料显示:
化学小组分析提出:①白色物质为CuCl。②红色物质可能有:__ 或者Cu2O;或者二者混合物。
实验Ⅱ:为探究阴极碳棒上附着的红色、白色物质,设计了如图实验:取出阴极碳棒,洗涤、干燥,并将其放入图2所示装置b中,进行实验。
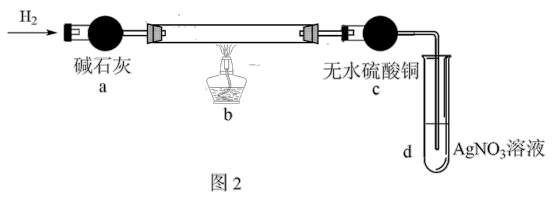
实验中,碳棒上的白色物质完全变为红色,无水硫酸铜不变色,d中出现白色沉淀。
(3)无水硫酸铜的作用是___ 。
(4)装置b中发生反应的化学方程式是___ 。
(5)电解CuCl2溶液时,阴极上产生白色物质的原因为___ (用电极反应式解释)。
Ⅱ.图甲是厨房用的天然气报警器,核心是气体传感器。当传感器遇到的甲烷达到一定浓度时,随之产生电信号并联动报警。工作原理类似燃料电池的工作原理,其装置如图乙所示。其中O2-可以在固体电解质ZrO2—Na2O中自由移动。回答下列问题。

(6)报警器触发工作时,多孔电极a极的电极反应式为___ 。
(7)O2-在传感器中移向电极__ (填“a”或“b”),当标准状况下56mL的甲烷在多孔电极a完全反应时,流入传感控制器电路的电子有__ mol。
I.某研究性小组进行以下相关探究。
实验Ⅰ:用图1装置电解CuCl2溶液产生的氯气通入NaOH溶液来制取少量漂白液:

(1)导气管W端应与出气口
(2)实验后发现阴极碳棒上除了附着有红色物质,还附着有少量白色物质。查阅资料显示:
| 物质名称及化学式 | 氯化亚铜CuCl | 碱式碳酸铜Cu2(OH)3Cl |
| 性质 | 白色固体、不溶于水 | 绿色固体、不溶于水 |
化学小组分析提出:①白色物质为CuCl。②红色物质可能有:
实验Ⅱ:为探究阴极碳棒上附着的红色、白色物质,设计了如图实验:取出阴极碳棒,洗涤、干燥,并将其放入图2所示装置b中,进行实验。

图2
实验中,碳棒上的白色物质完全变为红色,无水硫酸铜不变色,d中出现白色沉淀。
(3)无水硫酸铜的作用是
(4)装置b中发生反应的化学方程式是
(5)电解CuCl2溶液时,阴极上产生白色物质的原因为
Ⅱ.图甲是厨房用的天然气报警器,核心是气体传感器。当传感器遇到的甲烷达到一定浓度时,随之产生电信号并联动报警。工作原理类似燃料电池的工作原理,其装置如图乙所示。其中O2-可以在固体电解质ZrO2—Na2O中自由移动。回答下列问题。

(6)报警器触发工作时,多孔电极a极的电极反应式为
(7)O2-在传感器中移向电极
您最近一年使用:0次
7 . 熔融盐燃料电池具有高的发电效率,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,制得在650℃下工作的燃料电池做电源处理废水中的NH4NO3,模拟装置如图所示,a连接熔融盐电池中通氧气的电极,下列说法正确的是
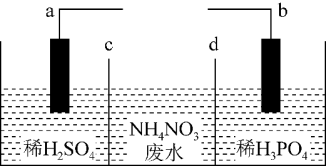

A.熔融盐电池工作时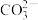 移向通氧气的电极 移向通氧气的电极 |
| B.b的电极反应式为:4OH--4e-=2H2O+O2↑ |
| C.c、d均是阳离子交换膜 |
| D.若a为Fe,工作一段时间该极区溶液变成棕黄色 |
您最近一年使用:0次
解题方法
8 . 铁铬液流电池是一种在酸性介质中,正、负极活性物质均为液体的电池,其工作原理如图所示,已知:氧化性:Fe3+>Cr3+。下列说法错误的是
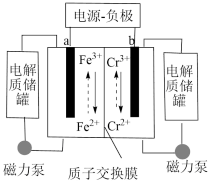

| A.放电时,电子由a电极经负载流向b电极 |
| B.放电时,电池的总反应为:Cr2++Fe3+=Cr3++Fe2+ |
| C.充电时,阴极电极反应式为:Cr3++e—=Cr2+ |
| D.充电时,H+由左侧电极室经交换膜移向右侧 |
您最近一年使用:0次
名校
9 . 利用CH4燃料电池电解制备Ca(H2PO4)2,并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法不正确的是
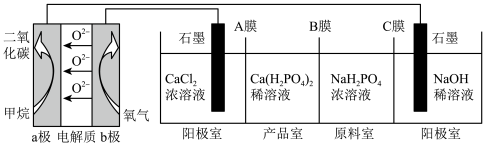

| A.a极反应:CH4-8e-+4O2-=CO2+2H2O |
| B.a极上通入标况下2.24L甲烷,阳极室Ca2+减少0.4mol |
| C.可用铁电极替换阴极的石墨电极 |
| D.A膜和C膜均为阴离子交换膜 |
您最近一年使用:0次
2022-01-05更新
|
118次组卷
|
2卷引用:山西省山西大学附属中学2021-2022学年高三上学期10月模块诊断考试化学试题
名校
解题方法
10 . 有机物液流电池因其电化学性能可调控等优点而备受关注。某研究团队设计了一种水系分散的聚合物微粒“泥浆"电池如图1所示。该电池在充电过程中聚对苯二酚(图2)被氧化。下列说法正确的是
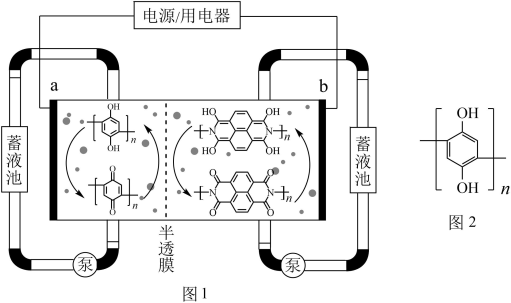

| A.充电时,a电极附近的pH增大 |
| B.放电时,电子由a电极流向b电极 |
| C.聚对苯二酚可以通过电池中间的半透膜 |
D.放电时,b电极的电极反应方程式为: -4ne-= -4ne-=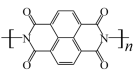 +4nH+ +4nH+ |
您最近一年使用:0次
2022-01-03更新
|
1238次组卷
|
2卷引用:广西玉林市、贵港市2021-2022学年高三上学期12月联合模拟考试理科综合化学试题



