利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g)
CH3OH(g) 
②CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 
③CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g) 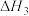
回答下列问题:
(1)反应①的化学平衡常数K的表达式为___________ 。
(2)已知反应①中相关的化学键键能数据如下:
由此计算 =
=___________ kJ·mol-1,已知 =-58kJ·mol-1,则
=-58kJ·mol-1,则 =
=___________ kJ·mol-1。
(3)科学家提出制备合成气反应历程分两步:
反应①:CH4(g)=C(ads)+2H2(g)(慢反应)
反应②:C(ads)+CO2(g)=2CO(g)(快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图所示:
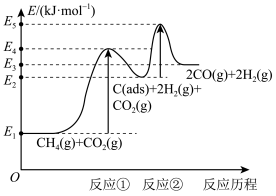
CH4与CO2制备合成气的热化学方程式为___________ 。
(4)利用铜基配合物1,10—phenanthroline—Cu催化剂电催化CO2还原制备碳基燃料(包括CO、烷烃和酸等)是减少CO2在大气中累积和实现可再生能源有效利用的关键手段之一,其装置原理如图所示。
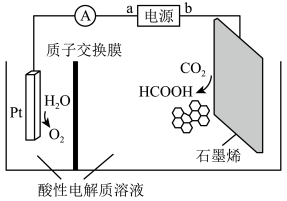
①该装置工作过程中,图中Pt电极附近溶液的pH___________ (填“变大”或“变小”),每转移2mol电子,阴极室溶液质量增加___________ g。
②阴极的电极反应式为___________ 。
③若该电源为铅蓄电池,当向外电路每提供2mol电子,理论上消耗硫酸的质量为___________ g。
④该装置工作过程中阳极的电极反应式为___________ 。
①CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g) 
②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 
③CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g) 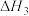
回答下列问题:
(1)反应①的化学平衡常数K的表达式为
(2)已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算
 =
= =-58kJ·mol-1,则
=-58kJ·mol-1,则 =
=(3)科学家提出制备合成气反应历程分两步:
反应①:CH4(g)=C(ads)+2H2(g)(慢反应)
反应②:C(ads)+CO2(g)=2CO(g)(快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图所示:

CH4与CO2制备合成气的热化学方程式为
(4)利用铜基配合物1,10—phenanthroline—Cu催化剂电催化CO2还原制备碳基燃料(包括CO、烷烃和酸等)是减少CO2在大气中累积和实现可再生能源有效利用的关键手段之一,其装置原理如图所示。

①该装置工作过程中,图中Pt电极附近溶液的pH
②阴极的电极反应式为
③若该电源为铅蓄电池,当向外电路每提供2mol电子,理论上消耗硫酸的质量为
④该装置工作过程中阳极的电极反应式为
2021·河北衡水·模拟预测 查看更多[4]
河北省衡水中学2021-2022学年高三上学期五调考试化学试题(已下线)二轮拔高卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(天津专用)(已下线)【直击双一流】09-备战2022年高考化学名校进阶模拟卷(通用版)(已下线)押江苏卷第18题 化学反应原理综合题 -备战2022年高考化学临考题号押题(江苏卷)
更新时间:2022-02-22 20:20:06
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质,请回答下列问题:
(1)知25℃和101KPa时,液态甲醇( )的燃烧热
)的燃烧热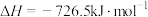 。请写出表示甲醇燃烧热的热化学方程式
。请写出表示甲醇燃烧热的热化学方程式___________ 。
(2) 资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使
资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使 转化为
转化为 。反应体系中主要反应的热化学方程式为:
。反应体系中主要反应的热化学方程式为:
反应Ⅰ: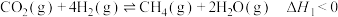
反应Ⅱ: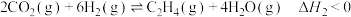
①将反应后气体通入___________ (填试剂名称),可证明反应Ⅱ发生。
②计算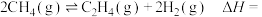
___________ (用 和
和 表示)
表示)
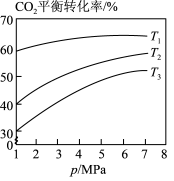
③相同投料比时,体系内 的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为___________ 。
(3)镍氢催化剂活性因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应:
积碳反应:
消碳反应:
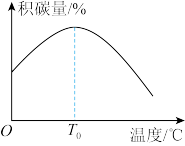
其他条件相同时,催化剂表面积碳量与温度的关系如图所示, ℃之后,温度升高积碳量减小的主要原因
℃之后,温度升高积碳量减小的主要原因___________ 。
(1)知25℃和101KPa时,液态甲醇(
 )的燃烧热
)的燃烧热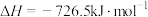 。请写出表示甲醇燃烧热的热化学方程式
。请写出表示甲醇燃烧热的热化学方程式(2)
 资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使
资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使 转化为
转化为 。反应体系中主要反应的热化学方程式为:
。反应体系中主要反应的热化学方程式为:反应Ⅰ:
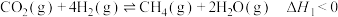
反应Ⅱ:
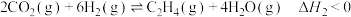
①将反应后气体通入
②计算
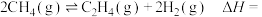
 和
和 表示)
表示)③相同投料比时,体系内
 的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
(3)镍氢催化剂活性因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应:

积碳反应:

消碳反应:

其他条件相同时,催化剂表面积碳量与温度的关系如图所示,
 ℃之后,温度升高积碳量减小的主要原因
℃之后,温度升高积碳量减小的主要原因
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】 是一种丰富的碳资源,将清洁转化为高附加值化学品以实现资源利用是研究热点。
是一种丰富的碳资源,将清洁转化为高附加值化学品以实现资源利用是研究热点。
I.合成甲醇
在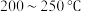 的
的 加氢反应器中,主要反应有:
加氢反应器中,主要反应有:
反应i
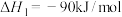
反应ii
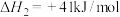
反应iii

(1)
______ KJ/mol。
(2)同时也存在副反应iv: ,反应器进行一段时间后要间歇降到室温,可提高甲醇的产率。对比反应iii、iv,解释其原因
,反应器进行一段时间后要间歇降到室温,可提高甲醇的产率。对比反应iii、iv,解释其原因______ 。(已知 的沸点为
的沸点为 的沸点为
的沸点为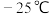 )
)
Ⅱ.甲醇的综合利用:以 和甲醇为原料直接合成碳酸二甲酯
和甲醇为原料直接合成碳酸二甲酯 。
。
反应v
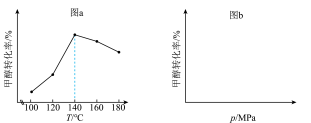
(3)在不同的实验条件下,测定甲醇的转化率。温度的数据结果为图a,压强的数据结果在图b中未画出。
①反应 的
的
______ 0(填“>”或“<”)。
②在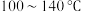 之间,随着温度升高,甲醇转化率增大的原因是
之间,随着温度升高,甲醇转化率增大的原因是______ 。
③在图b中绘制出压强和甲醇转化率之间的关系(作出趋势即可)______ 。
 是一种丰富的碳资源,将清洁转化为高附加值化学品以实现资源利用是研究热点。
是一种丰富的碳资源,将清洁转化为高附加值化学品以实现资源利用是研究热点。I.合成甲醇

在
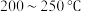 的
的 加氢反应器中,主要反应有:
加氢反应器中,主要反应有:反应i

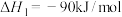
反应ii

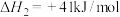
反应iii


(1)

(2)同时也存在副反应iv:
 ,反应器进行一段时间后要间歇降到室温,可提高甲醇的产率。对比反应iii、iv,解释其原因
,反应器进行一段时间后要间歇降到室温,可提高甲醇的产率。对比反应iii、iv,解释其原因 的沸点为
的沸点为 的沸点为
的沸点为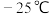 )
)Ⅱ.甲醇的综合利用:以
 和甲醇为原料直接合成碳酸二甲酯
和甲醇为原料直接合成碳酸二甲酯 。
。反应v

(3)在不同的实验条件下,测定甲醇的转化率。温度的数据结果为图a,压强的数据结果在图b中未画出。
①反应
 的
的
②在
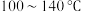 之间,随着温度升高,甲醇转化率增大的原因是
之间,随着温度升高,甲醇转化率增大的原因是③在图b中绘制出压强和甲醇转化率之间的关系(作出趋势即可)

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】不同的化学反应具有不同的反应热,人们可以通过不同的方法获得反应热数据,可以实验测定,也可以理论推算。
(1)已知:在稀溶液中,强酸与强碱发生中和反应生成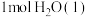 时释放的热量为
时释放的热量为 ,若改用醋酸与氢氧化钠溶液进行测量中和热,测量值
,若改用醋酸与氢氧化钠溶液进行测量中和热,测量值_______ (填偏大或偏小),写出醋酸电离方程式并分析误差原因_______ ,某化学兴趣小组用盐酸, 溶液(稍过量)进行中和热测定,计算结果
溶液(稍过量)进行中和热测定,计算结果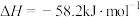 ,其原因可能是
,其原因可能是_______ 。(填字母标号)
A.盐酸与 溶液混合后立即记录温度 B.分三次将盐酸溶液缓慢倒入
溶液混合后立即记录温度 B.分三次将盐酸溶液缓慢倒入 溶液中
溶液中
C.用量筒量取盐酸时仰视读数 D.使用玻璃搅拌器搅拌
(2)标准状况下,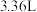 仅由C、H两种元素组成的某气体质量为
仅由C、H两种元素组成的某气体质量为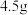 ,在25℃和
,在25℃和 下完全燃烧生成
下完全燃烧生成 和
和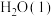 时,放出
时,放出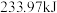 的热量。
的热量。
①该气体的分子式为_______ 。
②表示该气体燃烧热的热化学方程式为_______
(3)2022年北京冬奥会用 作为火炬燃料,而热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下所示:
作为火炬燃料,而热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下所示:
反应I:
反应II: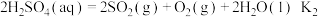
反应I: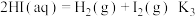
则反应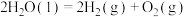

_______ 。(用 表示)
表示)
2008年北京奥运会火炬燃料是丙烷( ),已知丙烷的燃烧热为
),已知丙烷的燃烧热为 ,氢气的燃烧热为
,氢气的燃烧热为 。室温下将
。室温下将 (已折算为标准状况下体积)
(已折算为标准状况下体积) 和
和 的混合气体完全燃烧,共放
的混合气体完全燃烧,共放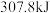 热量,则该混合气体中
热量,则该混合气体中 和
和 的体积比为
的体积比为_______ 。
(1)已知:在稀溶液中,强酸与强碱发生中和反应生成
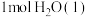 时释放的热量为
时释放的热量为 ,若改用醋酸与氢氧化钠溶液进行测量中和热,测量值
,若改用醋酸与氢氧化钠溶液进行测量中和热,测量值 溶液(稍过量)进行中和热测定,计算结果
溶液(稍过量)进行中和热测定,计算结果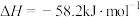 ,其原因可能是
,其原因可能是A.盐酸与
 溶液混合后立即记录温度 B.分三次将盐酸溶液缓慢倒入
溶液混合后立即记录温度 B.分三次将盐酸溶液缓慢倒入 溶液中
溶液中C.用量筒量取盐酸时仰视读数 D.使用玻璃搅拌器搅拌
(2)标准状况下,
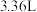 仅由C、H两种元素组成的某气体质量为
仅由C、H两种元素组成的某气体质量为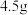 ,在25℃和
,在25℃和 下完全燃烧生成
下完全燃烧生成 和
和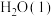 时,放出
时,放出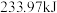 的热量。
的热量。①该气体的分子式为
②表示该气体燃烧热的热化学方程式为
(3)2022年北京冬奥会用
 作为火炬燃料,而热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下所示:
作为火炬燃料,而热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下所示:反应I:

反应II:
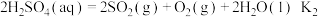
反应I:
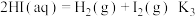
则反应
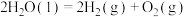

 表示)
表示)2008年北京奥运会火炬燃料是丙烷(
 ),已知丙烷的燃烧热为
),已知丙烷的燃烧热为 ,氢气的燃烧热为
,氢气的燃烧热为 。室温下将
。室温下将 (已折算为标准状况下体积)
(已折算为标准状况下体积) 和
和 的混合气体完全燃烧,共放
的混合气体完全燃烧,共放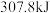 热量,则该混合气体中
热量,则该混合气体中 和
和 的体积比为
的体积比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】300℃下,在一密闭容器中充入一定量的 与
与 发生反应:
发生反应: ,一段时间后反应达平衡;若其他条件不变,温度从300℃升至500℃,反应重新达到平衡时,
,一段时间后反应达平衡;若其他条件不变,温度从300℃升至500℃,反应重新达到平衡时, 的体积分数增加。
的体积分数增加。
(1)下列说法正确的是_______(填字母)。
(2)一定条件下,反应体系中 平衡转化率
平衡转化率 与L和X的关系如图所示,L和X表示温度或压强。
与L和X的关系如图所示,L和X表示温度或压强。
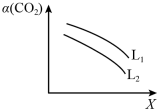
①X表示的物理量是_______ 。
②
_______  (填“<”或“>”)。
(填“<”或“>”)。
(3)一定量的 与足量的C在恒压密闭容器中发生反应:
与足量的C在恒压密闭容器中发生反应: ,平衡时体系中气体体积分数与温度的关系如图所示,回答下列问题:
,平衡时体系中气体体积分数与温度的关系如图所示,回答下列问题:
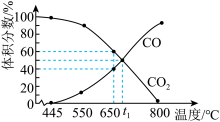
①650℃时 的平衡转化率为
的平衡转化率为_______ 。
② ℃时反应达到平衡状态,若再充入等物质的量的CO和
℃时反应达到平衡状态,若再充入等物质的量的CO和 气体,则平衡
气体,则平衡_______ (填“正向”“逆向”或“不”)移动。
 与
与 发生反应:
发生反应: ,一段时间后反应达平衡;若其他条件不变,温度从300℃升至500℃,反应重新达到平衡时,
,一段时间后反应达平衡;若其他条件不变,温度从300℃升至500℃,反应重新达到平衡时, 的体积分数增加。
的体积分数增加。(1)下列说法正确的是_______(填字母)。
A.该反应的 |
B.平衡常数大小: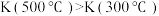 |
C.300℃下,减小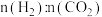 的比值, 的比值, 平衡转化率升高 平衡转化率升高 |
D.反应达到平衡时 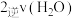 |
 平衡转化率
平衡转化率 与L和X的关系如图所示,L和X表示温度或压强。
与L和X的关系如图所示,L和X表示温度或压强。
①X表示的物理量是
②

 (填“<”或“>”)。
(填“<”或“>”)。(3)一定量的
 与足量的C在恒压密闭容器中发生反应:
与足量的C在恒压密闭容器中发生反应: ,平衡时体系中气体体积分数与温度的关系如图所示,回答下列问题:
,平衡时体系中气体体积分数与温度的关系如图所示,回答下列问题:
①650℃时
 的平衡转化率为
的平衡转化率为②
 ℃时反应达到平衡状态,若再充入等物质的量的CO和
℃时反应达到平衡状态,若再充入等物质的量的CO和 气体,则平衡
气体,则平衡
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氮及其化合物在工农业生产、生活中有着重要的作用,请回答。
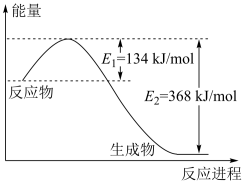
(1)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式___________ 。
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)⇌ 2NH3(g) ΔH<0,其化学平衡常数K与温度的关系如表:
完成下列问题:
①比较K1、K2的大小:K1___________ K2(填“>”、“=”或“<”);
②判断该反应达到化学平衡状态的依据是___________ (填序号);
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(3)25℃时,水的电离达到平衡:H2O⇌H++OH- ∆H>0,下列叙述正确的是___________
(4)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
①写出盐酸肼第一步水解反应的离子方程式___________ 。
②盐酸肼水溶液中离子浓度的排列顺序正确的是___________ (填序号)。
A.c(Cl-)>c(N2H )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.c(Cl-)>c([N2H5•H2O]+)>c(H+)>c(OH-)
C.2c(N2H )+c([N2H5•H2O]+)+c(H+)=c(Cl-)+c(OH-)
)+c([N2H5•H2O]+)+c(H+)=c(Cl-)+c(OH-)
D.c(N2H )>c(Cl-)>c(H+)>c(OH-)
)>c(Cl-)>c(H+)>c(OH-)
(1)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式

(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)⇌ 2NH3(g) ΔH<0,其化学平衡常数K与温度的关系如表:
| 温度(℃) | 25 | 125 | 225 | … |
| 平衡常数 | 4.1×106 | K1 | K2 | … |
完成下列问题:
①比较K1、K2的大小:K1
②判断该反应达到化学平衡状态的依据是
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(3)25℃时,水的电离达到平衡:H2O⇌H++OH- ∆H>0,下列叙述正确的是___________
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
①写出盐酸肼第一步水解反应的离子方程式
②盐酸肼水溶液中离子浓度的排列顺序正确的是
A.c(Cl-)>c(N2H
 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)B.c(Cl-)>c([N2H5•H2O]+)>c(H+)>c(OH-)
C.2c(N2H
 )+c([N2H5•H2O]+)+c(H+)=c(Cl-)+c(OH-)
)+c([N2H5•H2O]+)+c(H+)=c(Cl-)+c(OH-)D.c(N2H
 )>c(Cl-)>c(H+)>c(OH-)
)>c(Cl-)>c(H+)>c(OH-)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】CO和H2可作为能源和化工原料,应用十分广泛。
(1)已知:C(s)+O2(g)===CO2(g)ΔH1=-393.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g)ΔH2=-483.6 kJ·mol-1
C(s)+H2O(g)===CO(g)+H2(g)ΔH3=131.3 kJ·mol-1
则反应CO(g)+H2(g)+O2(g)===H2O(g)+CO2(g)的ΔH=________ kJ·mol-1。标准状况下的煤气(CO、H2)44.8 L与氧气反应生成CO2和H2O,反应过程中转移________ mol电子。
(2)密闭容器中充有10 mol CO与20 mol H2,在催化剂作用下反应生成甲醇:
CO(g)+2H2(g) CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如图所示。
CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如图所示。
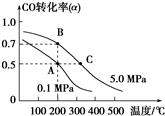
①若A、B两点表示在某时刻达到的平衡状态,此时在B点时容器的体积为6 L,则该温度下的平衡常数K=________ ;此时在A点时容器的体积VA_______ 6 L(填“大于”“小于”或“等于”)。该反应为________ (填“放热反应”或“吸热反应”)。
②若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA________ tC(填“大于”“小于”或“等于”)。
(1)已知:C(s)+O2(g)===CO2(g)ΔH1=-393.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g)ΔH2=-483.6 kJ·mol-1
C(s)+H2O(g)===CO(g)+H2(g)ΔH3=131.3 kJ·mol-1
则反应CO(g)+H2(g)+O2(g)===H2O(g)+CO2(g)的ΔH=
(2)密闭容器中充有10 mol CO与20 mol H2,在催化剂作用下反应生成甲醇:
CO(g)+2H2(g)
 CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如图所示。
CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如图所示。
①若A、B两点表示在某时刻达到的平衡状态,此时在B点时容器的体积为6 L,则该温度下的平衡常数K=
②若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g),△H=-1275.6 kJ/mol
②2CO(g)+O2(g)=2CO2(g), △H=-566.0kJ/mol
③H2O(g)=H2O(l), △H=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式__________________ 。
(2)某实验小组依据甲醇燃烧的反应原理,设计如图所示的装置。
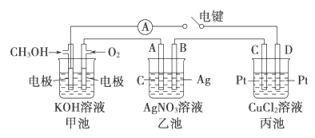
①甲池负极的电极反应为__________________ 。
②工作一段时间后,测得甲中溶液的pH减小,该电池总反应的离子方程式为______ 。
③乙池中A(石墨)电极的名称为__________________ (填“正极”、“负极”或“阴极”、“阳极”),乙池中总反应式为_________ 。
④当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为__ mL(标准状况),假设乙池、丙池中的溶液均为足量,丙池中____ (填“C”或“D”)极析出______ g铜。
(1)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g),△H=-1275.6 kJ/mol
②2CO(g)+O2(g)=2CO2(g), △H=-566.0kJ/mol
③H2O(g)=H2O(l), △H=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式
(2)某实验小组依据甲醇燃烧的反应原理,设计如图所示的装置。

①甲池负极的电极反应为
②工作一段时间后,测得甲中溶液的pH减小,该电池总反应的离子方程式为
③乙池中A(石墨)电极的名称为
④当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:
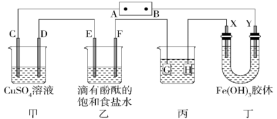
(1)若AB电源是甲醇在酸性环境的燃料电池,则甲中C极的电极反应式为___________ 。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为___________ 。
(3)丙是一个给铜件镀银的装置,当乙中溶液的c(OH-)=0.1mol/L时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为___________ g。
Ⅱ.某同学用稀硝酸和铜反应制NO,发现化学反应速率较慢,因此改用浓硝酸按下图所示装置制取NO。
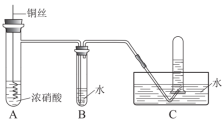
(1)浓硝酸一般盛放在棕色试剂瓶中,原因是___________ 。
(2)B中反应的化学方程式是___________ 。

(1)若AB电源是甲醇在酸性环境的燃料电池,则甲中C极的电极反应式为
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为
(3)丙是一个给铜件镀银的装置,当乙中溶液的c(OH-)=0.1mol/L时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为
Ⅱ.某同学用稀硝酸和铜反应制NO,发现化学反应速率较慢,因此改用浓硝酸按下图所示装置制取NO。

(1)浓硝酸一般盛放在棕色试剂瓶中,原因是
(2)B中反应的化学方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞 (如图1)。
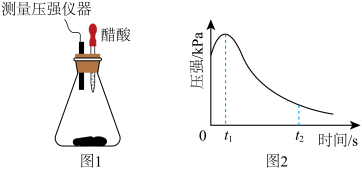
从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了____________ 腐蚀,此时,碳粉表面发生的电极反应式是____________ 。
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确 的是______ 。
A.太阳光催化分解水制氢气比电解水制氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的总反应式相同
(3)电动车采用了一种高效耐用的新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
①该电池放电时负极电极反应式为_________ ;
②充电时阳极电极反应式为_______ 。
(4)下列描述中,符合生产实际的是( )
A. 电解食盐水制得金属钠 B. 电解熔融氯化铝制取金属铝,用石墨作阳极
C. 一氧化碳高温还原铁矿石制得铁 D.电解熔融氧化镁制取金属镁,用铁作阳极
(5)金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)( )
A.阴极发生还原反应,其电极反应式:Ni2++2e-=Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt

从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法
A.太阳光催化分解水制氢气比电解水制氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的总反应式相同
(3)电动车采用了一种高效耐用的新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。①该电池放电时负极电极反应式为
②充电时阳极电极反应式为
(4)下列描述中,符合生产实际的是
A. 电解食盐水制得金属钠 B. 电解熔融氯化铝制取金属铝,用石墨作阳极
C. 一氧化碳高温还原铁矿石制得铁 D.电解熔融氧化镁制取金属镁,用铁作阳极
(5)金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)
A.阴极发生还原反应,其电极反应式:Ni2++2e-=Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
您最近一年使用:0次



