解题方法
1 . 制作一个简单的燃料电池
(1)设计思路
将水电解器电解得到的氢气和氧气,通入两个石墨电极把氢气和氧气反应的化学能转化为电能。
(2)分析氢氧燃料电池的工作原理,NaOH溶液做离子导体,写出电极反应式、化学反应方程式。
负极反应式:___________ ;正极反应式___________ :总反应方程式:___________ 。
【情境问题思考】
(3)若选择稀硫酸代替NaOH溶液做做离子导体,写出电极反应式。
负极反应式:___________ ;正极反应式___________ 。
(1)设计思路
将水电解器电解得到的氢气和氧气,通入两个石墨电极把氢气和氧气反应的化学能转化为电能。
| 设计目标 | 选择实验用品及目的 | 实验装置 | 实验现象 |
| 获得氢气和氧气 | 电解水发生器:获取氢气和氧气的装置。 蒸馏水:制取氢气和氧气。 KOH溶液: | 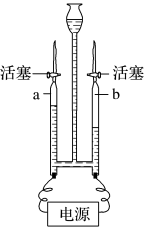 | a、b两管均产生无色气体,且体积比为 |
| 制作氢氧燃料电池 | KOH溶液:离子导体 石墨棒:做电极 U形管:发生装置 电流表、导线:检测产生的电流 | 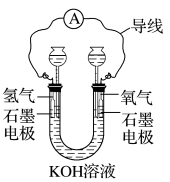 | 电流表指针 |
负极反应式:
【情境问题思考】
(3)若选择稀硫酸代替NaOH溶液做做离子导体,写出电极反应式。
负极反应式:
您最近半年使用:0次
2 . 铅蓄电池是最常见的二次电池。铅蓄电池的充、放电总反应为Pb+PbO2+2H2SO4(aq) 2PbSO4+2H2O。
2PbSO4+2H2O。


(1)放电过程,作原电池:
负极:___________ ;正极:___________ 。
(2)充电过程,作电解池:
阴极:___________ ;阳极:___________ 。
【情境问题思考】
(3)可充电的二次电池中的放电反应与充电反应是否互为可逆反应___________ ,说明理由___________ ?
 2PbSO4+2H2O。
2PbSO4+2H2O。

(1)放电过程,作原电池:
负极:
(2)充电过程,作电解池:
阴极:
【情境问题思考】
(3)可充电的二次电池中的放电反应与充电反应是否互为可逆反应
您最近半年使用:0次
解题方法
3 . 实验探究:铜锌原电池的构造与工作原理
(1)实验装置示意图如下:盐桥中装有饱和的KCl、KNO3等溶液和琼胶制成的胶冻。
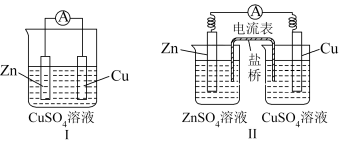
(2)【情境问题思考】
①比较铜锌原电池Ⅰ与铜锌原电池Ⅱ构成上的差异,哪一种原电池化学能转化电能的效率高___________ ?说明理由___________ ?
②铜锌原电池Ⅱ中,盐桥的作用是什么___________ ?
(1)实验装置示意图如下:盐桥中装有饱和的KCl、KNO3等溶液和琼胶制成的胶冻。

| 实验现象 | 锌片 | |
| 溶液颜色 | ||
| 取出右侧装置中的盐桥,电流表指针回到 | ||
| 能量转化 | ||
| 原因解释 | 电极名称 电极反应 | 锌电极为 |
| 铜电极为 | ||
| 电池总反应 | ||
| 电子流向 | 导线(电子导体)中,电子从 | |
| 离子移向 | 硫酸锌溶液中的 | |
| 盐桥(内有KCl)中: | ||
①比较铜锌原电池Ⅰ与铜锌原电池Ⅱ构成上的差异,哪一种原电池化学能转化电能的效率高
②铜锌原电池Ⅱ中,盐桥的作用是什么
您最近半年使用:0次



