1 . 实验室制备硝基苯的反应原理和实验装置如下:
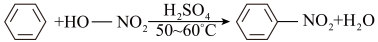 ΔH<0
ΔH<0
存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯。
有关数据列如下表
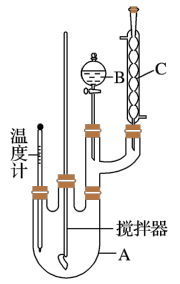
实验步骤如下:
取100mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混和酸,将混合酸小心加入B中。把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
(1)装置B的名称是_______________ 。装置C的作用是_________________________ 。
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:________________ 。
(3)为了使反应在50℃~60℃下进行,常用的方法是______________________ 。
(4)在洗涤操作中,第二次水洗的作用是__________________________ 。
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用直形冷凝管的原因是_____________________________________________ 。
(6)本实验所得到的硝基苯产率是____________________________________ 。
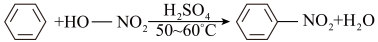 ΔH<0
ΔH<0存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯。
有关数据列如下表
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |

实验步骤如下:
取100mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混和酸,将混合酸小心加入B中。把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
(1)装置B的名称是
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:
(3)为了使反应在50℃~60℃下进行,常用的方法是
(4)在洗涤操作中,第二次水洗的作用是
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用直形冷凝管的原因是
(6)本实验所得到的硝基苯产率是
您最近一年使用:0次
解题方法
2 . 用A、B、C三种装置都可制取溴苯。请分析三套装置,并完成下列问题:
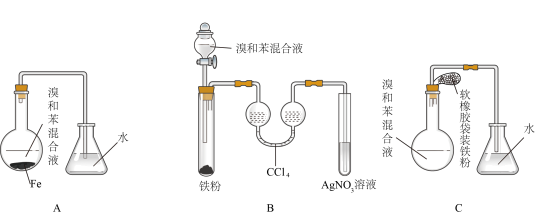
(1)写出制取溴苯的化学反应方程式:___________ ,
(2)装置A、C中的长导管作用:一是导出HBr气体,二是___________ 。
(3)C装置已连接好,并进行了气密性检验,也装入了合适的药品,接下来要使反应开始,对C应进行的操作是___________ 。
(4)a、b、c三套装置中容易造成环境污染的是___________ ,原料利用率低的是___________ 。
(5)B中采用了双球吸收管,其作用和可能出现的现象是___________ ;

(1)写出制取溴苯的化学反应方程式:
(2)装置A、C中的长导管作用:一是导出HBr气体,二是
(3)C装置已连接好,并进行了气密性检验,也装入了合适的药品,接下来要使反应开始,对C应进行的操作是
(4)a、b、c三套装置中容易造成环境污染的是
(5)B中采用了双球吸收管,其作用和可能出现的现象是
您最近一年使用:0次



