11-12高二上·广西北海·期中
1 . 氮族元素属于第_____ 族,原子核外最外层电子数为___________ ,最高价氧化物的通式为___________ ,其氢化物通式为___________ ,随核电荷数的递增,氢化物的稳定性逐渐______ 。
您最近一年使用:0次
10-11高一下·海南·期末
2 . 四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
请回答下列问题:
(1)元素Z位于周期表中第_______ 周期,_______ 族;
(2)这些元素的氢化物中,水溶液碱性最强的是_____________ (写化学式);
(3)XW2的电子式为________________________ ;
(4)Y的最高价氧化物的化学式为_________________ 。
| X | Y | |
| Z | W |
请回答下列问题:
(1)元素Z位于周期表中第
(2)这些元素的氢化物中,水溶液碱性最强的是
(3)XW2的电子式为
(4)Y的最高价氧化物的化学式为
您最近一年使用:0次
2011-07-27更新
|
956次组卷
|
5卷引用:2010—2011学年海南中学高一第二学期期末考试(2-20班)化学试卷
(已下线)2010—2011学年海南中学高一第二学期期末考试(2-20班)化学试卷(已下线)2013-2014学年海南省海南中学第二学期高一期末考试化学试卷(已下线)2015届陕西省宝鸡市岐山县高三上学期期中考试化学试卷2014-2015河南省南阳方城一中高一下学期学期第一次月考化学试卷甘肃省玉门一中2018-2019学年高一下学期期末考试化学试题
11-12高二上·江苏淮安·期末
3 . 下图是元素周期表中的一部分。

在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。请回答:
(1)硅的相对原子质量为____ ;原子序数为8的元素位于元素周期表的第__ 周期,元素符号为___ ,它属于______ (填“金属”或“非金属”)元素。
(2)原子半径:钠__ 镁(填“>”或“=”或“<”,下同),原子得电子能力:硫__ 氯。

在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。请回答:
(1)硅的相对原子质量为
(2)原子半径:钠
您最近一年使用:0次
11-12高一上·黑龙江绥化·期末
4 . (1) 同期表中位于第8纵行的铁元素属于第________ 族;
(2) 同期表中最活泼非金属元素位于第________ 纵行;
(3) 所含元素超过18种的周期是第________ 、________ 周期。
(2) 同期表中最活泼非金属元素位于第
(3) 所含元素超过18种的周期是第
您最近一年使用:0次
10-11高三上·北京·阶段练习
5 . 元素在周期表中的位置,反映了元素的原子结构和元素的性质,右图是元素周期表的一部分。
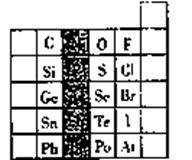
(1)阴影部分元素在元素周期表中的位置为第_________ 族。根据元素周期律、预测;酸性强弱H3AsO4______ H3PO4(用“>”或“<”表示)
(2)元素S的最高正价和最低负价的代数和为________ ,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度)。请判断:在相同条件下Se与H2反应的限度比S与H2反应限度____________ 。(选填“更大”、“更小”或“相同”)
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是__________
(4)下列说法正确的是__________
A.C、N、O、F的原子半径随着原子数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱

(1)阴影部分元素在元素周期表中的位置为第
(2)元素S的最高正价和最低负价的代数和为
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是
(4)下列说法正确的是
A.C、N、O、F的原子半径随着原子数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱
您最近一年使用:0次
10-11高二上·北京·期末
6 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。请依据元素周期表回答问题。
(1)填写下表
(2)丙的原子结构示意图是__________ ,该元素与同周期ⅦA族元素组成的化合物类型是_________ 。
(1)填写下表
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 原子序数 | 6 | 13 | ||
| 元素周期表中的位置 | 第二周期第ⅥA族 | 第三周期第IA族 |
(2)丙的原子结构示意图是
您最近一年使用:0次



