1 . (1)碳原子2p亚层上的2个电子不相同的方面是____ (选填序号)。
a.能量 b.电子云形状 c.电子云伸展方向 d.自旋状态
14N 原子与12C原子比,质子数和中子数都更多,但原子半径却更小,请解释__________________ 。
(2)铍(Be)与铝性质相似。
①以下对铍及其化合物的推断肯定不正确的是______ (选填序号)。
a.铍会在浓硫酸中钝化 b.氯化铍固体会发生升华现象
c.氧化铍坚硬难熔 d.铍的熔点低于镁
②写出BeCl2溶液和Na2BeO2溶液混合后反应的离子方程式____________________________ 。
(3)将BeCl2溶液加热蒸干后灼热,再使其熔融,用直流电电解,可得到单质铍和一种单质气体,则该气体的化学式为_______ 。
(4)氮化铝(AlN)广泛应用于集成电路,其制备原理是将氧化铝与碳粉混合均匀,在持续流动的氮气流中加热至1750℃,发生如下反应:
2Al2O3(s) 4Al(g)+3O2(g) ①
4Al(g)+3O2(g) ①
2C(s)+ O2(g) 2CO(g) ②
2CO(g) ②
2Al(g)+N2(g) 2AlN(s) ③
2AlN(s) ③
试分析反应②对制备AlN的作用______________________________________________ 。
a.能量 b.电子云形状 c.电子云伸展方向 d.自旋状态
14N 原子与12C原子比,质子数和中子数都更多,但原子半径却更小,请解释
(2)铍(Be)与铝性质相似。
①以下对铍及其化合物的推断肯定不正确的是
a.铍会在浓硫酸中钝化 b.氯化铍固体会发生升华现象
c.氧化铍坚硬难熔 d.铍的熔点低于镁
②写出BeCl2溶液和Na2BeO2溶液混合后反应的离子方程式
(3)将BeCl2溶液加热蒸干后灼热,再使其熔融,用直流电电解,可得到单质铍和一种单质气体,则该气体的化学式为
(4)氮化铝(AlN)广泛应用于集成电路,其制备原理是将氧化铝与碳粉混合均匀,在持续流动的氮气流中加热至1750℃,发生如下反应:
2Al2O3(s)
 4Al(g)+3O2(g) ①
4Al(g)+3O2(g) ① 2C(s)+ O2(g)
 2CO(g) ②
2CO(g) ②2Al(g)+N2(g)
 2AlN(s) ③
2AlN(s) ③试分析反应②对制备AlN的作用
您最近一年使用:0次
名校
2 . X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
(1)Z在元素中期表中的位置是______________________________ 。
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是__________ (填离子符号)。
(3)周期表中有些处于对角线(左上→右下)位置的元素,它们的单质及其化合物的性质相似,则M的氧化物与强碱溶液反应的离子方程式______________________________ 。
(4)Q和R按原子个数比1:1组成的化合物甲是一种“绿色”氧化剂。
①甲中所含共价键类型是____________________ 。
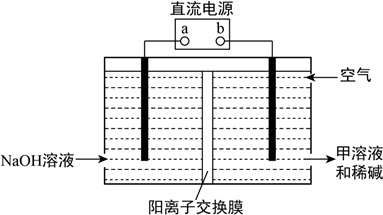
②空气阴极法电解制备甲的装置如图所示。在碱性溶液中,利用空气中的氧气还原得到甲和稀碱的溶液。图中a是__________ 极,阴极的电极反应式是____________________ 。
| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(1)Z在元素中期表中的位置是
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是
(3)周期表中有些处于对角线(左上→右下)位置的元素,它们的单质及其化合物的性质相似,则M的氧化物与强碱溶液反应的离子方程式
(4)Q和R按原子个数比1:1组成的化合物甲是一种“绿色”氧化剂。
①甲中所含共价键类型是
②空气阴极法电解制备甲的装置如图所示。在碱性溶液中,利用空气中的氧气还原得到甲和稀碱的溶液。图中a是

您最近一年使用:0次
2018-01-10更新
|
237次组卷
|
4卷引用:2016届山东省枣庄三中高三上学期12月质检化学试卷



