1 . 完成下列问题。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________
(2)①基态Cu原子有___________ 种不同能级的电子。位于在周期表___________ 区(填s、p、d或ds)。Cu+的价电子排布式为___________ 。
②N原子中最高能级的电子的电子云轮廓图为___________ 。
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是___________ 。
(3)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:___________ 。
(4)高锰酸钾是一种重要的化学试剂,实验室常常利用高锰酸钾溶液测定草酸晶体(H2C2O4·xH2O)中 的值,高锰酸钾溶液需用
的值,高锰酸钾溶液需用___________ 盛装(填 酸式滴定管 或 碱式滴定管)滴定终点溶液的判断是___________ 颜色变化为由无色变为浅红色。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
(2)①基态Cu原子有
②N原子中最高能级的电子的电子云轮廓图为
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
(3)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:
(4)高锰酸钾是一种重要的化学试剂,实验室常常利用高锰酸钾溶液测定草酸晶体(H2C2O4·xH2O)中
 的值,高锰酸钾溶液需用
的值,高锰酸钾溶液需用
您最近一年使用:0次
名校
2 . Be与 类似,
类似, 也能与
也能与 溶液反应并转化为结构与四羟基合铝酸钠类似的盐,试写出
溶液反应并转化为结构与四羟基合铝酸钠类似的盐,试写出 和
和 反应的离子方程式
反应的离子方程式___________ 。
 类似,
类似, 也能与
也能与 溶液反应并转化为结构与四羟基合铝酸钠类似的盐,试写出
溶液反应并转化为结构与四羟基合铝酸钠类似的盐,试写出 和
和 反应的离子方程式
反应的离子方程式
您最近一年使用:0次
名校
解题方法
3 . 元素周期律反映了元素性质的周期性变化规律。
(1)氮氧化铝(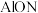 )是一种高硬度,耐高温的防弹材料,
)是一种高硬度,耐高温的防弹材料, 、O、N三种元素的简单离子半径由大到小的排列顺序是
、O、N三种元素的简单离子半径由大到小的排列顺序是___________ 。
(2)在元素周期表中, ,
, 具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:
具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:___________ 。
(3)锡为主族元素,其原子结构示意图: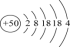 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是___________ , 能与
能与 溶液反应生成钠盐,写出发生反应的化学方程式:
溶液反应生成钠盐,写出发生反应的化学方程式:___________ 。
(4)硒 是与人类的健康密切相关的一种元素,工业上用浓
是与人类的健康密切相关的一种元素,工业上用浓 ,焙烧
,焙烧 的方法提取硒(其中
的方法提取硒(其中 转化为
转化为 ),且有
),且有 和
和 (固体)生成,写出发生反应的化学方程式:
(固体)生成,写出发生反应的化学方程式:___________ 。理论上该反应每转移 电子,可得到的
电子,可得到的 的质量为
的质量为___________ g。
(1)氮氧化铝(
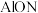 )是一种高硬度,耐高温的防弹材料,
)是一种高硬度,耐高温的防弹材料, 、O、N三种元素的简单离子半径由大到小的排列顺序是
、O、N三种元素的简单离子半径由大到小的排列顺序是(2)在元素周期表中,
 ,
, 具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:
具有相似的化学性质。写出铍与氢氧化钠溶液反应的离子方程式:(3)锡为主族元素,其原子结构示意图:
 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是 能与
能与 溶液反应生成钠盐,写出发生反应的化学方程式:
溶液反应生成钠盐,写出发生反应的化学方程式:(4)硒
 是与人类的健康密切相关的一种元素,工业上用浓
是与人类的健康密切相关的一种元素,工业上用浓 ,焙烧
,焙烧 的方法提取硒(其中
的方法提取硒(其中 转化为
转化为 ),且有
),且有 和
和 (固体)生成,写出发生反应的化学方程式:
(固体)生成,写出发生反应的化学方程式: 电子,可得到的
电子,可得到的 的质量为
的质量为
您最近一年使用:0次
4 . 磷酸亚铁锂(LiFePO4)和锰酸锂(LiMn2O4)均可用作锂电池的正极材料。回答下列问题:
(1)在周期表中,与Li化学性质最相似的邻族元素是___________ (填元素符号)。基态O原子的价电子排布图为___________ 。基态P原子电子占据最高能级的电子云在空间有___________ 个伸展方向。
(2)写出H2O2的电子式___________ 。
(3)原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为___________ 。
(4)第三周期元素中,第一电离能介于A1和P之间的元素有___________ 种。
(5)Fe元素位于周期表的___________ 区。已知:I3(Mn)=3248kJ/mol,I3(Fe)=2957kJ/mol。第三电离能I3(Mn)>I3(Fe),其主要原因是___________ 。
(1)在周期表中,与Li化学性质最相似的邻族元素是
(2)写出H2O2的电子式
(3)原子核外电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为(4)第三周期元素中,第一电离能介于A1和P之间的元素有
(5)Fe元素位于周期表的
您最近一年使用:0次
名校
5 . 下列8种化学符号: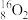 、
、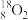 、
、 、
、 、
、 、
、 、
、 、
、 。
。
(1)表示核素的符号共___________ 种。
(2)互为同位素的是___________ 。
(3)质量相同的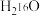 和
和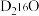 所含中子数之比为
所含中子数之比为___________ 。
根据周期表对角线规则,金属Be与A1单质及其化合物性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应的离子方程式:___________ 。
(5) 与
与 可用
可用___________ 鉴别。
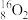 、
、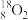 、
、 、
、 、
、 、
、 、
、 、
、 。
。(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的
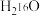 和
和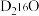 所含中子数之比为
所含中子数之比为根据周期表对角线规则,金属Be与A1单质及其化合物性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应的离子方程式:
(5)
 与
与 可用
可用
您最近一年使用:0次
23-24高二·全国·假期作业
解题方法
6 . 仔细观察如图,回答下列问题:

(1)B的原子结构示意图为___________ ,B元素位于元素周期表的第___________ 周期第___________ 族。
(2)铍的最高价氧化物对应的水化物是___________ 化合物(填“酸性”“碱性”或“两性”),证明这一结论的有关离子方程式是 Be(OH)2+2OH-=BeO +2H2O,Be(OH)2+2H+=Be2++2H2O。
+2H2O,Be(OH)2+2H+=Be2++2H2O。
(3)根据周期律知识,硼酸酸性比碳酸___________ ,理由是___________ 。
(4)根据Mg在空气中的燃烧情况,Li在空气中燃烧生成的产物为___________ (用化学式表示)。

(1)B的原子结构示意图为
(2)铍的最高价氧化物对应的水化物是
 +2H2O,Be(OH)2+2H+=Be2++2H2O。
+2H2O,Be(OH)2+2H+=Be2++2H2O。(3)根据周期律知识,硼酸酸性比碳酸
(4)根据Mg在空气中的燃烧情况,Li在空气中燃烧生成的产物为
您最近一年使用:0次
7 . 钇及其化合物在航天、电子、超导等方面有着广泛的应用,工业上以硅铍钇矿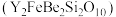 为原料生产氧化钇(
为原料生产氧化钇( )。
)。
(1)钇(Y)与钪同族,位于元素周期表中钪(Sc)的下一周期,基态钇(Y)原子的价电子排布图为______ ,与 元素同周期的基态原子中,未成对电子数与
元素同周期的基态原子中,未成对电子数与 原子相同的元素还有种
原子相同的元素还有种________ 。
(2)在元素周期表中, 和
和 处于第二周期和第三周期的对角线位置,化学性质相似。
处于第二周期和第三周期的对角线位置,化学性质相似。
①写出 的最高价氧化物对应水化物与烧碱溶液反应的离子方程式:
的最高价氧化物对应水化物与烧碱溶液反应的离子方程式:___________ 。
②已知 元素和
元素和 元素的电负性分别为1.5和4.0,则它们形成的化合物是
元素的电负性分别为1.5和4.0,则它们形成的化合物是_______ (填“离子化合物”或“共价化合物”)。
(3) 与
与 均为第二周期元素:
均为第二周期元素:
① 元素的原子核外共有
元素的原子核外共有____ 种不同空间运动状态的电子。
②电离能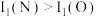 ,原因是
,原因是__________ 。
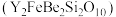 为原料生产氧化钇(
为原料生产氧化钇( )。
)。(1)钇(Y)与钪同族,位于元素周期表中钪(Sc)的下一周期,基态钇(Y)原子的价电子排布图为
 元素同周期的基态原子中,未成对电子数与
元素同周期的基态原子中,未成对电子数与 原子相同的元素还有种
原子相同的元素还有种(2)在元素周期表中,
 和
和 处于第二周期和第三周期的对角线位置,化学性质相似。
处于第二周期和第三周期的对角线位置,化学性质相似。①写出
 的最高价氧化物对应水化物与烧碱溶液反应的离子方程式:
的最高价氧化物对应水化物与烧碱溶液反应的离子方程式:②已知
 元素和
元素和 元素的电负性分别为1.5和4.0,则它们形成的化合物是
元素的电负性分别为1.5和4.0,则它们形成的化合物是(3)
 与
与 均为第二周期元素:
均为第二周期元素:①
 元素的原子核外共有
元素的原子核外共有②电离能
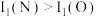 ,原因是
,原因是
您最近一年使用:0次
2024-01-06更新
|
363次组卷
|
2卷引用:吉林省辽源市田家炳高中友好学校七十六届期末联考2023-2024学年高二上学期1月期末化学试题
名校
8 . 元素周期表是学习化学的工具,也为化学的进一步探索与研究提供了理论指导,化学学习者和研究者一直关注周期表的运用与发展。试回答下列问题:
(1)“大爆炸理论”指出:200亿年以前,宇宙中所有物质都包含在一个密度无限大,温度无限高的原始核中,由于某种原因它发生了爆炸,首先产生了中子、质子和电子,随后就产生了元素。你由此可知最先产生的元素是_____ (填写元素符号)。
(2)2006年11月16日美国和俄罗斯科学家联合宣布,他们合成出了118号元素,新原子的质量数为297,则该新原子中子数与质子数之差为_____ 。
(3)人们研究发现第一周期与第二周期一些元素的性质与同族元素性质共性很少,有人建议将氢放在VIIA,写出一种能支持该观点的化合物:______ 。
(4)研究周期表发现存在对角线规则,处于对角线上的元素性质相似,如硼与硅处于对角线,请写出硼和氢氧化钠溶液反应的离子方程式:______ 。
(1)“大爆炸理论”指出:200亿年以前,宇宙中所有物质都包含在一个密度无限大,温度无限高的原始核中,由于某种原因它发生了爆炸,首先产生了中子、质子和电子,随后就产生了元素。你由此可知最先产生的元素是
(2)2006年11月16日美国和俄罗斯科学家联合宣布,他们合成出了118号元素,新原子的质量数为297,则该新原子中子数与质子数之差为
(3)人们研究发现第一周期与第二周期一些元素的性质与同族元素性质共性很少,有人建议将氢放在VIIA,写出一种能支持该观点的化合物:
(4)研究周期表发现存在对角线规则,处于对角线上的元素性质相似,如硼与硅处于对角线,请写出硼和氢氧化钠溶液反应的离子方程式:
您最近一年使用:0次
9 . 指出下列反应的氧化剂和还原剂
(1)2H2+O2=2H2O:氧化剂_______ ;还原剂_______ 。
(2)4P+5O2=2P2O5:氧化剂_______ ;还原剂_______ 。
(3)Fe+H2SO4=FeSO4+H2 :氧化剂
:氧化剂_______ ;还原剂_______ 。
(4)WO3+3H2=W+3H2O:氧化剂_______ ;还原剂_______ 。
(5)已知 与
与 属于两性氢氧化物,写出
属于两性氢氧化物,写出 分别溶于
分别溶于 溶液、盐酸的化学方程式:
溶液、盐酸的化学方程式:_______ 、_______ 。
(1)2H2+O2=2H2O:氧化剂
(2)4P+5O2=2P2O5:氧化剂
(3)Fe+H2SO4=FeSO4+H2
 :氧化剂
:氧化剂(4)WO3+3H2=W+3H2O:氧化剂
(5)已知
 与
与 属于两性氢氧化物,写出
属于两性氢氧化物,写出 分别溶于
分别溶于 溶液、盐酸的化学方程式:
溶液、盐酸的化学方程式:
您最近一年使用:0次
解题方法
10 . 随着能源技术的发展,科学家们将目光聚焦于锂的开发与研究。
(1)基态Be原子中电子占据最高能级的符号是_______ ,占据该能级电子的电子云轮廓图的形状为_______ 形。
(2)在周期表中,与Li元素的化学性质最相似的邻族元素是_______
(3)部分元素的第一电离能(I)如表所示。
①碱金属的第一电离能与碱金属的活泼性的联系是_______
②Be的第一电离能比Li的大,从原子结构角度分析其原因是_______
(4)海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如下图所示:

①金属锂在电极_______ (填“A”或“B”)上生成。
②阳极产生两种气体单质,写出阳极的电极反应:_______ 、_______ 。
(1)基态Be原子中电子占据最高能级的符号是
(2)在周期表中,与Li元素的化学性质最相似的邻族元素是
(3)部分元素的第一电离能(I)如表所示。
| 元素 | li | Be | Na | K |
| 11(kJ∙mol-1) | 520 | 900 | 496 | 419 |
②Be的第一电离能比Li的大,从原子结构角度分析其原因是
(4)海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如下图所示:

①金属锂在电极
②阳极产生两种气体单质,写出阳极的电极反应:
您最近一年使用:0次



