名校
1 . 亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:0.5 ℃,有毒)常温下是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成,并以液态储存 。
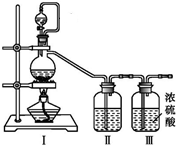
(1)甲组的同学拟制备原料气NO和Cl2,均采用上图制备装置:
①写出NOCl的N元素化合价:_______
②为制备纯净干燥的气体,下表中缺少的药品是(填写在横线上):
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
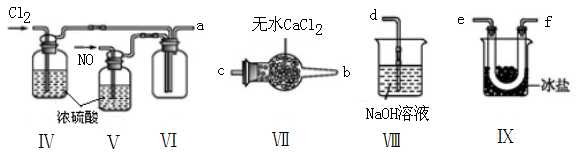
①装置连接顺序为a→____________________________ (按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是______________________________ 。
③装置Ⅵ在实验结束,拆解装置前,应作怎样的处理?_________________________ 。
④装置Ⅷ中吸收尾气时,NOCl发生的非氧化还原反应的化学方程式为___________________ 。

(1)甲组的同学拟制备原料气NO和Cl2,均采用上图制备装置:
①写出NOCl的N元素化合价:
②为制备纯净干燥的气体,下表中缺少的药品是(填写在横线上):
| 实验项目 | 装置Ⅰ | 装置Ⅱ | |
| 制备的气体 | 烧瓶中 | 分液漏斗中 | |
| a .制备纯净干燥的Cl2 | MnO2 | ||
| b .制备纯净干燥的NO | Cu | ||

①装置连接顺序为a→
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是
③装置Ⅵ在实验结束,拆解装置前,应作怎样的处理?
④装置Ⅷ中吸收尾气时,NOCl发生的非氧化还原反应的化学方程式为
您最近一年使用:0次
2018-12-19更新
|
615次组卷
|
3卷引用:福建省厦门市启悟中学2019届高三上学期期中考试化学试题



