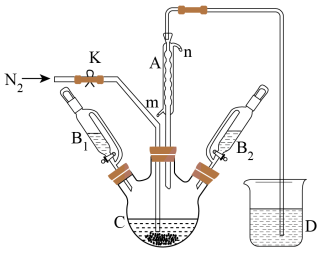
1 . 二茂铁可用作燃料的节能消烟剂、抗爆剂等。某兴趣小组拟用如图所示装置制备二茂铁(电磁搅拌装置、夹持装置略去),反应原理:2KOH+FeCl2+2C5H6(环戊二烯)=Fe(C5H5)2(二茂铁)+2KCl+2H2O。
制备二茂铁的实验步骤如下:
I.在C中加入25gKOH粉末,并加入60mL无冰乙醚,连接好仪器,充分搅拌,然后打开K,通入N2,排尽装置中的空气后,关闭K。
Ⅱ.打开B1的活塞,滴加5.5mL新蒸馏的环戊二烯,搅拌。
Ⅲ.将含一定质量的FeCl2的二甲亚砜溶液25mL由B2缓慢滴入C中,在45min时滴完,再继续搅拌45min,反应完毕。
Ⅳ.拆下仪器C,再向其中加入25mL无水乙醚,搅拌,将液体转移到分液漏斗中,依次用盐酸、水洗涤2~3次,分液得橙黄色溶液。
V.蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
步骤I中检验装置中的空气已排尽的方法是_______ 。
| 物质 | 熔点/°C | 沸点/°C | 密度/(g·cm-3) | 溶解性 |
| 二茂铁 | 173 | 249(100°C时开始升华) | 1.49 | 不溶于水和盐酸,溶于乙醚 |
| 环戊二烯 | -97.2 | 42.5 | 0.87 | 不溶于水,溶于乙醚和乙醇 |
| 乙醚 | -116 | 34.5 | 0.71 | 微溶于水,溶于乙醇 |
| 二甲亚砜 | 18.4 | 189 | 1.10 | 与水互溶,不溶于乙醚 |
I.在C中加入25gKOH粉末,并加入60mL无冰乙醚,连接好仪器,充分搅拌,然后打开K,通入N2,排尽装置中的空气后,关闭K。
Ⅱ.打开B1的活塞,滴加5.5mL新蒸馏的环戊二烯,搅拌。
Ⅲ.将含一定质量的FeCl2的二甲亚砜溶液25mL由B2缓慢滴入C中,在45min时滴完,再继续搅拌45min,反应完毕。
Ⅳ.拆下仪器C,再向其中加入25mL无水乙醚,搅拌,将液体转移到分液漏斗中,依次用盐酸、水洗涤2~3次,分液得橙黄色溶液。
V.蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
步骤I中检验装置中的空气已排尽的方法是
您最近半年使用:0次
名校
解题方法
2 . 盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室必备的重要试剂
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有___________ 性;硝酸应保存在棕色瓶中,这是因为硝酸具有___________ 性。
(2)如图是硫酸试剂瓶标签上的部分内容,该硫酸的浓度是___________ ;实验人员操作时不必需穿戴的安全用具是___________ 。
A.防护手套 B.实验服 C.防毒面具 D.护目镜
(3)在稀硝酸溶液中加入铜片使之充分反应,写出反应的离子方程式_________________ 。
(4)实验室中向烧杯内加入约20g蔗糖,向其中插入玻璃棒,滴加几滴蒸馏水,再加入适量浓硫酸。白色的蔗糖变为疏松多孔的黑色物质,放出大量的热使烧杯壁发烫。验证产生的气体有SO2的方法是___________________ ,验证该气体中还含有CO2的方法是_______________________ 。
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有
(2)如图是硫酸试剂瓶标签上的部分内容,该硫酸的浓度是
| 化学纯(CP)(500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g/cm3 质量分数: 98.9% |
(3)在稀硝酸溶液中加入铜片使之充分反应,写出反应的离子方程式
(4)实验室中向烧杯内加入约20g蔗糖,向其中插入玻璃棒,滴加几滴蒸馏水,再加入适量浓硫酸。白色的蔗糖变为疏松多孔的黑色物质,放出大量的热使烧杯壁发烫。验证产生的气体有SO2的方法是
您最近半年使用:0次
2023-04-23更新
|
72次组卷
|
2卷引用:广东省惠州市惠阳区部分学校2022-2023学年高一下学期期中联考化学试题
解题方法
3 . 氯元素能与许多元素形成种类繁多的化合物,这些含氯化合物在生活及工农业生产中发挥着重要的作用。
(1)从海水中获取粗盐的方法是_______ 。
(2)利用电解饱和食盐水可以制备氢气、氯气、氢氧化钠。电解时阳极产物为_______ ,该产物的检验方法为_______ 。
(3)工业上用氯气和消石灰反应制备漂白粉,其有效成分是_______ (填化学式);写出漂白粉露置在空气中失效过程中所涉及的化学方程式:_______ 、_______ 。
(4)H2与Cl2在点燃条件下可以制取HCl。某同学对HCl性质进行如下预测:
①从物质类别上看,HCl属于酸,其水溶液能与碳酸钙反应,相应的离子方程式为_______ 。
②从化合价角度看,HCl中的Cl元素显-1价,处于氯元素的最低价,因此-1价的Cl元素在反应中可以被_______ (选填“氧化”或“还原”),在一定条件下能与_______ 发生氧化还原反应(填编号)。
a.KI b.NaOH c.KMnO4
(5)已知HClO4是强酸,HClO4在水中的电离方程式为_______ 。
(1)从海水中获取粗盐的方法是
(2)利用电解饱和食盐水可以制备氢气、氯气、氢氧化钠。电解时阳极产物为
(3)工业上用氯气和消石灰反应制备漂白粉,其有效成分是
(4)H2与Cl2在点燃条件下可以制取HCl。某同学对HCl性质进行如下预测:
①从物质类别上看,HCl属于酸,其水溶液能与碳酸钙反应,相应的离子方程式为
②从化合价角度看,HCl中的Cl元素显-1价,处于氯元素的最低价,因此-1价的Cl元素在反应中可以被
a.KI b.NaOH c.KMnO4
(5)已知HClO4是强酸,HClO4在水中的电离方程式为
您最近半年使用:0次
解题方法
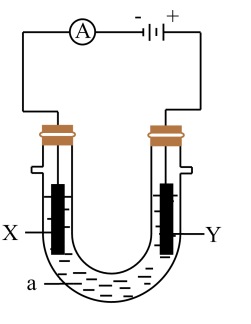
4 . 电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:Y电极上的电极反应式为_______ ,检验该电极反应产物的方法是_______ 。
(2)如要用电解方法精炼粗铜,则:X电极的材料是_______ ,电极反应式是_______ 。电解液a可以选用_______ 。

请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:Y电极上的电极反应式为
(2)如要用电解方法精炼粗铜,则:X电极的材料是
您最近半年使用:0次
名校
解题方法
5 . 浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的部分产物,某同学设计了如下图所示的实验。请据此回答下列问题:
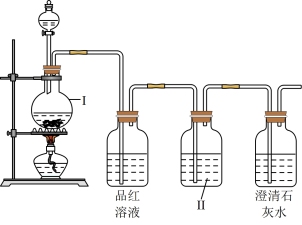
(1)设备I的仪器名称是_______ 。
(2)设备II中盛放的试剂是_______ ,该试剂的作用是_______ 。
(3)浓硫酸与木炭反应的化学方程式是_______ 。
(4)证明产物中含有CO2的实验现象是_______ 。

(1)设备I的仪器名称是
(2)设备II中盛放的试剂是
(3)浓硫酸与木炭反应的化学方程式是
(4)证明产物中含有CO2的实验现象是
您最近半年使用:0次
2022-06-24更新
|
328次组卷
|
2卷引用:浙江省嘉兴市2021-2022学年高一下学期期末检测化学试题
解题方法
6 . 小明买了一种“汽泡爽”的冲调饮料,饮料说明如下:
【主要原料】柠檬酸(C6H8O7)和小苏打(NaHCO3);
【使用说明】将一包“汽泡爽”粉末倒入玻璃杯中,加入200mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料。小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响。
(1)“汽泡爽”中的小苏打(NaHCO3)是我们生活中常见的一种酸式盐,请按照下列要求写出相关方程式:
①小苏打受热易分解:___________ 。
②小苏打和盐酸的反应:___________ 。
③小苏打和氢氧化钠溶液的反应:___________ 。
【实验】探究“汽泡爽”产生气体的成分。
(2)小明阅读资料发现:“汽泡爽”原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,填写生成气体的化学式:3NaHCO3+C6H8O7=C6H5O7Na3+3H2O+3___________ ↑
(3)为了检验该气体,小明选择的试剂是___________ 。
【主要原料】柠檬酸(C6H8O7)和小苏打(NaHCO3);
【使用说明】将一包“汽泡爽”粉末倒入玻璃杯中,加入200mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料。小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响。
(1)“汽泡爽”中的小苏打(NaHCO3)是我们生活中常见的一种酸式盐,请按照下列要求写出相关方程式:
①小苏打受热易分解:
②小苏打和盐酸的反应:
③小苏打和氢氧化钠溶液的反应:
【实验】探究“汽泡爽”产生气体的成分。
(2)小明阅读资料发现:“汽泡爽”原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,填写生成气体的化学式:3NaHCO3+C6H8O7=C6H5O7Na3+3H2O+3
(3)为了检验该气体,小明选择的试剂是
您最近半年使用:0次
7 . 草酸亚铁晶体(FeC2O4·2H2O,相对分子质量为180)呈淡黄色,可用作照相显影剂。纯净草酸亚铁晶体热分解产物的探究。气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:
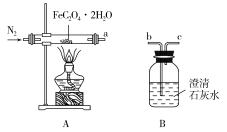

按照气流从左到右的方向,上述装置的连接顺序为___________ →尾气处理装置(填仪器接口的字母编号)。


按照气流从左到右的方向,上述装置的连接顺序为
您最近半年使用:0次
名校
解题方法
8 . 现有下列5种物质,根据要求将对应物质的序号字母 填入相应空格内。
A. B.
B. C.
C. D.
D. E.
E.
(1)属于单质的是_______ ,属于氧化物的是_______ ,属于盐的是_______ 。
(2)能与氢氧化钠( )发生中和反应的是
)发生中和反应的是_______ 。
(3)实验室常用_______ 的水溶液检验 气体。
气体。
A.
 B.
B. C.
C. D.
D. E.
E.
(1)属于单质的是
(2)能与氢氧化钠(
 )发生中和反应的是
)发生中和反应的是(3)实验室常用
 气体。
气体。
您最近半年使用:0次
2020-12-20更新
|
323次组卷
|
3卷引用:2019年12月吉林省普通高中学业考试化学试题
9 . 实验室所用少量氯气是用下列方法制取的:4HCl(浓)+MnO2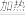 Cl2↑+MnCl2+2H2O,试回答下列问题:
Cl2↑+MnCl2+2H2O,试回答下列问题:
(1)该反应中氧化剂与还原剂的物质的量比为:__ 。
(2)写出该反应的离子方程式:___ 。
(3)当有0.2mol电子转移时,生成标准状况下Cl2的体积是___ L。
(4)若用足量二氧化锰与50ml36.5%1.2g/ml浓盐酸反应,制得的Cl2在标准状况下总小于3.36L,原因可能是①__ ,②__ 。
(5)检验氯气是否收集满的方法是用___ 试纸靠近集气瓶口,若试纸变蓝证明氯气已收集满。
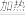 Cl2↑+MnCl2+2H2O,试回答下列问题:
Cl2↑+MnCl2+2H2O,试回答下列问题:(1)该反应中氧化剂与还原剂的物质的量比为:
(2)写出该反应的离子方程式:
(3)当有0.2mol电子转移时,生成标准状况下Cl2的体积是
(4)若用足量二氧化锰与50ml36.5%1.2g/ml浓盐酸反应,制得的Cl2在标准状况下总小于3.36L,原因可能是①
(5)检验氯气是否收集满的方法是用
您最近半年使用:0次
名校
解题方法
10 . 某探究小组采用下图所示装置进行Fe粉与水蒸气的反应。

(1)实验前检查装置气密性的方法为______________ 。
(2)检验实验中生成气体的实验操作是_____________ 。
(3)写出试管中发生的化学反应方程式________________

(1)实验前检查装置气密性的方法为
(2)检验实验中生成气体的实验操作是
(3)写出试管中发生的化学反应方程式
您最近半年使用:0次



