1 . 海水中化学资源的开发利用
(1)海水中溶解和悬浮着大量的____ 和____ 。海水中含量最多的____ 两种元素,加上Cl、Na、Mg、S、Ca、K、Br、C、Sr、B、F元素,其总含量超过99%,其他元素为____ 。虽然海水中元素的种类很多,总储量____ ,但许多元素的富集程度却____ 。
(2)海水制盐从海水中制得的氯化钠,可以食用,同时也是生产烧碱、纯碱、钠、氯气、盐酸等的化工原料。
①氯碱工业:电解饱和食盐水,可生产氢氧化钠、氢气和氯气。
化学反应方程式:______ 。
②制钠和氯气:______ 。
③制盐酸:________ 。
④制漂白剂(84消毒液):_______ 。
⑤制纯碱:__________ ;_________ 。
(3)海水提溴
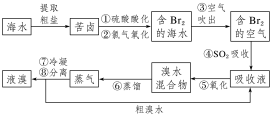
①海水提溴的方法(吹出法)
②氧化、吸收环节主要离子方程式:2Br-+Cl2=Br2+2Cl-、SO2+Br2+2H2O=4H++SO +2Br-。
+2Br-。
(1)海水中溶解和悬浮着大量的
(2)海水制盐从海水中制得的氯化钠,可以食用,同时也是生产烧碱、纯碱、钠、氯气、盐酸等的化工原料。
①氯碱工业:电解饱和食盐水,可生产氢氧化钠、氢气和氯气。
化学反应方程式:
②制钠和氯气:
③制盐酸:
④制漂白剂(84消毒液):
⑤制纯碱:
(3)海水提溴
①海水提溴的方法(吹出法)
| 工艺流程 |
| |
基本操作 | 浓缩 | 海水晒盐和海水淡化的过程中副产物Br-得到浓缩 |
氧化 | 向浓缩的海水中通入Cl2,将Br-氧化成Br2 | |
吹出 | 利用溴的挥发性,通入热空气和水蒸气,吹出溴蒸气 | |
吸收 | 吹出的溴蒸气用SO2吸收 | |
蒸馏 | 再用Cl2将HBr氧化得到产品溴后蒸馏分离 | |
②氧化、吸收环节主要离子方程式:2Br-+Cl2=Br2+2Cl-、SO2+Br2+2H2O=4H++SO
 +2Br-。
+2Br-。
您最近一年使用:0次