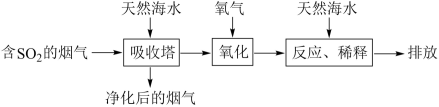
1 . 天然海水中主要含有Na+、K+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子。火力发电时燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示:下列说法错误的是( )

| A.天然海水pH≈8的原因是由于海水中的CO32-、HCO3-水解 |
| B.“氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42- |
| C.“反应、稀释”时加天然海水的目的是中和、稀释经氧化后海水中生成的酸 |
| D.“排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同 |
您最近一年使用:0次
2020-02-28更新
|
1215次组卷
|
3卷引用:辽宁省锦州市联合校2020届高三上学期期末考试化学试题
辽宁省锦州市联合校2020届高三上学期期末考试化学试题(已下线)考点17 化工生产诸要素及流程图分析-2020年高考化学命题预测与模拟试题分类精编湖南省永州市2020届高三“培优”理综化学模拟试卷(三)
名校
解题方法
2 . 海水中不仅含有丰富的非金属元素资源(如Cl、Br、I等),还含有丰富的金属元素资源(如Na、Mg、Fe、Cr等)。
(1)海水晒盐的原理是________ ;写出氯化钠的电子式:________________ ;与Na、Cl同周期,且简单离子半径最小的离子结构示意图:______________ ;
(2)晒出的粗盐常混有MgSO4、CaSO4等杂质,为了得到精制盐,则提纯过程操作步骤和加入试剂的顺序是:①溶解,②________ ,③加过量Na2CO3溶液,④________ ,⑤过滤除去杂质,⑥________ ,⑦蒸发结晶;
(3)晒盐得到的母液(盐卤)中含有丰富的镁元素,但其中常混有Fe2+、Cr3+等,为富集镁使其转化为MgCl2晶体。
有关资料:
为了有效除去杂质离子,又不引入新的杂质离子,且能满足“绿色化学理念”,则最佳试剂选择和操作是:
①先加________ ;目的是_______________________________ ;
②再加________ ;目的是_______________________________ 。
(1)海水晒盐的原理是
(2)晒出的粗盐常混有MgSO4、CaSO4等杂质,为了得到精制盐,则提纯过程操作步骤和加入试剂的顺序是:①溶解,②
(3)晒盐得到的母液(盐卤)中含有丰富的镁元素,但其中常混有Fe2+、Cr3+等,为富集镁使其转化为MgCl2晶体。
有关资料:
| M(OH)n | pH | |
| 沉淀完全 | 开始沉淀 | |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Mg(OH)2 | 9.5 | 11.0 |
| Cr(OH)3 | 4.3 | 5.0 |
为了有效除去杂质离子,又不引入新的杂质离子,且能满足“绿色化学理念”,则最佳试剂选择和操作是:
①先加
②再加
您最近一年使用:0次



