28. 过氧化镁(MgO
2)是一种重要的化工原料,可用来处理被地下水污染的土壤,还可以用于配制牙膏,对牙齿有漂白和防过敏的作用。
(一)过氧化镁的性质
(1)过氧化镁是一种白色粉末。化学性质不够稳定,加热时会分解生成氧气和氧化镁;也不溶于水,但在水中会逐渐分解放出氧气。
(2)过氧化镁易溶于稀盐酸,发生反应:MgO
2+2HCl==MgCl
2+H
2O
2,同时放出大量的热。
(二)过氧化镁的制备
(1)煅烧:煅烧Mg
2(OH)
2CO
3得到三种氧化物,其中一种常温下是气体,且能使澄清石灰水变浑浊,煅烧时反应的化学方程式为
_____ 。检测煅烧过程碱式碳酸镁完全分解的方法是
_____ (写出具体的操作和现象)。
(2)转化:向所得固体中加双氧水充分搅拌,发生反应MgO+H
2O
2=MgO
2+H
2O
(3)分离:得到产品。
(4)测定:在生产过程中,过氧化镁中常常含有少量的氧化镁杂质(其他杂质不考虑)。
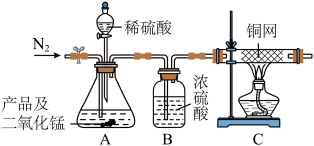
以下是某小组进行过氧化镁样品纯度检测的实验装置和实验步骤。
已知:a.MnO
2与稀盐酸不反应
b.MgO+C

Mg+CO↑
实验前称取产品及二氧化锰共12g,先缓慢通入N
2一段时间,加热铜网至红热后,再缓慢滴入过量稀盐酸,直至A中样品完全反应,继续缓慢通N
2一段时间后停止加热。对锥形瓶中的剩余物过滤,洗涤,干燥,得到滤渣2g。
①样品完全反应后继续缓慢通N
2的目的是
_____ ;
②装置B的作用
_____ (填字母代号)
a.除去气体中水蒸气 b.便于观察和控制气流速度
③实验测得C装置中铜网增重1.6g,该产品中过氧化镁的含量为
_____ %(计算结果精确:到0.1%)
④经讨论,该小组又设计了下列3种方案,分别取5.0g产品进行实验,能确定MgO
2质量分数的是
_____ (填序号)。
a.加热,使MgO
2完全分解,测出剩余固体的质量
b.与足量炭粉在高温下充分反应,测出生成Mg的质量
c.先加足量稀盐酸,再加足量NaOH溶液,充分反应,测出Mg(OH)
2质量