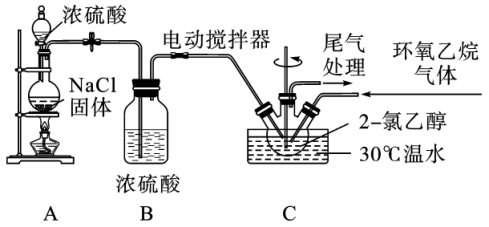
17. 2-氯乙醇是一种重要的有机化工原料,溶于水,受热时易分解。通常是以适量的2-氯乙醇为溶剂,用氯化氢与环氧乙烷反应制得新的2-氯乙醇。制取反应装置如图所示。
反应原理为:

(g)+HCl(g)
⇌ClCH
2CH
2OH(l)
△H<0
部分实验药品及物理量:
| 化合物名称 | 相对分子质量 | 熔点(℃) | 沸点(℃) |
| 环氧乙烷 | 44 | -112.2 | 10.8 |
| 2-氯乙醇 | 80.5 | -67.5 | 128.8 |
制取与测定实验步骤如下:
I.2-氯乙醇的制取
①将溶剂2-氯乙醇加入
______(填仪器名称)中,启动搅拌器;
②分别将氯化氢与环氧乙烷两种气体按6:5物质的量的配比通入反应器中,使其在溶剂中充分溶解反应;
③反应温度控制在30℃,持续反应100 min;
④采用减压蒸馏、收集产品。
(1)实验装置A、B中均用到了浓硫酸,分别体现的浓硫酸的性质为
______,
______。
(2)步骤③控制反应温度在30℃,如果温度高于30℃可能的后果有
______。
(3)在步骤④中,采用减压蒸馏的原因是
______。
II.2-氯乙醇样品中Cl元素的测定
①取样品1.00 mL于锥形瓶中,加入NaOH溶液,加热;待反应完全后加稀硝酸至酸性;
②加入32.50 mL 0.4000 mol·L
-1 AgNO
3溶液,使Cl
-完全沉淀;
③加入指示剂,用0.1000 mol·L
-1 NH
4SCN溶液滴定过量的Ag
+至终点,消耗NH
4SCN溶液10.00 mL;
④另取样品1.00 mL加水稀释至10.00 mL,用pH计测定,测得溶液pH为1.00。
已知:
a.K
sp(AgCl)=1.8×10
-10、K
sp(AgSCN)=1.0×10
-12b.2-氯乙醇样品中还含有一定量的氯化氢和其他杂质(杂质不与NaOH和AgNO
3溶液反应),密度约为1.10 g·mL
-1。
(1)ClCH
2CH
2OH与NaOH反应生成NaCl和另一种物质,该物质的分子式为
______。
(2)步骤④中选用的指示剂可以是下列的
______。(选填序号)
A.淀粉溶液
B.酚酞溶液 C.NH
4Fe(SO
4)
2溶液
D.NaCl溶液
(3)根据实验测定的数据计算,样品中2-氯乙醇的质量分数为
______。
(4)ClCH
2CH
2OH与乙酸发生酯化反应的方程式
______。