14. 初三学生在学习浓硫酸性质时,老师提到浓硫酸与金属铜在加热条件下能产生气体,引起了同学们的兴趣,设计了实验进行探究:
【提出问题】铜与浓硫酸反应生成物是什么?其中气体是什么?
【猜想假设】同学们对产生的气体提出了猜想。
猜想一:氢气
猜想二:二氧化硫
猜想三:氢气和二氧化硫的混合物
【查阅资料】
(1)二氧化硫可以使品红溶液褪色,也能和碱溶液反应;
(2)H
2 + CuO

Cu + H
2O
【实验探究】师生设计了如下装置进行实验(部分仪器省略),请完成填空:
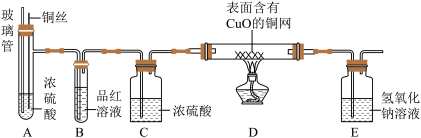
第一步:加热装置A一段时间,装置B中品红溶液褪色,证明有
______气体产生;
第二步:点燃装置D处酒精灯,发现D玻璃管中
______,则猜想二正确;
第三步:停止加热,将铜丝上提,向装置A中玻璃管鼓入空气;
第四步:冷却,将A中液体用水稀释,A中液体为
_______色,则有硫酸铜生成。
【表达交流】请完成铜与浓硫酸反应的化学方程式: Cu + 2H
2SO
4(浓)

CuSO
4 + SO
2 ↑ + 2
______。
【反思拓展】
(1)装置C的作用:
________;装置E的作用:①
________、 ②阻止空气进入D装置;
(2)用碳代替铜与浓硫酸共热也会发生反应,产生两种既不能燃烧,也不支持燃烧的气体,其中一种气体是SO
2,你认为另一种气体为
_______(写化学式)。