河南省新野县第一高级中学2018届高三上学期第一次月考化学试题
河南
高三
阶段练习
2017-09-27
223次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.医院里的血液透析利用了胶体的性质 |
| B.PM2.5中含有铅、铬、钒、砷等对人体有害的金属元素 |
| C.工业冶炼铝常用焦炭还原氧化铝 |
| D.煤经过气化和液化的物理变化可变为清洁燃料 |
【知识点】 化学科学对人类文明发展的意义解读 化学在农业中的应用
| A.该溶液中,H+、NH4+、SO42-、Br-可以大量共存 |
| B.该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存 |
| C.向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+= Cl-+2Fe3++H2O |
| D.向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
【知识点】 离子反应的发生及书写 限定条件下的离子共存解读

| A.有一种物质过量 | B.发生的是分解反应 |
| C.发生的是置换反应 | D.生成了两种产物 |
【知识点】 物质的分类
| A.标准状况下2.24 L HF,分子数为0.1 NA |
| B.将1 mol Cl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2NA |
| C.常温常压下16 g O2和O3混合气体中,氧原子数为NA |
| D.7.8 g Na2O2与足量水反应,转移电子数为0.2NA |
【知识点】 阿伏加德罗常数的求算解读 阿伏加德罗常数的应用解读
二、多选题 添加题型下试题
| A.过量的氢气与氮气 | B.过量的浓盐酸与二氧化锰 |
| C.过量的铜与浓硫酸 | D.过量的锌与18 mol/L硫酸 |
三、单选题 添加题型下试题
①Cl2具有漂白性,可以直接使有色布条褪色;②SO2具有较强的还原性,不能用浓硫酸干燥;③SiO2是酸性氧化物,能与氢氟酸反应;④Al(OH)3是两性氢氧化物,能溶于强酸或强碱。
| A.①②③ | B.②③④ | C.③④ | D.①②④ |
【知识点】 卤素及其化合物
| A.Na2O2能分别与H2O、CO2反应产生氧气,可用作供氧剂 |
| B.硅胶多孔、吸水能力强,常用作袋装食品的干燥剂 |
| C.K2FeO4具有强还原性且被氧化生成Fe3+,可用于水的消毒和净水 |
| D.液氨气化时能吸收大量的热,使周围温度急剧降低,因此可用作制冷剂 |
【知识点】 氮族元素及其化合物
| A.肯定不含I- | B.可能含SO42- |
| C.肯定含有SO32- | D.肯定含有NH4+ |

| A.用图①装置,制取干燥纯净的NH3 |
| B.用图②装置,实验室制备Fe(OH)2 |
| C.用图③所示实验,可比较氯、碳、硅三种元素的非金属性强弱 |
| D.用图④装置测量Cu与浓硝酸反应产生气体的体积 |
【知识点】 氨气的实验室制法解读 物质性质实验方案的设计解读
| A.反应中:转移电子3.01×1022个 | B.反应后:剩余硫酸0.30 mol |
| C.原混合物:n (Fe2O3):n(Fe)=1:2 | D.所得溶液:c(FeSO4)=1.7mol/L |
【知识点】 氧化还原反应有关计算
A. |
B. |
C. |
D. |
【知识点】 二氧化硅的化学性质解读 钠与氧气等非金属的反应解读 铁
| A.等质量的铝分别与足量Fe2O3或Fe3O4发生铝热反应时,转移电子的数目相等 |
| B.质量分数分别为40%和60%的硫酸溶液等体积混合,所得溶液的质量分数为50% |
| C.金属钠着火时,立即用泡沫灭火器灭火 |
| D.洗涤做焰色反应的铂丝,可选用稀盐酸或稀硫酸 |
| A.氟单质与水反应制氧气 | B.钠与水反应制氢气 |
| C.氯气与水反应制次氯酸 | D.过氧化钠与水反应制氧气 |
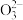 、HC
、HC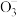 、Al
、Al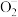 、Al3+的物质的量与加入盐酸的体积变化关系如图所示,则下列说法正确的是( )
、Al3+的物质的量与加入盐酸的体积变化关系如图所示,则下列说法正确的是( )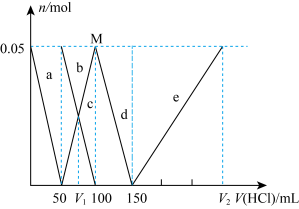
A.原混合溶液中的C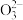 与Al 与Al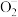 的物质的量之比为1∶2 的物质的量之比为1∶2 |
| B.V1∶V2=1∶5 |
| C.M点时生成的CO2为0.05 mol |
D.a线表示的离子方程式为:Al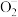 +H++H2O=Al(OH)3↓ +H++H2O=Al(OH)3↓ |
【知识点】 离子方程式的书写解读 偏铝酸钠与盐酸的反应解读

| A.已知C的浓溶液在催化剂存在的条件下加热,能与B反应生成D,由此可以推断B的氧化性比MnO2强 |
B.反应②的离子方程式为MnO2+4H++2Cl- Cl2↑+Mn2++2H2O Cl2↑+Mn2++2H2O |
| C.新配制的F溶液一般需要加入铁屑和稀盐酸,前者用于防止Fe2+被空气氧化成Fe3+,后者可抑制Fe2+的水解 |
| D.若反应①在常温下进行,则1 mol A在反应中能转移1 mol 电子 |
四、解答题 添加题型下试题

(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入
(2)如右图所示,过滤操作中的一处错误是
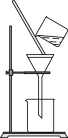
(3)判断流程中沉淀是否洗净所用的试剂是
(4)无水AlCl3(183°C升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
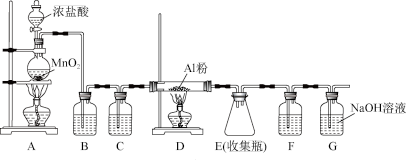
装置 B中盛放饱和NaCl溶液,该装置的主要作用是
五、填空题 添加题型下试题

查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成难溶物Sn(OH)Cl(碱式氯化亚锡)。
III.Sn(OH)2的性质与Al(OH)3性质相似。请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,这样操作的原因是
(2)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子方程式是
(3)将反应I滤液中的溶质提取出来的操作是
(4)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是
(5)称取SnSO4·x H2O晶体50.2g,在隔绝空气的情况下小火加热至结晶水全部失去,冷却称量固体质量为43g,列式计算该晶体的化学式为
【知识点】 化学与材料的发展
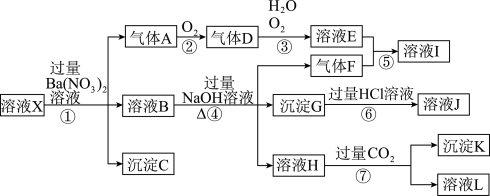
(1)由强酸性条件即可判断溶液X中一定不存在的离子有
(2)溶液X中,关于NO3-的判断一定正确的是
a.一定有 b.一定没有 c.可能有
(3)产生气体A的离子方程式为
(4)转化⑥发生反应的现象为
(5)转化④中产生H的离子方程式为
(6)若转化③中,D、H2O、O2三种物质恰好发生化合反应生成E,则反应中D与O2的物质的量之比为
(7)对不能确定是否存在的离子,可以另取X溶液,加入下列溶液中的一种,根据现象即可判断,该试剂最好是
①NaOH溶液,②KSCN溶液,③石蕊试剂,④pH试纸,⑤KMnO4溶液,⑥氯水和KSCN的混合溶液
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读 无机综合推断 离子的检验
六、计算题 添加题型下试题
(1)NO的体积为
(2)参加反应的硝酸的物质的量是
(3)待产生的气体全部释放后,向溶液加入VmL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水
试卷分析
试卷题型(共 20题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 化学科学对人类文明发展的意义 化学在农业中的应用 | |
| 2 | 0.4 | 离子反应的发生及书写 限定条件下的离子共存 | |
| 3 | 0.64 | 物质的分类 | |
| 4 | 0.65 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 | |
| 5 | 0.64 | 氧族元素及其化合物 | |
| 7 | 0.64 | 卤素及其化合物 | |
| 8 | 0.64 | 氮族元素及其化合物 | |
| 9 | 0.65 | 限定条件下的离子共存 离子反应在化合物组成的分析、鉴定的应用 | |
| 10 | 0.65 | 氨气的实验室制法 物质性质实验方案的设计 | |
| 11 | 0.65 | 氧化还原反应有关计算 | |
| 12 | 0.65 | 二氧化硅的化学性质 钠与氧气等非金属的反应 铁 | |
| 13 | 0.65 | 物质的量有关计算 钠 焰色试验 | |
| 14 | 0.65 | 氧化还原反应的几组概念 氯气与水的反应 钠与水反应原理 过氧化钠与水的反应 | |
| 15 | 0.65 | 离子方程式的书写 偏铝酸钠与盐酸的反应 | |
| 16 | 0.4 | 氯气 铁的其他化合物 | |
| 二、多选题 | |||
| 6 | 0.65 | 氯气的制法 氮气 硫酸 | |
| 三、解答题 | |||
| 17 | 0.65 | 仪器使用与实验安全 常见无机物的制备 常见气体的制备与收集 化学实验方案的设计与评价 | 实验探究题 |
| 四、填空题 | |||
| 18 | 0.4 | 化学与材料的发展 | |
| 19 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 无机综合推断 离子的检验 | |
| 五、计算题 | |||
| 20 | 0.65 | 基于氧化还原反应守恒规律的计算 有关酸性环境下硝酸根氧化性的有关计算 铜与强氧化性酸的反应 | |




