湖北省武汉市华中师大一附中高三理科四调综合训化学试题
湖北
高三
模拟预测
2020-04-30
1065次
整体难度:
适中
考查范围:
化学反应原理、化学与STSE、认识化学科学、物质结构与性质、有机化学基础、化学实验基础
湖北省武汉市华中师大一附中高三理科四调综合训化学试题
湖北
高三
模拟预测
2020-04-30
1065次
整体难度:
适中
考查范围:
化学反应原理、化学与STSE、认识化学科学、物质结构与性质、有机化学基础、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
解题方法
1. 2019年7月1日起,上海进入垃圾分类强制时代,随后全国各地也纷纷开始实行垃圾分类。这体现了我国保护环境的决心,而环境保护与化学息息相关,下列有关说法正确的是( )
| A.废弃的聚乙烯塑料属于白色垃圾,不可降解,能使溴水褪色 |
| B.可回收的易拉罐中含金属铝,可通过电解氯化铝制取 |
| C.含棉、麻、丝、毛及合成纤维的废旧衣物燃烧处理时均只生成CO2和H2O |
| D.废旧电池中含有镍、镉等重金属,不可用填埋法处理 |
您最近一年使用:0次
2020-06-03更新
|
529次组卷
|
15卷引用:四川省天府名校2020届高三上学期第一轮联合质量测评化学试题
四川省天府名校2020届高三上学期第一轮联合质量测评化学试题河北省“五个一”名校联盟2020届高三上学期一轮复习收官考试理综化学试题河北省廊坊市三河市第三中学2020届高三12月月考理综化学考试题2020届高三《新题速递·化学》12月第01期(考点01-06)2020届高三《新题速递·化学》1月第02期(考点01-06)陕西省西安市西安中学2020届高三下学期第3次考试化学试题天津塘沽一中2020届高三3月网上测试化学试题湖北省武汉市华中师大一附中高三理科四调综合训化学试题天津市塘沽一中2020届高三第二次模拟考试化学试题宁夏回族自治区银川一中2019-2020学年高一下学期期中考试化学试题重庆育才中学高2020级高三下学期入学考试理科化学试题广西名校高三2019-2020学年第一学期第一次大联考-化学西南四省名校2020届高三第一次大联考理综化学试题河北省安平中学2019--2020学年下学期高一第二次质量检测考试化学试题海南省琼海市嘉积第三中学2021-2022学年高三下学期第二次月考化学科试题
单选题
|
较难(0.4)
名校
2. NA为阿伏加 德罗常数的值。关于常温下pH=2的H2SO4溶液,溶液中不存在H2SO4分子,但存在HSO4一离子,下列说法错误的是
| A.每升溶液中的H+数目为0.01NA |
| B.Na2SO4溶液中:c(Na+)=2c(SO42-)>c(H+)=2c(OH-) |
C.向稀硫酸中逐滴滴加浓硫酸,溶液中 减小 减小 |
| D.NaHSO4不是弱电解质 |
【知识点】 弱电解质的电离平衡
您最近一年使用:0次
2019-12-26更新
|
548次组卷
|
4卷引用:2019年四川省南充市高考第一次高考适应性考试理综化学试题
单选题
|
适中(0.65)
名校
解题方法
3. 一定量的某磁黄铁矿(主要成分FexS,S为-2价)与100mL盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成3.2g硫单质、0.4molFeCl2和一定量H2S气体,且溶液中无Fe3+。则下列说法正确的是( )
| A.该盐酸的物质的量浓度为4.0mol·L-1 |
| B.该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为2:1 |
| C.生成的H2S气体在标准状况下的体积为8.96L |
| D.该磁黄铁矿中FexS的x=0.85 |
【知识点】 基于氧化还原反应守恒规律的计算解读
您最近一年使用:0次
2020-01-04更新
|
1426次组卷
|
18卷引用:2019年湖南省永州市高三上学期第一次模拟考试化学试卷
2019年湖南省永州市高三上学期第一次模拟考试化学试卷2020届高三《新题速递·化学》1月第02期(考点01-06)陕西省西安市西安中学2020届高三下学期第3次考试化学试题山东省日照一中2020届高三新高考3月份自测化学试题河南省郑州市第一中学2020届高三下学期周考理科综合化学试题湖北省武汉市华中师大一附中高三理科四调综合训化学试题河南省郑州市第一中学2021届高三上学期开学测试化学试题鲁科版(2019)高一必修第一册第二章B 素养拓展区 过综合 章末素养综合检测江西省南昌市实验中学2022届高三第一次模拟考试化学试题江西省抚州市黎川县第一中学2021-2022学年上学期高三第三次同步考试化学试题湖南省娄底涟源市第一中学2022届高三下学期四月月考化学试题(已下线)专题04氧化还原反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题04氧化还原反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题04氧化还原反应-三年(2020~2022)高考真题汇编(全国卷)山东省东营市胜利第一中学2022届高三仿真演练押题化学试题江西省新余市第一中学2022-2023学年高三上学期新生入学考试化学试题福建省厦门第一中学2023-2024学年高一上学期12月月考化学试题福建省厦门第一中学2023-2024学年高一上学期第二次月考化学试卷
单选题
|
较易(0.85)
名校
4. 短周期主族元素W、X、Y、Z的原子序数依次增大,W在大气中有两种同素异形体且均能支持燃烧,X的原子半径是所有短周期主族元素中最大的,非金属元素Y的原子序数是Z的最外层电子数的2倍。下列叙述不正确的是( )
| A.Y、Z的氢化物稳定性Y>Z |
| B.Y单质的熔点高于X单质 |
| C.X、W、Z能形成具有强氧化性的XZW |
D. 中W和Y都满足8电子稳定结构 中W和Y都满足8电子稳定结构 |
您最近一年使用:0次
2019-12-31更新
|
484次组卷
|
6卷引用:2019年四川省雅安市高三第一次诊断考试理综化学试题
单选题
|
较易(0.85)
名校
解题方法
5. 碳酸亚乙酯是一种重要的添加剂,其结构简式为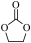 。用环氧乙烷合成碳酸亚乙酯的反应为:
。用环氧乙烷合成碳酸亚乙酯的反应为: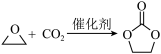 。下列说法错误的是
。下列说法错误的是
 。用环氧乙烷合成碳酸亚乙酯的反应为:
。用环氧乙烷合成碳酸亚乙酯的反应为: 。下列说法错误的是
。下列说法错误的是| A.上述反应属于加成反应 |
| B.碳酸亚乙酯的二氯代物只有两种 |
| C.碳酸亚乙酯中的所有原子处于同一平面内 |
| D.1mol碳酸亚乙酯最多可消耗2molNaOH |
您最近一年使用:0次
2020-01-15更新
|
333次组卷
|
4卷引用:山东省泰安市2020届高三上学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
6. 十九大报告中提出要“打赢蓝天保卫战”,意味着对污染防治比过去要求更高。某种利用垃圾渗透液实现发电、环保二位一体结合的装置示意图如下,当该装置工作时,下列说法正确的是


| A.盐桥中Cl-向Y极移动 |
| B.电路中流过7.5 mol电子时,共产生标准状况下N2的体积为16.8L |
| C.电流由X极沿导线流向Y极 |
| D.Y极发生的反应为2NO3-+10e-+6H2O=N2↑+12OH-,周围pH增大 |
您最近一年使用:0次
2021-08-05更新
|
1217次组卷
|
25卷引用:湖北省荆门市2019—2020学年高三上学期元月调研考试理综化学试题
湖北省荆门市2019—2020学年高三上学期元月调研考试理综化学试题2020届高三《新题速递·化学》1月第02期(考点07-10)【百强校】江西省南昌市第十中学2020届高三下学期综合模拟考试化学试题湖北省武汉市华中师大一附中高三理科四调综合训化学试题天津市七校联考2020届高三二模化学试卷福建省安溪一中、养正中学、惠安一中、泉州实验中学2020-2021学年高二上学期期中联考化学试题(已下线)模块八 电化学基础(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省大庆铁人中学2021-2022学年高二上学期开学考试化学试题(已下线)专题讲座(四)新型电源及电极反应式的书写(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)1.2.1 原电池的工作原理-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)江苏省华东师范大学盐城实验中学2021-2022学年高二上学期第一次月考化学试题 江西省崇义中学2020-2021学年高一上学期期中考试(A卷)化学试题(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-测试甘肃省天水市第一中学2021-2022学年高二下学期开学检测化学试题福建省漳州第一中学2021-2022学年高三下学期第五次阶段考化学试题(已下线)必刷卷03-2022年高考化学考前信息必刷卷(山东专用)湖南省株洲市醴陵市第一中学2021-2022学年高三下学期期中考试化学试题福建省福州市三校2022-2023学年高二上学期期中联考化学试题山东省烟台市福山区第一中学2021-2022学年高三上学期9月月考化学试题.河南省信阳市普通高中2022-2023学年高三上学期第二次教学质量检测化学试题福建省福州第二中学2022-2023学年高二上学期期末考试化学试题河南省信阳高级中学2022-2023学年高二下学期开学考试化学试题江苏省苏州第一中学校2023-2024学年高二上学期10月月考化学试题
单选题
|
较难(0.4)
名校
解题方法
7. 下列设计的实验方案能达到相应实验目的的是
选项 | 实验目的 | 实验方案 |
A | 探究化学反应的 限度 | 取5mL0.1mol/LKI溶液,滴加0.1mol/LFeCl3溶液5~6滴,充分反应,可根据溶液中既含I2又含I-的实验事实判断该反应是可逆反应 |
B | 探究浓度对化学反应速率的影响 | 用两支试管各取5mL0.1mol/L的KMnO4溶液,分别加入2mL0.1mol/L和0.2mol/L的草酸溶液,记录溶液褪色所需的时间 |
C | 证明溴乙烷的消去反应有乙烯生成 | 将NaOH的乙醇溶液加入溴乙烷中加热,将产生的气体直接通入酸性KMnO4溶液中 |
D | 验证醋酸钠溶液中存在水解平衡 | 取CH3COONa溶液于试管中并加入几滴酚酞试剂,再加入醋酸铵固体其水溶液呈中性,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-04-02更新
|
1411次组卷
|
7卷引用:重庆市北碚区2020届高三上学期第一次诊断性考试理综化学试题
重庆市北碚区2020届高三上学期第一次诊断性考试理综化学试题天津塘沽一中2020届高三3月网上测试化学试题(已下线)2020年高考化学押题预测卷02(新课标Ⅰ卷)--《2020年高考押题预测卷》湖北省武汉市华中师大一附中高三理科四调综合训化学试题天津市塘沽一中2020届高三第二次模拟考试化学试题西藏山南市第二高级中学2020届高三第三次模拟考试理综化学试题海南省三亚市第一中学2021-2022学年高三下学期最后一卷化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
8. 三氯乙醛(CCl3CHO)是生产农药、医药的重要中间体,实验室制备三氯乙醛的反应装置示意图(加热装置未画出)和有关数据如下:

①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
②相关物质的相对分子质量及部分物理性质:
(1)恒压漏斗中盛放的试剂的名称是_____ ,盛放KMnO4仪器的名称是_____ 。
(2)反应过程中C2H5OH和HCl可能会生成副产物C2H5Cl,同时CCl3CHO(三氯乙醛)也能被次氯酸继续氧化生成CCl3COOH(三氯乙酸),写出三氯乙醛被次氯酸氧化生成三氯乙酸的化学方程式:_____ 。
(3)该设计流程中存在一处缺陷是_____ ,导致引起的后果是_____ ,装置B的作用是______ 。
(4)反应结束后,有人提出先将C中的混合物冷却到室温,再用分液的方法分离出三氯乙酸。你认为此方案是否可行_____ (填是或否),原因是_____ 。
(5)测定产品纯度:称取产品0.36g配成待测溶液,加入0.1000mol•L−1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mol•L−1Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液20.00mL。则产品的纯度为_____ (计算结果保留四位有效数字)。滴定原理:CCl3CHO+OH-=CHCl3+HCOO-、HCOO-+I2=H++2I-+CO2、I2+2S2O32-=2I-+S4O62-

①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
②相关物质的相对分子质量及部分物理性质:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | |
| C2H5OH | 46 | -114.1 | 78.3 | 与水互溶 |
| CCl3CHO | 147.5 | -57.5 | 97.8 | 可溶于水、乙醇 |
| CCl3COOH | 163.5 | 58 | 198 | 可溶于水、乙醇、三氯乙醛 |
| C2H5Cl | 64.5 | -138.7 | 12.3 | 微溶于水,可溶于乙醇 |
(1)恒压漏斗中盛放的试剂的名称是
(2)反应过程中C2H5OH和HCl可能会生成副产物C2H5Cl,同时CCl3CHO(三氯乙醛)也能被次氯酸继续氧化生成CCl3COOH(三氯乙酸),写出三氯乙醛被次氯酸氧化生成三氯乙酸的化学方程式:
(3)该设计流程中存在一处缺陷是
(4)反应结束后,有人提出先将C中的混合物冷却到室温,再用分液的方法分离出三氯乙酸。你认为此方案是否可行
(5)测定产品纯度:称取产品0.36g配成待测溶液,加入0.1000mol•L−1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mol•L−1Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液20.00mL。则产品的纯度为
您最近一年使用:0次
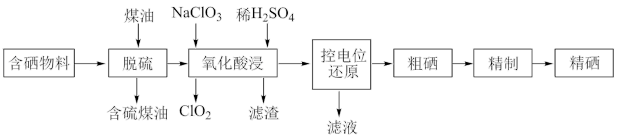
9. 随着人们对硒的性质深入认识及产品硒的纯度提高,硒的应用范围越来越广。某科学小组以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、Fe2O3、CuO、ZnO、SiO2等)提取硒,设计流程如下:______ 。最佳温度是________ 。
(2)“氧化酸浸”中,Se转化成H2SeO3,该反应的离子方程式为_____________ 。
(3)采用硫脲[(NH2)2CS]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。下表是“氧化酸浸”液中主要粒子的电位。
①控制电位在0.740~1.511V范围内,在氧化酸浸液中添加硫脲,可选择性还原ClO2。该过程的还原反应(半反应)式为___________ 。
②为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在_____ V。
(4)粗硒的精制过程:Na2SO3浸出[Se转化成硒代硫酸钠(Na2SeSO3)]→Na2S净化→H2SO4酸化等步骤。
①净化后的溶液中c(S2-)达到0.026 mol·L-1,此时溶液中的c(Cu2+)的最大值为________ ,精硒中基本不含铜。[Ksp(CuS)=1.3×10-36]
②硒代硫酸钠酸化生成硒的化学方程式为____________ 。
(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μg·g-1,则精硒中铁的质量分数为________ %,与粗硒中铁含量为0.89%相比,铁含量明显降低。

(2)“氧化酸浸”中,Se转化成H2SeO3,该反应的离子方程式为
(3)采用硫脲[(NH2)2CS]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。下表是“氧化酸浸”液中主要粒子的电位。
| 名称 | Cu2+/Cu | Zn2+/Zn | Fe2+/Fe | Fe3+/Fe2+ | ClO2/Cl- | H2SeO3/Se |
| 电位/V | 0.345 | -0.760 | -0.440 | 0.770 | 1.511 | 0.740 |
②为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在
(4)粗硒的精制过程:Na2SO3浸出[Se转化成硒代硫酸钠(Na2SeSO3)]→Na2S净化→H2SO4酸化等步骤。
①净化后的溶液中c(S2-)达到0.026 mol·L-1,此时溶液中的c(Cu2+)的最大值为
②硒代硫酸钠酸化生成硒的化学方程式为
(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μg·g-1,则精硒中铁的质量分数为
您最近一年使用:0次
2020-02-11更新
|
831次组卷
|
6卷引用:福建省宁德市2019-2020学年高三上学期期末质量检测理综化学试题
福建省宁德市2019-2020学年高三上学期期末质量检测理综化学试题(已下线)2020届高三《新题速递·化学》2月第01期(考点10-12)河北省衡水中学2020届高三下学期一调理综化学试题(已下线)考点17 化工生产诸要素及流程图分析-2020年高考化学命题预测与模拟试题分类精编湖北省武汉市华中师大一附中高三理科四调综合训化学试题(已下线)微专题35 非金属及其化合物制备流程与实验探究(S、Se、Te、Cl、Br、I)-备战2022年高考化学考点微专题
解答题-原理综合题
|
适中(0.65)
名校
解题方法
10. 随着氮氧化物对环境及人类活动影响的日趋严重,如何消除大气污染物中的氮氧化物成为人们关注的主要问题之一。
Ⅰ.利用NH3的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:4NH3(g)+6NO(g) 5N2(g)+6H2O(l) △H<0
5N2(g)+6H2O(l) △H<0
(1)写出一种可以提高NO的转化率的方法:__________
(2)一定温度下,在恒容密闭容器中按照n(NH3)︰n(NO) =2︰3充入反应物,发生上述反应。下列不能 判断该反应达到平衡状态的是___________
A.c(NH3)︰c(NO) =2︰3 B.n(NH3)︰n(N2) 不变 C.容器内压强不变 D.容器内混合气体的密度不变 E.1molN—H键断裂的同时,生成1molO—H键
(3)已知该反应速率v正=k正·c4(NH3)·c6 (NO),v逆=k逆·cx(N2)·cy(H2O) (k正、k逆分别是正、逆反应速率常数),该反应的平衡常数K=k正/k逆,则x=_____ ,y=_______ 。
(4)某研究小组将2molNH3、3molNO和一定量的O2充入2L密闭容器中,在Ag2O催化剂表面发生上述反应,NO的转化率随温度变化的情况如图所示:
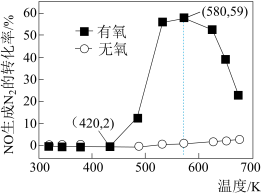
①在5min内,温度从420K升高到580K,此时段内NO的平均反应速率v(NO)=_______ ;
②在有氧条件下,温度580K之后NO生成N2的转化率降低的原因可能是___________ 。
Ⅱ.用尿素[(NH2)2CO]水溶液吸收氮氧化物也是一种可行的方法。NO和NO2不同配比混合气通入尿素溶液中,总氮还原率与配比关系如图。
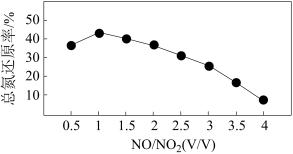
(5) 用尿素[(NH2)2CO]水溶液吸收体积比为1∶1的NO和NO2混合气,可将N元素转变为对环境无害的气体。写出该反应的化学方程式____ 。
(6)随着NO和NO2配比的提高,总氮还原率降低的主要原因是________________ 。
Ⅰ.利用NH3的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:4NH3(g)+6NO(g)
 5N2(g)+6H2O(l) △H<0
5N2(g)+6H2O(l) △H<0(1)写出一种可以提高NO的转化率的方法:
(2)一定温度下,在恒容密闭容器中按照n(NH3)︰n(NO) =2︰3充入反应物,发生上述反应。下列
A.c(NH3)︰c(NO) =2︰3 B.n(NH3)︰n(N2) 不变 C.容器内压强不变 D.容器内混合气体的密度不变 E.1molN—H键断裂的同时,生成1molO—H键
(3)已知该反应速率v正=k正·c4(NH3)·c6 (NO),v逆=k逆·cx(N2)·cy(H2O) (k正、k逆分别是正、逆反应速率常数),该反应的平衡常数K=k正/k逆,则x=
(4)某研究小组将2molNH3、3molNO和一定量的O2充入2L密闭容器中,在Ag2O催化剂表面发生上述反应,NO的转化率随温度变化的情况如图所示:

①在5min内,温度从420K升高到580K,此时段内NO的平均反应速率v(NO)=
②在有氧条件下,温度580K之后NO生成N2的转化率降低的原因可能是
Ⅱ.用尿素[(NH2)2CO]水溶液吸收氮氧化物也是一种可行的方法。NO和NO2不同配比混合气通入尿素溶液中,总氮还原率与配比关系如图。

(5) 用尿素[(NH2)2CO]水溶液吸收体积比为1∶1的NO和NO2混合气,可将N元素转变为对环境无害的气体。写出该反应的化学方程式
(6)随着NO和NO2配比的提高,总氮还原率降低的主要原因是
您最近一年使用:0次
2020-01-16更新
|
313次组卷
|
4卷引用:福建省龙岩市2020届高三上学期期末考试化学试题
福建省龙岩市2020届高三上学期期末考试化学试题(已下线)2020届高三《新题速递·化学》2月第01期(考点10-12)广东省兴宁一中2020届高三年级3月质量检测考试(全国I卷)理综化学试题湖北省武汉市华中师大一附中高三理科四调综合训化学试题
解答题-结构与性质
|
较难(0.4)
名校
解题方法
11. 微量元素硼和镁对植物的叶的生长和人体骨骼的健康有着十分重要的作用,其化合物也应用广泛。
(1)基态B原子的电子排布图为________________________ ,其第一电离能比Be___________ (填“大”或“小”)。
(2)三价B易形成配离子,如[B(OH)4]-、[BH4]-等。[B(OH)4]-的结构简式为___________ (标出配位键),其中心原子的杂化方式为________ ,写出[BH4]-的一种阳离子等电子体_______ 。
(3)下图表示多硼酸根的一种无限长的链式结构,其化学式可表示为____________ (以n表示硼原子的个数)。
(4)硼酸晶体是片层结构,下图表示的是其中一层的结构。每一层内存在的作用力有_________ 。
(5)三氯化硼的熔点比氯化镁的熔点低,原因是_______________________ 。
(6)镁单质晶体中原子的堆积模型如下图,它的堆积模型名称为_______ ;紧邻的四个镁原子的中心连线构成的正四面体几何体的体积是2a cm3,镁单质的密度为ρ g·cm-3,已知阿伏加 德罗常数为NA,则镁的摩尔质量的计算式是________________ 。
(1)基态B原子的电子排布图为
(2)三价B易形成配离子,如[B(OH)4]-、[BH4]-等。[B(OH)4]-的结构简式为
(3)下图表示多硼酸根的一种无限长的链式结构,其化学式可表示为
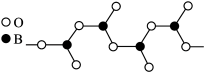
(4)硼酸晶体是片层结构,下图表示的是其中一层的结构。每一层内存在的作用力有
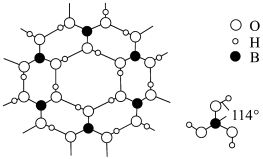
(5)三氯化硼的熔点比氯化镁的熔点低,原因是
(6)镁单质晶体中原子的堆积模型如下图,它的堆积模型名称为
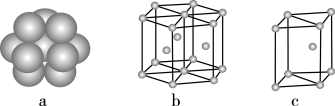
您最近一年使用:0次
2019-06-01更新
|
1237次组卷
|
6卷引用:湖北省部分重点中学2018-2019学年下学期高二期末联考化学试题
解答题-有机推断题
|
适中(0.65)
12. 有机物 W 在医药和新材料等领域有广泛应用。W 的一种合成路线如图:

已知部分信息如下:
请回答下列问题:
(1)Y 的化学名称是___ ;Z 中官能团的名称是___ ;
(2) 中
中_____________ (填“有”或“无”)手性碳原子;图示中 X 转化为 Y 的反应类型是___ 。
(3)生成 W 的化学方程式为___ 。
(4)G 是对硝基乙苯的同分异构体,G 能和碳酸钠反应产生气体且分子中含有—NH2(氨基),G的同分异构体有___ 种(不考虑立体结构),其中在核磁共振氢谱上峰的面积比为 1∶2∶2∶2∶2 的结构简式为_________________ 。
(5)设计以苯乙烯和丙酮为原料制备药物中间体 的合成路线
的合成路线__________ (无机试剂自选)。

已知部分信息如下:
| ① | 1molY完全反应生成2molZ,且在加热条件下Z不能和新制氢氧化铜悬浊液反应 |
| ② |  +R1COOH +R1COOH |
| ③ | RCH2NH2+ +H2O +H2O |
(1)Y 的化学名称是
(2)
 中
中(3)生成 W 的化学方程式为
(4)G 是对硝基乙苯的同分异构体,G 能和碳酸钠反应产生气体且分子中含有—NH2(氨基),G的同分异构体有
(5)设计以苯乙烯和丙酮为原料制备药物中间体
 的合成路线
的合成路线
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学反应原理、化学与STSE、认识化学科学、物质结构与性质、有机化学基础、化学实验基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 废弃电池的污染及回收 化学科学对人类文明发展的意义 “白色污染”危害及防治 塑料 | |
| 2 | 0.4 | 弱电解质的电离平衡 | |
| 3 | 0.65 | 基于氧化还原反应守恒规律的计算 | |
| 4 | 0.85 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 “位构性”关系理解及应用 | |
| 5 | 0.85 | 有机官能团的性质及结构 同分异构体的数目的确定 有机分子中原子共面的判断 多官能团有机物的结构与性质 | |
| 6 | 0.65 | 原电池电子流向判断及应用 原电池正负极判断 原电池电极反应式书写 原电池有关计算 | |
| 7 | 0.4 | 测定某些反应的反应速率 探究影响盐类水解平衡的因素 物质的检验 化学实验方案的设计与评价 | |
| 二、解答题 | |||
| 8 | 0.4 | 常见有机物的制备 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 9 | 0.4 | 化学反应条件的控制及优化 溶度积常数相关计算 常见无机物的制备 探究物质组成或测量物质的含量 | 工业流程题 |
| 10 | 0.65 | 化学反应速率计算 化学平衡状态的判断方法 化学平衡常数的概念及表达方式 转化率的相关计算及判断 | 原理综合题 |
| 11 | 0.4 | 物质结构与性质综合考查 利用杂化轨道理论判断化学键杂化类型 配合物的结构与性质 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 根据要求书写同分异构体 有机物的合成 根据题给物质选择合适合成路线 信息给予的有机合成 | 有机推断题 |



