某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是___________ 。
(2)该反应中,发生还原反应的过程是_____________ →_____________ 。
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目:_________ 。
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为_________ L。
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目:
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为
2017高一·全国·课时练习 查看更多[3]
更新时间:2017-11-27 16:01:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】. 用双线桥法表示下列化学反应中的电子转移情况,是离子反应的将其改写为离子方程式,不是离子反应的可不填.
(1) 加热硝酸铵_______
5NH4NO3 4N2↑+2HNO3+9H2O
4N2↑+2HNO3+9H2O
(2)在含有Na2S和Na2SO3的溶液中,加入稀硫酸_______
2Na2S+Na2SO3+3H2SO4==3Na2SO4+3S↓+3H2O
(3)铜片与稀硝酸反应_______
3Cu+8HNO3(稀)===3Cu(NO3)2+2NO+4H2O
(1) 加热硝酸铵
5NH4NO3
 4N2↑+2HNO3+9H2O
4N2↑+2HNO3+9H2O(2)在含有Na2S和Na2SO3的溶液中,加入稀硫酸
2Na2S+Na2SO3+3H2SO4==3Na2SO4+3S↓+3H2O
(3)铜片与稀硝酸反应
3Cu+8HNO3(稀)===3Cu(NO3)2+2NO+4H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】黑火药是中国的“四大发明”之一.黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S═K2S+N2↑+3CO2↑.该反应中,被氧化的元素是______ ,氧化剂是______ ,氧化产物是______ .
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
I.KClO3和浓盐酸在一定温度下反应会生成黄绿色的有毒气体氯气。其变化可表示为: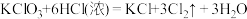 。
。
(1)请用“双线桥”表示上述反应电子转移的方向和数目___________ 。
(2)反应中,氧化剂为___________ ,氧化产物为:___________ 。
(3)浓盐酸在反应中体现出来的性质有___________ (填序号)。
①还原性 ②酸性 ③氧化性 ④碱性
Ⅱ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为 ,该反应中还原剂是
,该反应中还原剂是___________ 。(填化学式)
(5)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。
、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:___________ 。
②每生成1个 转移
转移___________ 个电子。
I.KClO3和浓盐酸在一定温度下反应会生成黄绿色的有毒气体氯气。其变化可表示为:
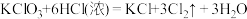 。
。(1)请用“双线桥”表示上述反应电子转移的方向和数目
(2)反应中,氧化剂为
(3)浓盐酸在反应中体现出来的性质有
①还原性 ②酸性 ③氧化性 ④碱性
Ⅱ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为
 ,该反应中还原剂是
,该反应中还原剂是(5)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。
、Cl-、H2O。①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成1个
 转移
转移
您最近一年使用:0次
【推荐1】根据氮及其化合物的转化关系回答下列问题:
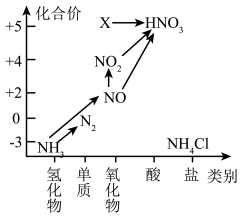
(1)X的化学式为_______ ,从化合价上看,X 具有_______ 性(填“氧化”或“还原”)。
(2)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为_______ ;下列试剂不能用于干燥NH3的是 _______ (填字母)。
A.浓硫酸 B.碱石灰 C. NaOH固体 D.无水CaCl2
(3)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO的化学方程式为_______ 。
②NO→NO2实验现象是_______ 。
③NO2+H2O→HNO3氧化剂与还原剂物质的量之比为_______ 。

(1)X的化学式为
(2)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
A.浓硫酸 B.碱石灰 C. NaOH固体 D.无水CaCl2
(3)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO的化学方程式为
②NO→NO2实验现象是
③NO2+H2O→HNO3氧化剂与还原剂物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O。
(1)被氧化的元素是________ ,被还原的元素是_______ ,发生氧化反应的物质是_______ ,发生还原反应的物质是_______ 。NO是否是酸性氧化物_______ (填“是”或“否”)。
(2)用双线桥法表示反应中电子转移的方向和数目________ 。
(3)用单线桥法表示反应中电子转移的方向和数目________ 。
(1)被氧化的元素是
(2)用双线桥法表示反应中电子转移的方向和数目
(3)用单线桥法表示反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知反应:
①SO3+H2O=H2SO4
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤Na2O+2HCl=2NaCl+H2O
⑥Al2O3+2NaOH=2NaAlO2+H2O
(1)上述反应不属于氧化还原反应的有___________ (填序号,下同)。H2O被氧化的是___________ ,H2O被还原的是___________ 。
(2)用双线桥法表示反应②的电子转移方向和数目:___________ 。
(3)用单线桥法表示反应③的电子转移方___________ 。
(4)写出反应④的离子方程式:___________ 。
①SO3+H2O=H2SO4
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤Na2O+2HCl=2NaCl+H2O
⑥Al2O3+2NaOH=2NaAlO2+H2O
(1)上述反应不属于氧化还原反应的有
(2)用双线桥法表示反应②的电子转移方向和数目:
(3)用单线桥法表示反应③的电子转移方
(4)写出反应④的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某反应中反应物与生成物有: 、
、 、
、 、
、 、
、 、
、 和一种未知物质X。
和一种未知物质X。
(1)已知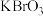 在反应中得到电子,则该反应的还原剂是
在反应中得到电子,则该反应的还原剂是___________ ;
(2)已知2个 在反应中得到10个电子生成X,则X的化学式为
在反应中得到10个电子生成X,则X的化学式为___________ 。
(3)根据上述反应可推知___________。
(4)请配平下面反应的反应方程式,并用单线桥法标出转移电子的方向和数目___________ 。

 、
、 、
、 、
、 、
、 、
、 和一种未知物质X。
和一种未知物质X。(1)已知
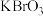 在反应中得到电子,则该反应的还原剂是
在反应中得到电子,则该反应的还原剂是(2)已知2个
 在反应中得到10个电子生成X,则X的化学式为
在反应中得到10个电子生成X,则X的化学式为(3)根据上述反应可推知___________。
A.氧化性: | B.氧化性: |
C.还原性: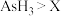 | D.还原性: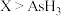 |

您最近一年使用:0次
【推荐3】(1)已知甲、乙两物质分别由H、C、Na、O、Cl、Fe元素中的一种或几种组成,请按要求填空:
①若甲物质为碱性氧化物,则甲的化学式为___________________ (写一种)。
②若乙物质可用于呼吸面具中作为氧气来源,则乙是___________ ,其供氧原理是__________ (用化学方程式表示)。
(2)在横线上填入合适的符号:________ +2H+=CO2↑+H2O+Ba2+
(3)写出氯气与水反应的化学方程式,并用双线桥法标出电于转移的方向和数目:______________________________________________________ 。
(4)选择合适的试剂除去下列括号内的杂质。(填化学式)
①若甲物质为碱性氧化物,则甲的化学式为
②若乙物质可用于呼吸面具中作为氧气来源,则乙是
(2)在横线上填入合适的符号:
(3)写出氯气与水反应的化学方程式,并用双线桥法标出电于转移的方向和数目:
(4)选择合适的试剂除去下列括号内的杂质。(填化学式)
| 物质 | 选择的试剂 |
| ①FeCl2(FeCl3) | |
| ②NO气体(NO2) |
您最近一年使用:0次
【推荐1】二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。已知:工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。
完成下列填空:
(1)将二氧化氯通入品红试液中,看到的现象是__ ;理由是__ 。
(2)请配平下列反应的化学方程式(CH3OH中H为+1价,O为-2价):
___CH3OH+__NaClO3+__→__CO2↑+__C1O2↑+__Na2SO4+__□__
(3)该反应中,被氧化的元素是__ 。还原产物与氧化产物的物质的量之比是__ 。
(4)根据上述反应可推知__ 。
a.氧化性:C1O2>NaClO3 b.氧化性:NaClO3>CH3OH
c.还原性:CH3OH>ClO2 d.还原性:CH3OH>Na2SO4
(5)若转移的电子数目为0.3NA(NA为阿伏加 德罗常数),则反应产生气体(标准状况)为__ 升。
(6)消毒效率常以单位质量的消毒剂得到的电子数表示。ClO2的消毒效率是Cl2的__ 倍。
完成下列填空:
(1)将二氧化氯通入品红试液中,看到的现象是
(2)请配平下列反应的化学方程式(CH3OH中H为+1价,O为-2价):
___CH3OH+__NaClO3+__→__CO2↑+__C1O2↑+__Na2SO4+__□
(3)该反应中,被氧化的元素是
(4)根据上述反应可推知
a.氧化性:C1O2>NaClO3 b.氧化性:NaClO3>CH3OH
c.还原性:CH3OH>ClO2 d.还原性:CH3OH>Na2SO4
(5)若转移的电子数目为0.3NA(NA为阿伏加 德罗常数),则反应产生气体(标准状况)为
(6)消毒效率常以单位质量的消毒剂得到的电子数表示。ClO2的消毒效率是Cl2的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氧化还原反应是一类重要的化学反应,在工农业生产、日常生活中都有广泛的用途。
请回答下列问题。
Ⅰ.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式: 。
。 、
、 、
、 、
、 四种物质中的一种物质(甲)能使上述还原过程发生。
四种物质中的一种物质(甲)能使上述还原过程发生。
(1)物质(甲)为_______ (填化学式)。
(2)反应中若产生5molNO分子,则转移电子的数目是_______ 。
Ⅱ.亚硝酸钠( )像食盐一样有咸味但有很强的毒性,误食
)像食盐一样有咸味但有很强的毒性,误食 会使人中毒。已知亚硝酸钠能发生如下反应:
会使人中毒。已知亚硝酸钠能发生如下反应: 。
。
(3)用双线桥法标出该反应中电子转移的方向及数目:_______ ,被氧化的原子与被还原的原子数目之比为_______ 。
(4)自来水中的 对人类健康会产生危害碱性条件下Al粉还原
对人类健康会产生危害碱性条件下Al粉还原 ,产物是
,产物是 ,发生的反应可表示如下,完成方程式并配平。
,发生的反应可表示如下,完成方程式并配平。_______
_______Al+_______ +_______
+_______ _______
_______ _______
_______ _______
_______
请回答下列问题。
Ⅰ.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
 。
。 、
、 、
、 、
、 四种物质中的一种物质(甲)能使上述还原过程发生。
四种物质中的一种物质(甲)能使上述还原过程发生。(1)物质(甲)为
(2)反应中若产生5molNO分子,则转移电子的数目是
Ⅱ.亚硝酸钠(
 )像食盐一样有咸味但有很强的毒性,误食
)像食盐一样有咸味但有很强的毒性,误食 会使人中毒。已知亚硝酸钠能发生如下反应:
会使人中毒。已知亚硝酸钠能发生如下反应: 。
。(3)用双线桥法标出该反应中电子转移的方向及数目:
(4)自来水中的
 对人类健康会产生危害碱性条件下Al粉还原
对人类健康会产生危害碱性条件下Al粉还原 ,产物是
,产物是 ,发生的反应可表示如下,完成方程式并配平。
,发生的反应可表示如下,完成方程式并配平。_______Al+_______
 +_______
+_______ _______
_______ _______
_______ _______
_______
您最近一年使用:0次
填空题
|
适中
(0.65)
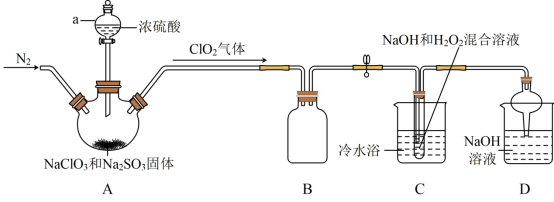
【推荐3】二氧化氯(ClO2)与亚氯酸钠(NaClO2)都具有强氧化性。两者作漂白剂时,不伤害织物;作饮用水消毒剂时,不残留异味。某研究性学习小组利用如图装置由二氧化氯制备NaClO2·3H2O,并探究其性质。
①ClO2易与碱反应生成亚氯酸盐和氯酸盐。
②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
利用题中原理制备出NaClO2·3H2O晶体的试样,可以用“间接碘量法”测定试样(杂质与I-不发生反应)的纯度,过程如下:(已知:I2+2 =
=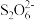 +2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现
+2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现_______ (填实验现象),达到滴定终点,共消耗该标准溶液25.00mL,经计算该试样中NaClO2·3H2O的百分含量为_______ (结果保留3位有效数字)。
①ClO2易与碱反应生成亚氯酸盐和氯酸盐。
②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
利用题中原理制备出NaClO2·3H2O晶体的试样,可以用“间接碘量法”测定试样(杂质与I-不发生反应)的纯度,过程如下:(已知:I2+2
 =
=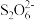 +2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现
+2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现
您最近一年使用:0次




